-
Постов
59 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные 13 лет
-
-
Все те же,что и у фенола,но анилин проявляет основные свойства
C6H5NH2+H2O=(C6H5NH3)OH
C6H5NH2+HCl=(C6H5NH3)Cl
Фенол как кислота
С6H5OH+Na=C6H5ONa+0.5H2
C6H5OH+NaOH=C6H5ONa+H2O
Общие реакции с Br,HNO3,H2
-
2AgNO3 + Na2PHO3 = 2NaNO3 + Ag2PHO3
ахаха,ОВР,конеш)
-
Вы больше доверяете экзаменационному билету, чем здравому смыслу?
)))))
-
а с этим никак не могу разобраться(((
K2CrO7 + K2SO3 + H2SO4 -> Cr2(SO4)3 + K2SO4 + H2O
Потому что K2Cr2O7
Попробуйте еще раз
-
А здесь я правильно сделал?
KMnO4+KNO2+H2SO4 ---> MnSO4+KNO3+K2SO4+H2O
2| Mn(+7) +5e -> Mn (+2)
5| N(+3) -2e -> N(+5)
2 KMnO4 + 5 KNO2 + 3 H2SO4 ---> 2 MnSO4 + 5 KNO3 + K2SO4+ 3 H2O
Да
-
железо удваивать надо. т.к. Fe2(!)(SO4)3; поэтому баланс 2/5; а не 1/5. Если у Вас 1/5 получилось, почему тогда двойка идет перед KMnO4?
Удваивают же водород да другие галогены.Никогда металлы не удваивал
По поводу K,то просто поставил т.к в правой части 2.Может,меня просто как-то по-другому учили)
Да и если посчитать по коэффициентам все правильно выходит
-
[quote name=Жеконечка
 ' timestamp='1339160680' post='666204]
' timestamp='1339160680' post='666204]1) Предположим, что NaCl полностью подвергся электролизу:
тогда выделилось по 0,05 моль Cl2 и H2
2)V(газа,получ.в результате электролиза H20)=8,96-(0,05+0,05)*22,4=6,72(л)
3) Пусть в результате электролиза воды выделилось x моль O2 и 2х моль Н2
(х+2х)*22,4=6,72 х=0,3(моль)
4)m(Cl2)=0,05*71=3,55(г)
5)m(H2)=0,05*2+0,2=0,3(г)
6)m(O2)=0,1*32=3,2(г)
7)m(полученного раствора)=117-3,55-0,3-3,2=109,95(г)
8)W(NaOH)=0,1*40/109,95=0,037
Ответ: 3,7% NaOH
так??
Интересная задача
Спасибо qerik за решение
Но я бы усомнился в ваших расчетах,если позволите,и не совсем понял ход вашего решения
(х+2х)*22,4=6,72
В данном уравнении x=0.1,а не 0.3 как у вас.Хотя вы потом подставляете 0.1 все-таки
m(H2)=(0,05+0,2)*2=0.5г
В итоге масса раствора 109.75))
Массовая доля 3.64
-
не совсем верно.
2Fe(2+)-2e = 2Fe(3+); вот почему перед KMnO4 не 1, как у Вас написано, а 2.
Простите,не понял,что вы имели в виду.
Просто сделал тоже и получилось,как у DezKa
-
Спасибо)Перерешал
-
При сгорании органического вещества массой 2г образуется 2.12г воды 6.48 углекислого газа.Относительная плотность по водороду 34
-
Да, ответ такой.
Спасибо огромное
-
То есть по сути масса воды будет 1000г?Я же так и считал в принципе,но у меня чет не сошлось.Ответ 666.6?
-
-
-
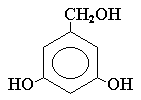
-СН2ONa
-ONa
-ONa
Название?
-
Смотря сколько натрия будет взято..
Допустим избыток
-
-
-
Нагревание смеси ацетилена, водорода и хлороводорода. Тоже бредово но придраться также не просто.
Очень бредово,я бы сказал)
-
Да нет,хлорэтан,все верно)
-
-
-
Смесь пропанола-1 и метанола массой 13.6 г обработали избытком магния.В результате реакции образовался водород объемом 3584 мл.Вычислите массовые доли спиртов в исходной смеси.
Собстно не выходит ответ.Вроде,должно быть,что водорода в обеих реакциях выделилось одинакого.1,792л,но не выходит чет.Объясните пожалуйста
Порцию трет-бутилового спирта массой обработали концентрированной бромоводородной кислотой.В результате образовался монобромид?
Что за формула у него?Просто не могу даже реакцию написать
-
CoO+H3PMoO40
Что-то,вроде,этого)Что получается
Вообще сначала получал CoO из "Кобальт углекислый основной водный" нагревая и добавив лимонную кислоту
Так вот что получится,если к оксиду добавить фосфорномолибденовую кислоту?



Задачи из неорганической химии
в Решение заданий
Опубликовано
Задача 2. Исходя из значений квантовых чисел для электронов внешнего энергетического уровня (n = 2; l = 1; ml= -1, 0, +1; ms= ±1/2, ±1/2, ±1/2), напишите электронную формулу этого элемента. Укажите его название и свойства – металл или неметалл.
Задача 7. Определите:
а) возможность самопроизвольного протекания процессов;
б) предпочтительность той или иной реакции;
в) количество тепла (кДж), которое выделится или поглотится при прохождении каждой реакции (н.у.).
Уравнения реакций:
Sn(к) + O2(г) = SnO2 (к)
Используйте
для расчетов таблицу термо
Sn(к) + 0,5O2(г) = SnO(к)
динамических характеристик веществ при стандартных условиях.
Задача 10. Во сколько раз уменьшается скорость химических реакций при понижении температуры от 40 оС до 20 оС, если температурный коэффициент γ равен трем?
Помогите,пожалуйста,с данными задачами.Не знаю,как решать их