Гена Букин
Пользователи-
Постов
73 -
Зарегистрирован
-
Посещение
Посетители профиля
2022 просмотра профиля
Достижения Гена Букин
-
С получением хлоратов уже выше разобрались. Далее есть достаточно простой способ получения перхлоратов из хлоратов, описанный во многих книгах. Это диспропорционирование хлорноватой кислоты на хлорную и диоксид хлора. Для этого можно просто присыпать хлораты щелочных металлов к серной концентрированной серной кислоте (80-90% хватит). Выделяющийся газ можно поглощать щелочами, получая попутно при этом хлориты и хлораты. Разумеется, нужно думать о технике безопасности. Присыпать хлорат понемногу, не допускать нагрева (выше 50 градусов) и скапливания диоксида хлора. Единственный недостаток - это желательно применять хлорат натрия. Из хлората калия получится перхлорат калия, из которого в дальнейшем мало что можно сделать. А в отличии от хлората калия, которого легко можно получить и очистить, хлорат натрия в чистом виде получить сложнее. Скорее всего будут примеси хлоридов, которые в кислой среде будут давать побочную реакцию с хлоратом c образованием хлора. С хлоратом натрия должно быть проще. Присыпал к серке, нейтрализовал кислоту, экстрагировал перхлорат натрия (например, ацетоном) и т.д.
-
По всей видимости, ТС спрашивает про реактивы, продающиеся не в химмагах, а в обычных магазинах, вроде хозтоваров. Есть такой вариант: достаточно разбавленный (чтобы был почти бесцветен) раствор медного купороса + нашатырный спирт. Должно получиться темно-синее окрашивание. Вполне возможно, что именно этот опыт демонстрируют в фильме "Иван Васильевич меняет профессию", когда героев пытаются машиной времени вернуть из прошлого.
-
Все правильно, добавляют. В справочнике азотчика написано, что для улучшения грануляции. А гранулированная форма менее гигроскопична. Приложу отрывок из статьи. Самый простой способ удалить нитрат аммония - прогреть. Градусов 300 должно хватить. Проверено на опыте, поначалу смесь очень сильно дымит, без хорошей вытяжки делать не стоит. Потом перестает. Не знаю насколько сильный осушитель нитрат кальция по сравнению с другими материалами, но в порошкообразной форме отсыревает на воздухе значительно быстрее нитрата аммония и превращается в лужицу. Для каких-нибудь несильных осушек может и потянет. ТГНК в статье - это тетрагидрат нитрата кальция.
-
Сам не делал. Вот ролик с Youtube, первый, что нашелся. https://www.youtube.com/watch?v=VEXJsPSZvWo А так, если нет цели лично получить химическим путем, то проще купить в том же Русхиме из верхнего сообщения.
-
Есть способы из сахарозы с азотной кислотой и из опилок со щелочью. Можно поискать в интернете. В хозяйственном можно приобрести средство Санокс с щавелевой кислотой. Которую можно попытаться осадить через оксалат железа. Последний, например, разложить натриевой щелочью до оксалата натрия, (отфильтровать гидроксид) и после обработать серной кислотой. Из-за большого количества примесей не все может пойти гладко в первой реакции. Вторые две провести несложно. В обычных хозяйственных магазинах я ни разу не видел щавелевую кислоту в составах для пчел. Хотя может где-нибудь и есть.
-
Для определения концентрации полезно приобрести ареометр, чтобы по определению плотности хотя бы примерно знать концентрацию раствора. Но в случае белизны надо помнить, что кроме гипохлорита натрия в ней так же будут содержаться (даже если это и не написано) хлорид, гидроксид натрия, а также какое-то количество хлората и карбоната натрия. И все эти в-ва также повышают плотность раствора.
-
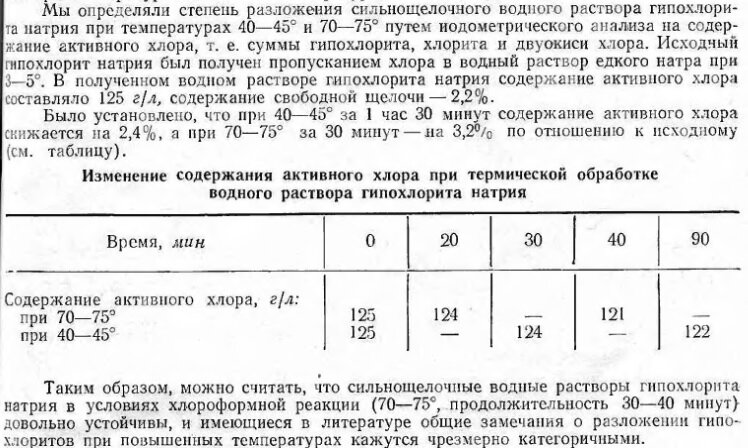
Согласен, не совсем понятно, что значит "сильнощелочные". Хотя выше в статье написано содержание щелочи (2,2%). И с тем, что надо подкислить, тоже согласен. Но даже после подкисления все равно придется несколько часов кипятить, периодически подливая воду. Из личного опыта знаю, так как сам делал таким способом, правда очень давно (в прошлом столетии), когда еще достаточно честная, концентрированная белизна продавалась. Так вот, однажды, налил в большую кастрюлю 1л белизны, аккуратно подкислил, поставил на медленный огонь и забыл. Часа через два произошел громкий хлопок. Прибегаю на кухню, сама кастрюля осталась на плите, но крышка валялась на полу и весь пол был усыпан округлыми гранулами, похожими на гранулы карбамида. Получается, что часть гипохлорита пережила не только нагрев, но и осушку. И это при температуре кипения раствора, что свыше 100 градусов. Также еще вспомнил, как примерно в те же времена делал сульфат гидразина. Из продажной белизны ничего не получалось, т.к. была слишком разбавлена. В рецептах из интернета предлагалось вымораживать воду. Но были большие потери (т.к. лед много "забирал" гипохлорита), а многократное вымораживание по чуть-чуть - ну очень утомительно. И тогда я стал быстро выпаривать белизну (естественно, уже не подкисляя) примерно в два раза или больше. И уже из такого раствора получалось до 10 грамм сульфата гидразина из 1л. исходной белизны. Т.к. что и в этом случае гипохлорит переживал кипячение, ну или точнее, большая его часть. Вот.
- 21 ответ
-
- 1
-

-
При 70оС придется не один месяц греть. Прикладываю фрагмент статьи "О термической устойчивости гипохлорита натрия". Причем там данные для концентрированных растворов NaOCl. Разбавленные - еще стабильнее.
- 21 ответ
-
- 2
-

-
-
Очень похоже по описанию на Крапивницу https://ru.wikipedia.org/wiki/%D0%9A%D1%80%D0%B0%D0%BF%D0%B8%D0%B2%D0%BD%D0%B8%D1%86%D0%B0 аллергического происхождения. У меня так было после одновременного приема 2 таблеток Имодиум. (Так что надо на всякий случай побочные действия у лекарств изучать.) Примерно через 2 суток после приема таблеток на теле быстро стали появляться волдыри в большом количестве, которые стали увеличиваться в размерах и срастаться (примерно 50% от поверхности всего тела). И еще раз также повторилось через несколько дней, но уже после 1-й таблетки. Но Супрастин быстро помог. От такой "заразы" помогают и другие более дешевые антигистаминные препараты, например, Лоратадин.
-
Лакокрасочные работы в непроветриваемых помещениях могут быть смертельно опасны. Вот первая ссылка, что выдал Яндекс: http://sredaobitaniyatv.ru/garages-killer-or-toluene-poisoning/ Со мной очень давно произошел случай, который на всю жизнь запомнился. В школе на летней практике заставили красить батареи нитрокраской. Хоть это был и обычный кабинет, а не подвал какой-нибудь, все равно надышался парами. Уже спустя несколько часов дома закружилась голова. Пошел в туалет, где сразу потерял сознание и упал на водопроводные трубы. Ладно хоть отделался ссадинами на лице, а не разбил себе чего-нибудь.
-
А что мешает парообразованию? У железоалюминиевого термита температура горения примерно 2500 градусов. А реакция с KClO3 должна идти с большим тепловыделением. Поэтому вызывает сомнение, что теплофизические характеристики у KCl настолько велики по сравнению с Fe, что он сможет поглотить столько энергии, что конечная температура будет равняться температуре кипения KCl, т.е. 1407 градусов.
-
Что-то я не совсем понял, парообразование все-таки есть или нет?
-
А вот интересно, почему некоторые считают, что реакции KClO3 с активными металлами идут без газообразования? Температура кипения KCl 1407 оС, что значительно ниже температуры реакции, так что KCl должен находится в парообразном состоянии некоторое время. Если этим фактом пренебрегать, то тогда точно также можно заявить, что и при горении водорода не образуется газообразных веществ, потому что водяной пар может конденсироваться до жидкого состояния.