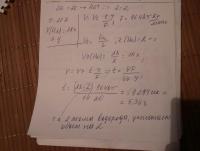ElenaLipetsk
Пользователи-
Постов
32 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент ElenaLipetsk
-
K2Cr6+2O7 + 7H2SO4 + 3Zn0→ 3Zn2+SO 4 + Cr23+(SO4)3 + К2SO4 + 7Н2О Cr6+ -3e = Cr 3+ I 2 окислитель Zn 0 + 2e = Zn 2+ I 3 восстановитель K2Cr6+2O7 + 6Fe2+SO4 +7H2SO4→ Cr23+(SO4)3 + 3Fe23+(SO4)3 + К2SO4 + 7Н2О Cr6+ -3e = Cr 3+ I 1 окислитель Fe2+ + 1e = Fe 3+ I 3 восстановитель Здравствуйте! Теперь всё верно?
-
Закончить уравнения реакций, составить электронные уравнения, расставить коэффициенты, указать окислитель и восстановитель в каждой реакции: а) K2Cr2O7 + H2SO4 + Zn→ ZnSO 4 + Cr2(SO4)3 +K ; б) K2Cr2O7 + FeSO4 +H2SO4→ K. Решение: K2Cr2O7 + 7H2SO4 + 3Zn→ 3ZnSO 4 + Cr2(SO4)3 + К2SO4 + 7Н2О 2К+ + 2Сr6+ + 7O2- + 7H+ + SO2-4 +3 Zn0 = 3Zn2+ + SO2-4 + 2Cr3+ + 3SO2-4 + 2K+ + SO2-4 + 7H2O 7O2- + 7H+2 = 7H2O Cr6+ -3e = Cr 3+ I 2 окислитель Zn 0 + 1e = Zn 2+ I 3 восстановитель K2Cr2O7 + 6FeSO4 +7H2SO4→ Cr2(SO4)3 + 3Fe2(SO4)3 + К2SO4 + 7Н2О 2К+ + 2Сr6+ + 7O2- + 6Fe2+ + 6SO2-4 +7H+2 + 7SO2-4 = 2Cr3+ + 3SO2-4 + 6Fe3+ + 9SO2-4 + 2K+ +SO2-4 + 7H2O 7O2- + 7H+2 = 7H2O Cr6+ -3e = Cr 3+ I 1 окислитель Fe2+ + 1e = Fe 3+ I 3 восстановитель
-
Какое соединение образуется при прокаливании негашеной извести с углем? Что является окислителем и восстановителем в этой реакции? Составить электронные и молекулярные уравнения. CaO + C⁰ ⇒ CaC₂⁻ + C⁺²O C⁰ +e⁻ ⇒ C⁻ 1 C⁰ -2e⁻⇒ C⁺² 2 C⁰ +e⁻ окислитель C⁰ -2e⁻ восстановитель CaO + 3C = CaC₂ +CO
-
Указать окислитель, восстановитель и подобрать коэффициенты в уравнениях: PbO2 + Mn(NO3)2 + HNO3 →Pb(NO3)2 + HMnO 4 + H2O ; Al + K2Cr2O7 + H2SO4 →Al 2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O . 5PbO2+2Mn(No3)2+6HNO3=5Pb(NO3)2+2HMnO4+2H2O Pb(+4) +2e=Pb(+2) |5 - окисл. Mn(+2) -5e=Mn(+7) |2 - восстан. 2Al+K2Cr2O7+6H2SO4=Al2(SO4)3+Cr2(SO4)3+K2SO4+3H2O Al(0) -3e=Al(+3) |3|1 -восст. Cr(+6) +3e=Cr(+3 )|3|1 - окисл.
-
ЭДС рассч-ся по ур-ю: ЭДС = Е катода - Е анода, а Е в свою очередь - по ур-ю Нернста: E = E0+1.984*10^-4*(T/z)*lg А, где E0 - станд-й элек-й пот-л (Ag/Ag+ = +0.799 В), Т - темп-ра в К (станд-е усл-я 25 С = 298 К), z - заряд иона Men+ и А - активность ионов; считаем, что в данном случае активность ионов Ag+ равна 1, а поскольку Ag+ - 1-зарядный ион (z = 1), т.е. Сн=Сm;
-
Спасибо, всё поняла! пот-л 1 элек-да сос-т Е1 = +0.799+1.984*10^-4*(298/1)*lg 0.01 = 0.6216304 В; б) пот-л 2 элек-да - соот-но Е2 = +0.799+1.984*10^-4*(298/1)*lg 0.1 = 0.740 В; поскольку Е2>Е1, то Е2 - катод (+), а Е1 - анод (-). А в проверочном калькуляторе получается 0,682 В и 0,741 В , что я делаю не так?
-
Посмотрите, пожалуйста, правильно ли я решила задачу.
ElenaLipetsk опубликовал тема в Решение заданий
Какой гальванический элемент называется концентрационным? Составить схему, написать электронные уравнения электродных процессов и вычислить эдс гальванического элемента, состоящего из серебряных электродов, опущенных: первый − в 0,01н, а второй − в 0,1н растворы AgNO3. Ответ: 0,058 В. Решение: Концентрационный элемент - это гальванический элемент, состоящий из двух одинаковых металлических электродов, опущенных в растворы соли металла с различными концентрациями. Катодом в этом случае будет являться электрод с большей концентрацией. (+) Ag I AgNO3 0.1 II 0.01 AgNO3 I Ag (-) A: Ag 0 -1е = Ag + K: Ag + +1e = Ag 0 E=(0.058/z)* (C1/C2)= (0.058/1)*lg(0.1/0.01)=0.058 B -
Посмотрите, пожалуйста, правильно ли я решила задачу.
ElenaLipetsk опубликовал тема в Решение заданий
Жѐсткость воды, содержащей только гидрокарбонат магния, равна 1,94 м-экв/л. Определить массу гидрокарбоната магния в этой воде. Решение: В 1л.воды содержится 1,94*1=1,94 ммоль-экв. или 0,00194 моль-экв.солей гидрокарбоната магния. Найдём массу Mg(HCO3)2 = 81 г/моль * 0,00194 моль = 0,157 г. 81 г/моль - молярная масса эквивалентов гидрокарбоната магния. Ответ: m(Mg(HCO3)2)=0.157 г. -
Спасибо!
-
Здравствуйте! Посмотрите теперь всё верно? Извините, что изображение боком, не получилось повернуть.
-
-
-
В течение какого времени необходимо пропускать электрический ток силой 20 А через раствор соляной кислоты, чтобы выделилось 28 л водорода (н. у.)?