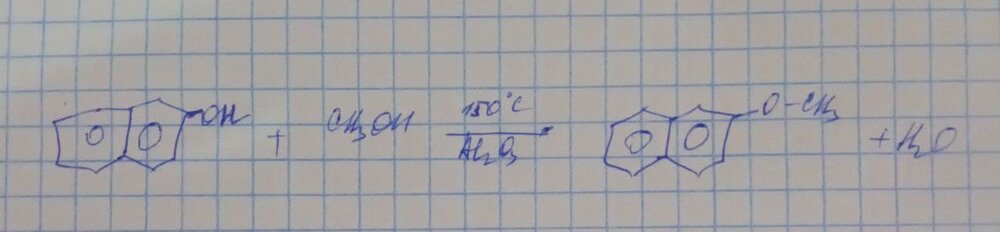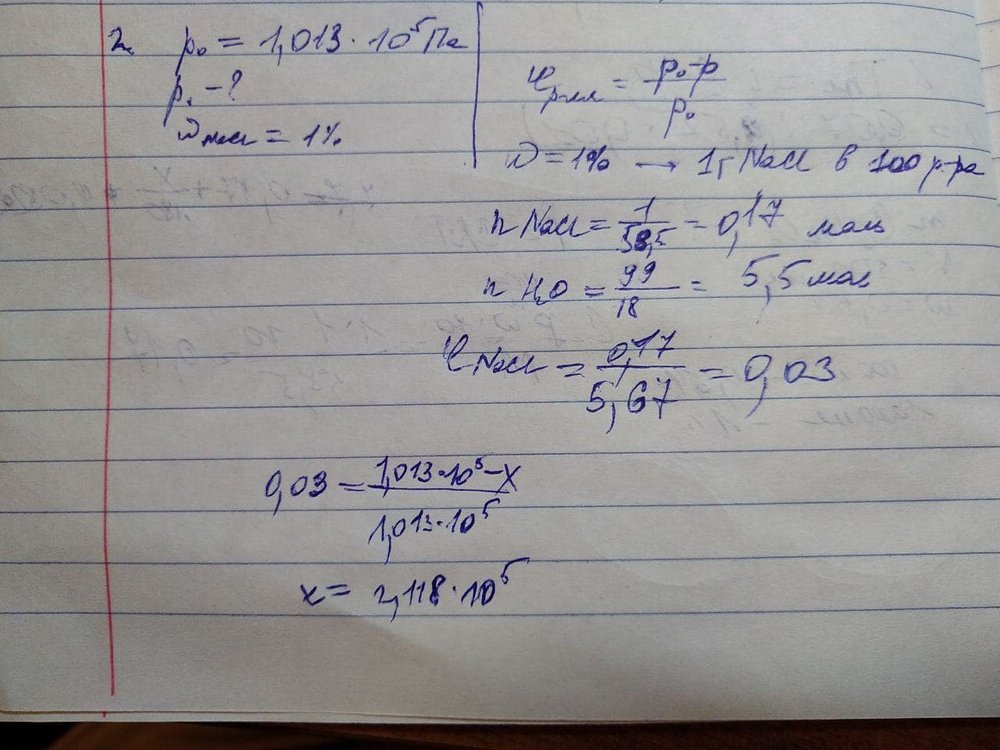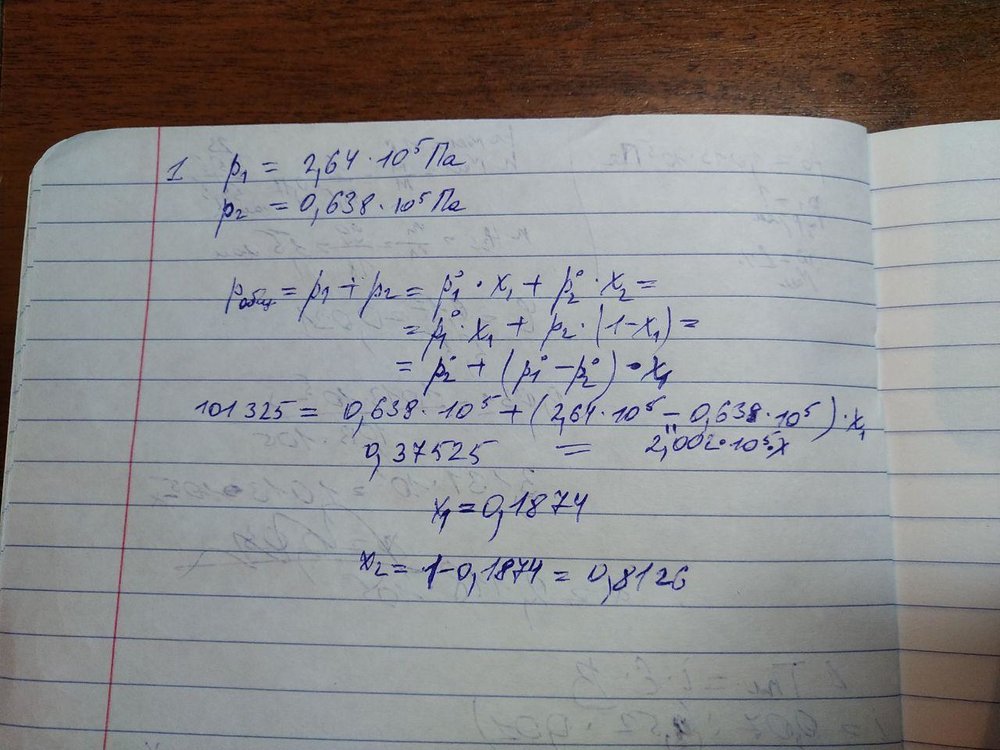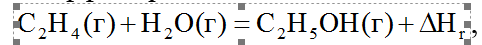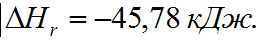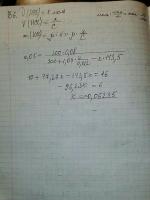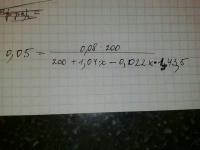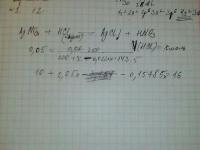-
Постов
78 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент vitaliusik
-
-
Здравствуйте! Помогите решить задачу по аналитической химии, мне уже скоро сдавать нужно, время на раздумья дали мало.
-
В четыре пробирки налейте небольшие объемы растворов иодида, бромида, хлорида и фторида калия. Во все пробирки прибавьте немного (2-3 капли) раствора нитрата серебра. Отметьте цвет образующихся осадков. Повторите опыт, предварительно наполнив пробирки на ¾ водой, добавив в каждую пробирку с соответствующими галогенидами калия 2-3 капли нитрата серебра. Можно ли теперь по цвету осадков определить, какой галогенид образуется? После опытов содержимое пробирок вылить в специальную банку для серебряных отходов. Как добавление воды повлияет на цвет осадка?
-
Доброго времени суток, помогите пожалуйста решить задачу, мое неверное решение прикрепил. Ответ: 6,3*10^2 Давление насыщенного водяного пара при нормальной температуре кипения воды (373К) равно 1,013*10^5 Па. Рассчитайте, насколько ниже давление пара на 1% раствором хлорида натрия при 373К, предполагая, что этот раствор является идеальным.
-
Помогите разобраться, что я делаю не так, в чем ошибка. Решения именно такого рода задач нет в интернете Прикрепляю условие и ход своих мыслей, итог которых не совпадает с ответом Условие в конце страницы под номером 1.
-
Вычислите тепловой эффект реакции если теплоты образования этилена, водяного пара и газообразного этанола соответственно равны 52,28 кДж/моль; –241,8 кДж/моль; –235,3 кДж/моль. Ответ: При вычислении теплового эффекта по следствию из уравнения Гесса не сходится с ответом. Для решения методом термохим уравнений нужны промежуточные реакции. Подскажите, пожалуйста, как выйти из ситуации.
-
Помогите пожалуйста! Текст задачи: В два раствора серной кислоты добавили одинаковые количества цинка. В одном растворе выделилась сера, в другом - сероводород. После завершения всех реакций массы растворов оказались равны. Сравните массы и концентрации исходных растворов. Моё решение:
-
Текст задачи: В два раствора серной кислоты добавили одинаковые количества цинка. В одном растворе выделилась сера, в другом - сероводород. После завершения всех реакций массы растворов оказались равны.Сравните массы и концентрации исходных растворов. Не получается решить, кто как думает?
-
Не понимаю как такое решать, подскажите пожалуйста. Текст задачи: Для полного гидролиза сложного эфира, образованного насыщенной одноосновной кислотой и насыщенным одноатомным спиртом, требуется 9,9 г воды. При сгорании такого же количества сложного эфира образуется CO2 объемом 86,24 дм3 (н. у.). Укажите максимально возможную разницу молярных масс (г/моль) продуктов гидролиза.
-
Нужно без промежуточных стадий осуществить данное превращение. Помогите пожалуйста. NaCl --> ZnCl2
-
HBrO3 + 5HBr = 3H2O + 3Br2 K = n(H2O)3 + n(Br2)3 / n(HBrO3) * n(HBr)5 n = m/M Не хватает масс веществ в условии?
-
Всем огромное спасибо!
-
Спасибо всем огромнейшее!
-
Опечатка. Там
-
Как такое дело обстоит с неизвестными газами? Текст задачи: В смеси газов А и Б массовая доля газа А равна 48%, а его объемная доля - 18,75%. Укажите относительную площадь газа А по газу Б.
-
Я правильно вас понял: по закону сохранения массы расписываем m(AgNO3)+m(HCl)=m(AgCl)+m(оставшегося AgNO3) Где масса HCl=n*p/C=p*V (ню*плотность:молярную концентрацю=плотность*объём=масса раствора HCl). Дальше что такое 20*(16-х*169,87)? 16-х*169,87 - масса оставшегося AgNO3. А что такое 20? Должно же быть m(р-ра)=m(в-ва)/w, где w-массовая доля нового 5%-ного раствора. То есть должно быть +(16-х*169,87)/0,05 А ещё почему мы не учитываем массу HNO3? Почему уравнение составляется не по такой схеме: m(AgNO3)+m(HCl)=m(AgCl)+m(HNO3)+m(оставшегося AgNO3)?
-
-
Как использовать плотность раствора для нахождения этой массы? Так? Четвёртое действие не понимаю Как молярную концентрацию использовать для нахождения объема?
-
-
А как найти объем? Что-то до меня не доходит
-
На сколько мне известно, это формула - C=n/v
-
Как через объём HCl выразить массу AgCl, используя молярную концентрацию и плотность хлороводорода?
-
HCl получается в недостатке?
-
Как получили 6 грамм? Не понимаю
-
Не понятно выражение "осадить разницу между этими процентами". В условии исходная массовая доля 8% и полученная массовая доля 5 %. Объясните, пожалуйста, что вы имеете в виду. Массу какой соли посчитать? AgCl? По массе AgNO3 считать? Как можно сделать такой вывод, не зная, что взяли в недостатке AgNO3 или HCl