-
Постов
1374 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Бертолле
-
-
если у кого есть методика получения о-нитробензилхлорида (бромида) скиньте пожалуйста, нужна для курсовой работы
-
Да, из орто-нитробензилхлорида. С натриймалоновым эфиром он будет на ура реагировать - тут никаких сложностей быть не должно. Берёте любую методику с малоновым эфиром и галогенидом (в руководствах и практикумах такую методику найти несложно). Труднее будет получить сам орто-нитробензилхлорид, если его из банки нельзя взять.
спасибо за информацию, мы вот сегодня только прошли дикарбоновые к-ты и синтезы с малоновым эфиром, так что теперь имею четкое представление что к чему
а с нитробензилхлоридом думаю придется повозиться, да и предельная осторожность нужна при его получении, как раз следом лабораторная по нитрованию, думаю может сразу это вещество дадут и получу его тогда уж
-
А чем Вам не нравится с малоновым эфиром синтез? Ссылку Вам же дали. Правда, Берихьте найти в электронном виде очень сомнительно - надо в библиотеках искать.
Хотя, я бы попробовал по аналогии сварить, по методике малонового синтеза с каким-нибудь бензилхлоридом, или - чем-то подобным..
я кажется начинаю понемногу въезжать, то есть можно исходить из 2-(нитробензил) молоновой кислоты диэтилового эфира? (ну или хлорбензила) а как онный реактив получить?
все, реакцию эту кажется разобрал, но остается вопрос, как же все таки получить этот диэтиловый эфир 2-(2-нитробензил) малоновой кислоты?
нужно исходить из орто-нитробензилхлорида?
-
А чем Вам не нравится с малоновым эфиром синтез? Ссылку Вам же дали. Правда, Берихьте найти в электронном виде очень сомнительно - надо в библиотеках искать.
Хотя, я бы попробовал по аналогии сварить, по методике малонового синтеза с каким-нибудь бензилхлоридом, или - чем-то подобным..
а как синтез с малоновым эфиром выглядит? по тому файлу, что сверху кто-то прикрепил, ничего особого не дал, там же толком нет ничего
-
Это 3 карбоновая кислота
Делал похожую штуку, в смысле, 1,2,3,4-тетрагидро-2-хинолон замещеный перегруппировкой Бекмана соответствующего оксима инданона.
боюсь, что, если осуществлять данную перегруппировку в моем случае, то нужно будет исходить из не очень, мягко говоря, доступного вещества
-
неужели нет ни у кого никаких версий, где можно найти методику получения сего препарата из индола, хотя бы эту, а там от нее двигаться уже, проблема в том, что нужно исключить из используемых реактивов уксусный ангидрид, но я не могу даже с ним методу найти
-
Это 3 карбоновая кислота
Делал похожую штуку, в смысле, 1,2,3,4-тетрагидро-2-хинолон замещеный перегруппировкой Бекмана соответствующего оксима инданона.
хотите сказать мне от сюда копать нужно, а можно поподробнее про метод
Поищите по Бейльштейну.Желательно бы увидеть её формулу. приложите фото или скан.
Поищите по Бейльштейну.Желательно бы увидеть её формулу. приложите фото или скан.
а Бельштейн это что, книга или что-то другое? можете скинуть или ссылку дать
-
-
Нужно синтезировать соединение 2-оксо-1,2,3,4-тетрагидро-4-хинолин карбоновую кислоту (вроде бы в названии не запутался)
никак не могу найти различные методики синтеза, слышал про методику, где используется уксусный ангидрид, мне ее желательно заменить, из-за нежелательности использования последнего, но хотелось бы хотябы взглянуть на саму методику, что бы было от чего отталкиваться
как прикрепить файл или как вставить нарисованную формулу теперь не понятно
-
тем более) Бертолле, а кто по твоему должен встать у руля или, может быть, вообще никто из нынешних.
мне кажется из нынешних никто ничто принципиального не сделает, такая же разруха будет, а то и хуже, так что трудно сказать...
-
нет ..... , 115.35% - нормально...
это еще по-божески, так сказать
в Ростовской области получилось около 140%, по-моему даже в большую сторону
-
Да вы что имеете ввиду фальсификацию?
да про это по-моему каждый знает, http://www.youtube.com/watch?v=7_SAUXJDzVc
причем это все так по телевизору показывали, остается только взять в руки калькулятор...
-
не удивлюсь, если будут точно такие же выборы, как выборы в 2011 году, когда в сумме по областям по 130-140% было, и как ни странно выиграли единоросы, так что здесь скорее всего тоже самое будет, у нас не будет честных выборов, это уже по-моему каждому известно, так что победит Путин
-
интересная формула) вот бы получить такую...
из интересных формул: мне кажется, интересны катенаны, то есть грубо говоря кольцо в кольце, член их класса - олимпиадан представляет собой циклы, которые похожи на олимпийские кольца
-
Вы лучше скажите - где Вы откопали такого кадавра? "Эпокси" - означает эпоксид (эпоксиэтан, к примеру), "оксиран" - это систематическое название собственно - эпоксиэтана Получается какое-то масло маслянное, да ещё и 3,4.
автор видимо не так выразился, он видимо имел ввиду класс соединений, содержащих трехчленный гетероцикл с атомом кислорода, т.е. эпоксиды, под названием оксиран видимо имел ввиду именно их, так как так их изредка называют, я сам встречал в некоторых источниках такое название
-
По заданным термохимическим уравнениям рассчитайте при Т = 298К стандартные энтальпию, энтропию и энергию Гиббса образования Се2О3
а) Се(т) + О2(г) = СеО2(т) ΔH = -1090, ΔS = -219 , ΔG = -1025
б) 3СеО2(т) + Се(т) = 2Се2О3(т) ΔH = -332, ΔS = +34 , ΔG = -342
Как здесь решать? Энтальпию первой реакции умножить на 3 и прибавить энтальпию второй реакции Это будет ответ?
По энтропии и Эн Гиббса в том же порядке?
Именно так, как пишешь, верно мыслишь, мы точно так же в универе решаем эти задачи
-
Помогите, пожалуйста, записать правильные уравнения и уровнять их ионно-электронным методом.
Mo + H2O =>(t=700C) MoO2 + H2
Mo + H2SO4(конц) => H4[Mo(SO4)O4]
Mo + H2SO4(разб) => реакции нет
Mo + HNO3(конц) --> MoO3 ?
Mo + NaOH --> Na2MoO4 + H2 ?
с концентрированной серной можно и так, как я выше написал, так даже лучше быдет, что бы не углубляться в подробности, это так для справки
с гидроксидом натрия при СПЛАВЛЕНИИ И В ПРИСУТСТВИИ ОКИСЛИТЕЛЯ! т.е.
NaOH + Mo + O2 --t*C--> Na2MoO4 + H2O
c азотной ---> NO + MoO3 + H2O
-
Добрый день!Я собираю старые банкноты,и вот мне попались несколько экземпляров на которых есть пятна чернил.Не подскажите мне как и чем можно смыть эти чернила не повредив банкноты.Заранее спасибо
поищите на ютубе, там есть видео по поводу снятия чернил; из реактивов нудны только р-р перманганата калия, уксуса и пероксида водорода
-
Нужна помощь в составлении уравнений реакций взаимодействия молибдена(Mo) с H20, H2SO4(конц. и разб.), HNO3(конц. и разб.)и NaOH.
Мои результаты:
Mo + H2O => реакции нет
Мо + H2SO4(конц) --> MoSO4 + H2O + S(H2S)
Мо + H2SO4(разб) --> MoSO4 + H2
Mo + HNO3(конц) --> MoNO3 + H2O + NO2
Mo + HNO3(разб) --> MoNO3 + H2O + N ?
Mo + NaOH --> ?
Не могу понять, как определять что восстановитель, а что окислитель. Из-за не получается уровнять методом полуреакций. Объясните, пожалуйста на примере реакций.
во-первых с молибденом не так все просто, как с другими металлами, он не похож на них тем, что практически не образует простых солей, а в основном только комплексные соли
во-вторых у вас не указанны условия реакций
тогда с водой молибден реагирует при 700*С давая диоксид
с концентрированной серной получается р-р, грубо говоря MoO2SO4 (на самом деле опять же таки комплексное соединение H4[Mo(SO4)O4])
с разб. серной реакции нет
с азотной кислотой получится триоксид, оседающий на поверхности металла, следовательно, р-я медленная
дымящей азотной пассивируется
с гидроксидом натрия при сплавлении в присутствии окислителя (вы же условия не указали) будет молибдат натрия Na2MoO4
-
Железо тоже нужно, только не сталь, чистое в форме гранул, слитка, чешуек, кусочков, чтобы было видно металлический блеск.
Все остальные элементы интересуют в такой же форме. Просто нет возможности расплавить ничего серьезнее алюминия
 Большие количества не нужны, не больше пенницилинового флакона. Цены предлагайте ваши.
Большие количества не нужны, не больше пенницилинового флакона. Цены предлагайте ваши.алюмотермия и электролиз в помощь, если грамотно сделать, то и ввиде кусков можно так получить хром, а там и никель, кобальт из оксидов алюминием вытеснить и другие металлы средней активности, так что дерзайте и удачи в поисках элементов
-
Проблемка... В синтезе: CuO + Р2О5 = получим примесь полифосфатов.
А по поводу водных растворов. Если с одной стороны взять Na3PO4, то получится примесь основной соли (из-за щелочной среды). С другой стороны если взять Na2HPO4, то получим примесь CuHPO4, который вероятно тоже нерастворим и выпадет в осадок.
Хотя... всегда есть равновесие НРО4(2-) = РО4(3-) + Н(+). Посмотрите ПР для Cu3(PO4)2 и CuHPO4. Какой из ПР меньше, та соль и выпадет при добавлении раствора Na2HPO4.
Другой вариант - взять раствор соли (NH4)3PO4. У него рН не щелочной, значит не будет примеси основной соли. Хотя... вероятно будет примесь двойного фосфата аммония-меди. То есть тут тоже надо ПР смотреть.
думаю если плавить оба оксида вместе, там еще хлеще, чем полифосфаты получатся, типа стекол каких-нибудь, нестехиометрия, эвтектика и прочее
только вот средний ортофосфат аммония не существует в водном р-ре..
а вопрос интересный на самом деле, ответа на него нет нигде, да и инфы очень мало
Есть еще одно извращение - окислить фосфид меди Cu3P2. Вот только чем? Может персульфатом аммония?
Или нагреть Cu3P2 и продувать кислород.
это уже слишком, хотя вариант
-
Вот и я не знаю. Да и с нитратом меди - проблема. Его ведь в безводном виде получить не так просто.
здесь только экспериментировать придется, а что если попробовать по реакции гидроксида меди с ортофосфорной кислотой, так скажем напрямую, хотя и не исключается образование кислых солей, но попробовать стоит
а по обычной реакции обмена между ортофосфатом образование основных солей гарантированно из-за слишком высокой pH среды
-
спасибо за наводку, теперь все нормально
-
А почему у меня некоторые темы, в которых я отвечал пропадают после нажатия кнопки "Просмотр новых сообщений"? Например, тема "Получение ортофосфата меди"




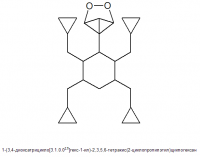
Получение эфиров
в Решение заданий
Опубликовано
Есть ли у кого много информации по получению и химическим свойствам сложных эфиров? Очень нужною