:))
Пользователи-
Постов
19 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент :))
-
100 г этилового и 100 г метилового спиртов образуют идеальный раствор, найдите давления паров каждого из спиртов над раствором при 20°С, если при этой температуре давление паров над чистым метанолом составляет 88.7 мм рт. ст., а над чистым этанолом - 44.55 мм рт. ст. Определите также мольные доли метилового спирта в растворе (Х) и в паре над ним Рассчитайте значения функций смешения при приготовлении этого раствора при температуре 20°С. По закону Рауля получается,что мольная доля метанола равна x 760= 44,55 + (88,7-44,55)*X Но тогда получается, что мольная доля больше единицы((( Помогите, пожалуйста
-
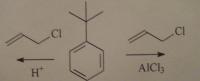
Объясните причину образования нестандартного продукта в этой реакции. Приведите механизм этого превращения.
-
Энергия Гельмгольца одного моля некоторого в-ва записывается уравнением F= a+ T (b-c-blnT-glnV), где a, b, c,g - константы. Найдите давление, энтропию и теплоемкость Cv этого тела Я решила так dF=dG- pdV dH=pdV=dG-F= dG - d(a+ T (b-c-blnT-glnV))=dG- d(a+Tb-Tc-TblnT-glnV)= dG-b+c+b-g/V как дальше упростить, если это верно? p=(dG-dF)/dV как дальше? что делать с теплоемкостью?
-
Рассчитайте абсолютную энтропию 2 моль паров SO2Cl2 при температуре 100*C и давлении 0,2 атм, если известно следующее температура испарения жидкого SO2Cl2 = 69*С, стандартная энтальпия испарения при этой температуре равна 30,4 кДж/моль, S(0, 298,ж)=217,2 Дж/моль К,теплоемкости Cp можно считать не зависящими от температуры, их значения для жидкого и газообразного SO2Cl2 составляют соответственно 131,8 и 77,4 Дж/моль К Не очень понятно, по предоставленным данным можно рассчитать только изменение энтропии, но не абсолютное значение, для этого нужны еще величины температуры плавления... Не понятно, зачем дана энтальпия Объясните, пожалуйста, ход решения
-
Рассчитайте абсолютную энтропию 2 моль паров SO2Cl2 при температуре 100*C и давлении 0,2 атм, если известно следующее температура испарения жидкого SO2Cl2 = 69*С, стандартная энтальпия испарения при этой температуре равна 30,4 кДж/моль, S(0, 298,ж)=217,2 Дж/моль К,теплоемкости Cp можно считать не зависящими от температуры, их значения для жидкого и газообразного SO2Cl2 составляют соответственно 131,8 и 77,4 Дж/моль К Не очень понятно, по предоставленным данным можно рассчитать только изменение энтропии, но не абсолютное значение, для этого нужны еще величины температуры плавления... Не понятно, зачем дана энтальпия Объясните, пожалуйста, ход решения
-
Энергия Гельмгольца одного моля некоторого в-ва записывается уравнением F= a+ T (b-c-blnT-glnV), где a, b, c,g - константы. Найдите давление, энтропию и теплоемкость Cv этого тела Я решила так dF=dG- pdV dH=pdV=dG-F= dG - d(a+ T (b-c-blnT-glnV))=dG- d(a+Tb-Tc-TblnT-glnV)= dG-b+c+b-g/V как дальше упростить, если это верно? p=(dG-dF)/dV как дальше? что делать с теплоемкостью?
-
Рассчитайте абсолютную энтропию 2 моль паров SO2Cl2 при температуре 100*C и давлении 0,2 атм, если известно следующее температура испарения жидкого SO2Cl2 = 69*С, стандартная энтальпия испарения при этой температуре равна 30,4 кДж/моль, S(0, 298,ж)=217,2 Дж/моль К,теплоемкости Cp можно считать не зависящими от температуры, их значения для жидкого и газообразного SO2Cl2 составляют соответственно 131,8 и 77,4 Дж/моль К
-
Определить поверхность раздела фаз (S) в 1 л пивной пены, если ее кратность составляет l =100, а диаметр пузырьков 250мкм. Кратность пены – это отношение общего объема пены к объему жидкости: l = Vпены/Vжидкости
-
Как соотносятся удельные поверхности (s* = S/V) наноразмерных объектов: 1 – пленки, площадью 1х1 м. толщиной 10 нм; 2 – нитей, сечением 10х10 нм и длиной 1 м; 3 – нитей цилиндрической формы длиной 1 м и радиусом 10 нм; 4 - кубических частиц с ребром 10 нм; 5 - сфер радиусом 10 нм ?
-
Определить поверхность раздела фаз (S) в 1 л пивной пены, если ее кратность составляет l =100, а диаметр пузырьков 250мкм. Кратность пены – это отношение общего объема пены к объему жидкости: l = Vпены/Vжидкости
-
Как соотносятся удельные поверхности (s* = S/V) наноразмерных объектов: 1 – пленки, площадью 1х1 м. толщиной 10 нм; 2 – нитей, сечением 10х10 нм и длиной 1 м; 3 – нитей цилиндрической формы длиной 1 м и радиусом 10 нм; 4 - кубических частиц с ребром 10 нм; 5 - сфер радиусом 10 нм ?
-
Спасибо большое) а как это определить? исходя из констант кислотности или как-то еще?
-
В серной кислоте растворены кислоты HCl, HNO3, CH3COOH. Укажите самый сильный донор протонов в этих растворах. Заранее спасибо)
-
Подскажите, пожалуйста, алгоритм решения следующих задач В качестве растворителя использовали серную кислоту, константа автопротолиза 1,59 * 10^(-4) Какое значение рН соответствует точке нейтральности? В серной кислоте растворены кислоты HCl, HNO3, CH3COOH. Укажите самый сильный донор протонов в этих растворах. Заранее спасибо)