-
Постов
67 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные teakkat
-
-
Для получения метанола на низкотемпературном катализаторе при 563 К и 5-10 МПа подберите тип реактора, приведите его эскиз, опишите конструкцию и метод расчета. Подберите материал для изготовления реактора и дайте обоснование этого выбора.
Выбрала реактор шахтного типа.
Какой метод расчета будет? Откуда можно взять и насколько подробно это нужно описывать? Помогите, пожалуйста.
-
В задаче необходимо на основании данных таблицы определить зависимость увеличения веса стального образца в сероводороде при температуре 250 градусов Цельсия от времени окисления.
время, час 90 180 270 360 450 540
увеличение массы, г/м2 72 134 167 215 255 270
если строю графики (p-t), (p-t^1/2), (p-lg(t)) все они получаются ломаные, как найти эту зависимость не понимаю. Тем более что зависимость вроде как ищется по толщине пленки - времени... Помогите, что делать?
-
-
Большое спасибо!скорее всего имелось ввиду "для чего предназначен каждый из компонентов?"
Что дает глюкоза в среде? энергию, пептон - аминокислоты, морская (именно морская!) соль - макро- и микроэлементы, дрожжевой эк-т - витамины и факторы роста
загуститель (агар, желатина, акрилат) есть? нет, значит среда жидкая, скорее всего накопительная
-
Охарактеризуйте питательную среду для культивирования простейших (г/100 мл): глюкоза - 0.5; пептон -0,2; морская соль -0,1; дрожжевой экстракт - 0.1 мл по составу и физическому состоянию. Как вообще нужно выполнить это задание? что-то считать? может есть какие-то подобные примеры. любая помощь пригодится.
-
Задание. Покажите как будет влиять на константу скорости жидкофазной реакции S2O82-+2I- -> I2+2SO42-
увеличение диэлектрической проницаемости среды, в которой протекает реакция. Подскажите, как это выполнить, пожалуйста
-
Как объяснить, что дзета потенциал уменьшается?
-
Золь иодида серебра получен смешанием равных объемов иодида калия и нитрата серебра. Пороги коагуляции для различных электролитов имеют следующие значения:
Ca(NO3)3 - 315
NaCl- 300
MgCL2 - 320
Na3PO4 -0,6
Na2SO4 - 20
AlCl3- 330. Какой из электролитов иодид калия или нитрат серебра взят в большей концентрации для приготовления золя? Нужен обоснованный ответ.
Уравнение реакции
AgNO3+KJ -> AgJ +KNO3
По значениям порогов коагуляции можно сделать следующие выводы.
У солей NaCl, Na3PO4,Na2SO4, имеющих одинаковые катионы значения порогов коагуляции различаются значительно, в то в время как у заданных хлоридов (с одинаковым анионом) они близки по значению. Значит коагулирующими ионами в растворе являются анионы, и следовательно мицелла золя заряжена положительно.
Записав формулу мицеллы, пишем, что Нитрат серебра взят в большей концентрации.
Подскажите, я правильно думаю? достаточно такого объяснения? Для чего дан порог соли кальция?
-
хотя бы в общем подскажите, о чем писать. Спасибо!
-
Задача по ПАХТ. Вычислить коэффициент теплопроводности 30% водного раствора хлористого кальция, удельная теплоемкость которого равняется 2,72*103 Дж/кг К
По нормограмме удельной теплоемкости, обратным ходом я определила, что температура жидкости -36 0 С. В данной мне таблице есть также плотность 25% водного раствора CaCl2 1195 кг/м3 при температуре от 0 до 20 градусов. Помогите, пожалуйста, найти плотность, которую нужно взять для дальнейшего накождения теплопроводности
-
-
Я вот нашла что-то про эффект Караша и радикальный механизм реакции при присоединении галогеноводородов к алкенам. Тогда получается
BrCH2-CH=CH2+HBr =>BrCH2-CH2-CH2Br (в присутствии перикиси)
Далее гидролиз галогеналкана, содержащего более одного атома галогена в молекуле
........................................ H2O
BrCH2-CH2-CH2Br +2NaOH = > CH2OH-CH2-CH2OH+2NaBr+2H2O
Может так можно?
-
задание как в первом сообщении в виде формул(пропандиол-1, 3), тема - радикальные реакцииBr- электроноакцепторный заместитель. Присоединение воды пойдет против Марковникова, а затем гидролизовать -Br.
Хотя что-то я сомневаюсь, а в чём - не пойму. Вроде, всё элементарно.
-
как из CH2=CH-CH2Br получить HOCH2CH2CH2OH?
-
Известно, что простые эфиры достаточно инертны в реакциях замещения SN1 и SN2. Однако, многие из них расщепляются при обработке концентрированной HI. В то же время с NaI эфиры не реагируют. Объясните, пожалуйста, эти факты.
Нашла следующее (своими словами): при насыщении простых эфиров иодистым водородом происходит расщепление связи между атомами углерода и кислорода. Это можно рассматривать как реакцию нуклеофильного замещения по Sn2-механизму. Иодоводород в реакции действует как источник нуклеофила в виде иодид-аниона. В результате того, что кислородный атом простого эфира присоединяет протон, частично положительный атом углерода в протонированной молекуле становится еще более положительным и поэтому более доступным для нуклеофильной атаки. Что написать про иодид натрия?! Подскажите, пожалуйста
-
в условиях какой реакции можно осуществить замещение RCl+F-=> RF+Cl-? Объясните
-
Подскажите, как ответить на теоретический вопрос контрольной:
Влияние вида изотерм сорбции на форму выходных кривых в колоночной и плоскостной хроматографии. Рекомендации для практической работы.
Здесь какой-то общий ответ? или для колоночной и плоскостной есть различные особенности? Может ссылку подскажите... Спасибо!
-
В задаче требуется рассчитать максимальное колебательное квантовое число и энергию диссоциации молекулы NO на основе справочных данных. В справочнике напротив NO стоит две строки
ωе=1916.54, xeωe=14.424
ωе=1906.43, xeωe=14.454
какой же x мне брать для расчетов? И почему строки две? Объясните, пожалуйста!
-
 1
1
-
-
Построить диаграмму кипения бинарной смеси н-гексан (Нормальная температура кипения 341,9 К, ΔHисп=28,89*106 Дж/Кмоль ) - н-гептан (Нормальная температура кипения 371,4 К, ΔHисп=31,74*106 Дж/Кмоль ) при давлении 1,01325*105Па. системы считать идеальными.
Есть примечание. Для решения задачи необходимо определить составы равновесных фаз (пара и жидкости) при нескольких температурах в интервале температур кипения низкокипящего и высококипящего компонентов системы.
Как определить эти составы в данном случае?
-
Теплота образования газообразного этилена при 298 К и давлении 101,325 кПа равна 52,3 кДж/моль. Зная стандартные теплоты образования жидкой воды и газообразного диоксида углерода, определить теплоту сгорания этилена при
1) P=const;
2) V=const и T=298 К.
Решение:Из справочникаΔHобр(H2O(ж))=-285,8 кДж/мольΔHобр(CO2(г))=-393,5 кДж/моль1) Тепловой эффект химической реакции в изобарном процессе (P=const).Qp=ΔU+pΔV=-ΔH – изменение энтальпииОпределим изменение энтальпии реакции по закону Гесса.C2H4(г)+3O2(г) ->2CO2(г)+2H2O(ж)52,3 0 -393,5 -285,8 - энтальпия образования, кДж/мольΔH2980=(2*(-393,5)+2*(-285,8)) – (52,3+0)=-787-571,6-52,3=-1410,9 кДжКоличество теплоты при сгорании одного моля этиленаQp=- ΔH2980=1410,9 кДж2) Тепловой эффект химической реакции в изохорном процессе (V=const)QV=ΔU+pΔV=ΔU (ΔV=0) – изменение внутренней энергииДля идеальных газовQp= Qv+ ΔnRTΔH=ΔU+Δn(RT), где Δn – изменение числа молей газообразных веществ,Δn=2-3-1=-2 моль,ΔU2980= ΔH2980- Δn(RT),ΔU2980=1410,9-(-2)*8,31*298=1410,9+4952,76=6363,66 кДжQv=6363,66 кДж -
Естественно.
А если нужно определить теплоту сгорания этилена при V=const и T=298 К
Вроде Q=дельта U
а дельта U чему равна?
-
Начальный объем не дан?
объем не дан, плотность я определила. Я не пойму, какая концентрация имеется в виду
просто есть еще формула p=nkt, из которой можно найти n - концентрацию молекул
,скорее всего, имеется в виду молярная концентрация, в моль/литр
значит я правильно нашла?
-
Задача: определить концентрацию и плотность газа азота - N2, при температуре Т=573 К и P=40 МПа
Решение:
PV=nRT
V=nRT/P
с другой стороны
V=n/С
Приравниваем, n сокращаются, находим, что С=P/RT
я правильно определяю концентрацию газа?! или тут что-то другое...
-
 1
1
-
-
а pH соляной кислоты рассчитывается через ионную силу и коэфициент активности?
у меня получилось
мю=0,6 (корень из 0,6=0,78)
lg f = -0.5*12*0.78/(1+0,78)+0,1*12*0,6=-0,158
f=0.7
тогда а=0,7*0,6=0,42
pH= - lg0.42 = 0.38
или меня опять не туда занесло?


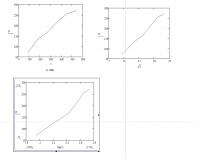
Время стадий полимеризации винилхлорида
в Решение заданий
Опубликовано
Подскажите, пожалуйста. Суспензионная полимеризация винилхлорида. Берем время всей операции - 12 часов. Из них 1 час на нагрев. Сколько можно взять на время реакции и время охлаждения?