Поиск
Показаны результаты для тегов 'графит'.
Найдено 10 результатов
-
Многие советуют делать электроды из графитовых вставок трамвайных пантографов, которые можно найти вдоль путей. Однако трамваи вымерли как рудимент, и никаких кусков графита не достать. Мне доступен лишь "карандашный графит", но он полный отстой -- быстро разрушается. Какая может быть легальная и дешевая альтернатива "трамвайному графиту"? Ехать в другой город ради того, чтобы шастать там вдоль трамвайных путей без гарантии что-то найти -- занятие такое себе. Спускать деньги на ветер, покупая платину или золото я тоже не хочу. Я планирую получить хлор и перхлорат натрия путем электролиза насыщенного раствора поваренной соли -- электроды не должны быстро разрушаться. P.S. Стоит ли пройтись вдоль обычных ж/д путей в поисках таких вставок, или там их найти маловероятно? Электрички тоже, по идее, от провода запитаны, тоже должен быть там графит
-
Нахожусь в Москве. 8 977 618 40 03 serg4003@mail.ru продам в Москве и отправлю почтой по РФ. Карбид кремния F1200 черный 54С 700 руб. кг от 200грамм (огнеупорный материал 1400-1900-2900 гр.С) (по накладной и надписи на мешке он черный а по цвету зеленоватый) из него делают шкурку нулевку. Карбид кремния F180 черный 53С 350 руб. кг Абразивный порошок крупного помола. Кварц - SiO2 30руб кг от 5кг, 50руб кг до 5кг. Графит кристаллический 150руб.кг Графит аморфный – сажа 150руб. кг
- 21 ответ
-
- кварц
- карбид кремния
-
(и ещё 1 )
C тегом:
-
Имеется микрокристаллическая смесь графита и алмаза. Разделение флотацией, тяжёлыми жидкостями, не даёт желаемого результата. Есть ли какие-то различия в реакционноспособности графита и алмаза? Окисление, или с водородом?
-
Хочется получить терморасширенный графит. "Известны способы получения вспененного графита путем его смачивания окислителями (перекисью водорода, бихроматом калия, перманганатом калия или галогенкислородными соединениями формулы МХОn) в сочетании с серной или азотной кислотой...". Но, вроде, электролизом это сделать проще и дешевле. Нашлись видеоролики только на английском. Но, не пойму подробностей процесса из-за проблемами с английским. electrochemical exfoliation H2SO4 Яндекс перевел как "электрохимическое отслаивание H2SO4" ( ) Exfoliation of Graphite by means of Plasma Electrolysis Conscious Energies (Отшелушивание графита посредством электролиза плазмы сознательная энергия) ( )
- 15 ответов
-
- интеркаляция
- графит
- (и ещё 2 )
-
Мелкозернистый плотный конструкционный графит марки МПГ-7 высший сорт. Зоготовки блок размером: 220х220х110 мм, 10кг, с небольшими сколами. Видно на фото. Цена: 400 рублей/кг. Бруски размером: 198х150х100 мм, 5,4 кг Цена:500 рублей/кг Есть дополнительная возможность распилить заготовки, для изделия ваших размеров. Физ-механические свойства: Плотность, не менее 1,8 г/cм3 Предел прочности при сжатии, не менее 65 МПа Предел прочности при изгибе, не менее 35 МПа Удельное Электрическое Сопротивление (УЭС), не более 12 мкОм*м Содержание золы, не более 0,25% Возможна доставка по РФ почтой: наложенным платежом. Или транспортными компаниями. Посмотреть графит МПГ можно в Екатеринбурге, район Упи Урфу Втузгородок. Подробности здесь в личке, или комментариях. А лучше по телефону. 8-922-027-89-85
- 8 ответов
-
- графит
- электролиз
- (и ещё 6 )
-
Чем приклеить стеклоуглкрод к серебряной пластинке, чтобы обезпечить минимальное сопротивление + чтоб оно не менялось. Пайка, я так понимаю, невозможна принципиально? Что посоветуете кроме токопроводящего клея Контактол?
- 59 ответов
-
- контакт
- стеклоуглерод
-
(и ещё 6 )
C тегом:
-
Поискал в интернете, не нашел. Для особой методики электрофореза нужны электроды из чистого графита. Как можно сделать?
-
Материалы: Шлак от плавки БрО5Ц5С5 (3.5 кг) Графитосодержащий тигель Лужcкого образивного 20 ой марки серии AX Графит измельченный (фракции по 50мм) (200 г ) Каолиновая вата Доброго времени суток форумчане! Завалялось в гараже, у моего соседа Иваныча ,пару десятков кг шлака ,от плавки БрО5Ц5С5. Шлак состоит из неметаллической составляющей (оксиды металлов) и металлической составляющей -это корольки металла запутавшиеся в шлаке. Рентгенофлуоресцентный анализ шлака показал вот такой результат: Сu - 1,38% Pb - 17,92% Zn - 15,78% Sn - 5,67% P - 5,47% Fe - 2,38% Al - 1,51% Восстановление Иваныч проводит двухэтапно, сначало проводит разделительную плавку (Отделяет металлическую составляющую от неметаллической). А затем восстанавливает оксиды металлов. Загрузил шлак в тигель, тигель поставил в печь (индукционная тигельная средней частоты), а печь поставил на разогрев до 1250-1300 C. Расплавился шлак через 20 мин. Общее время плавки составило 60мин, 20 на расплавление , а 40 минут Иваныч заложил на отделение металлической от неметаллической составляющей. Хочу заметить что обильно выделялся белый дым (Иванч думает что это Zn летит) Вы как считаете? Ровно час после закладки , решили мы сливаться... Как и предполагали времени на разделение хватило, на дне изложницы лежал кусок металла бело-желтоватого цвета весом 1800 г . 40 минут на разделение?? много это или нужно еще?, не знаю как проверить. Ведь если довести неметаллическую сотавляющую и металлическую до температуры плавления, металлическая должна сразу упасть на дно тигля ввиду своей плотности. Наверное слово сразу здесь неуместно, в течении какого времени должно произойти разделение но а как это время рассчитать?? Чтобы не сжечь лишние кВт энергии... Восстанавливать оксиды Иваныч решил графитом, благо когда-то "взял" его на работе. Загрузил шихту в тигель, печь поставил на разогрев и накрыл все это дело каолиновой ватой, а сам пошел курить. Печь (индукционная тигельная средней частоты) разогрелась до 1250-1300 С, ну и через 20 мин в тигле всё кипело и обильно выделялся белый дым в очень больших количествах. На восстановление заложили 90 минут. Восстанавливались оксиды при температуре 1250-1300 С. Выход составил : 200 г. Опять же вопрос , как рассчитать время нужно для полного восстановления?? Проводить десятки плавок на разное время и проверять хим состав??
-
- восстановление меди
- графит
-
(и ещё 1 )
C тегом:
-
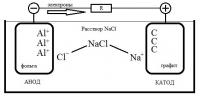
Заранее извиняюсь, я не химик по профессии, так что не будьте строги. Я тут заинтересовался самодельными батарейками. И занялся конструированием самой простой с солевым раствором в качестве электролита. Меня интересует какие химические продукты выделяющиеся в гальваническом элементе состоящим из соляного раствора NaCl•H2O и электродов из алюминия (фольга) и графита. Могу предположить следующее: 1.Натрий оседает на катоде (углероде, точнее графите) и не вступает с ним в реакцию. Хлор также оседает, но на аноде (алюминий, в моем случае фольга) и не вступает с ним в реакцию. 2. Либо... Далее натрий осевший на катоде реагирует с водой: 4Na + O2 +2H2O = 4NaOH И щелочь NaOH реагирует с алюминием (что мне кажется маловероятно): 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2↑ Или хлором, который осел на катод (что мне кажется более вероятным): 2NaOH + Cl2 = NaClO + NaCl + H2O А хлор, частично, вступает в реакцию с алюминием и в результате AlCl3 выпадает в осадок. И далее, AlCl3 реагирует со щелочью: AlCl3 + 3NaOH = Al(OH)3↓ + 3NaCl Мой элемент длительное время способен выдавать напряжение в 0.3 вольта, но если периодически протирать графит, то напряжение возрастает примерно в двое, до 0.6 вольт, но очень скоро падает до 0.5. А через час, после протирания, падает до 0.3 вольт. Правда это все без нагрузки (если не считать сопротивление старенького вольтметра). При том, что если протирать фольгу, то особого подъема напряжения я не заметил. Далее, я заметил, что можно и не протирать катод, а сделать два катода соединенного одним проводом.При этом в то время как первый катод находится в растворе, второй сушится на воздухе. Когда напряжение падает до 0.3 то, если их поменять местами, вижу, что напряжение возрастает до 0.5, но в течении пары минут падает до 0.4. И если каждый раз так менять катоды с периодом в семь минут, то напряжение меньше 0.35 вольт не упадет. Я так подумал, а что если катодов будет не два а пять, к примеру, то время смены можно уменьшить, а среднее напряжение возрастет. Про это я сумел найти только то, что при прерывистом разряде большими и средними токами работоспособность батареек заметно увеличивается по сравнению с непрерывным режимом работы. С тем же эффектом можно второй катод и не вынимать из раствора, а лишь провод коннектить то с одним, то с другим катодом... То есть если сделать некий электронный прерыватель работающий на той же батарейке которую он и регулирует, который переключатся между катодами, то напряжение можно усреднить и до 0.5 вольт. Я не физик, и не так хорошо знаком с электроникой, но мне кажется это очень интересным Итак, мои вопросы: 1. Почему так происходит с двумя катодами? 2. Какие все же реакции протекают в таком элементе?