
sergium
-
Постов
229 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные sergium
-
-
1) Получить можно по схеме R-MgBr + СО2 → R-COO-MgBr → R-COOH + Mg(OH)Br
Это получение с помощью реактива Гриньяра
2) Наберите в гугле сульфохлорирование карбоновых кислот, получение амидов карбоновых кислот
3) Формулы можно найти опять же. Например тут http://www.chemistry.ssu.samara.ru/chem4/pic/o4602.gif
Писать довольно много. Просто поищите по этим рекомендациям в инете, тут стандартные реакции и вопросы. А потом покажите проделанную работу
-
Это ОВР. Обычно в программах школ не составляют правую часть в данном типе реакций, а только делают баланс. По-крайней мере в украинских. Это детальнее проходят в институтах на первых курсах.
Тут свойства перманганата калия. В зависимости от среды, он восстанавливается в разные продукты. Почитайте тут
-
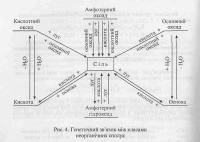
Вот генетическая схема в общем виде, правда на украинском, т.к. понятнее не нашел.
В правой части хим. реакции должно обязательно образовываться либо соль, либо кислота, либо основание, иногда и оксид (при реакции разложения)
Т.о. даже если вы не знаете, что в правой части, то можно составить её как пазл по имеющимся частям в левой части.
В общем-то этих знаний вполне достаточно для школы.
-
Как объянить, почему ртуть реагирует с серой легче, чем цинк, хотя активность первой меньше?
-
думаю, там реакция другая, просто N2O5 связвает азотную кислоту, воды там нет.
Т.е. типа такого
H[Au(NO3)4] + N2O5 --> Au(NO3)3 + HNO3*N2O5
Как понять связывает азотную кислоту? В виде чего?
Что-то первый раз слышу. Обычно N2O5 связывает воду
-
В последней реакции опять получится комплекс, только безводный.
Я делал по книге Третьякова, как предложил aversun.
Просто с N2O4 надо выделить сначала чистое золото из комплекса
"при взаимодействии соединения (H3O)[Au(NO3)4] с азотным ангидридом и последующем нагревании в вакууме при 80 °С возгоняются золотисто-желтые кристаллы нитрата Au(NO3)3."
Вот я эту реакцию и написал
-
"Получены также комплексные нитраты, например K|Au(NO3)4]. Имеются сведения о том, что при взаимодействии соединения (H3O)[Au(NO3)4] с азотным ангидридом и последующем нагревании в вакууме при 80 °С возгоняются золотисто-желтые кристаллы нитрата Au(NO3)3.
Таким образом, соли кислородсодержащих кислот золота в водных растворах не могут быть получены. Золото(III) не образует устойчивых аквакомплексов".
Неорганическая химия. Т. 3, кн. 2. Под ред. Ю.Д. Третьякова. стр. 222
Думаю, как вариант тогда может так сойти
Na[Au(OH)4] + HNO3 (t)--> NaNO3 + (H[Au(NO3)4] + H2O)
H[Au(NO3)4] + H2O + N2O5 --> Au(NO3)3 + 3HNO3
-
Паддефет в своей монографии по химии золота пишет, что ионы золота Au(3+) в свободном виде в водных растворах не образуются, в азотной кислоте образуется H[Au(NO3)4] (http://chemister.ru/Database/properties.php?dbid=1&id=8833)
тогда собственно в этом и вопрос. Как осуществить такое превращение Na[Au(OH)4] --> Au(NO3)3
может взять другой растворитель...
-
Mo+NaNO3+NaOH
Делаете слои сендвичем и прокаливаете
-
Стоит ли упоминать про сулему
-
Почему возник такой вопрос? По какой причине надо получить именно Au3+ в растворе? С другой стороны, ну, получили вы Au(NO3)3, а что вы можете сказать о константе его диссоциации, может она близка к нулю, тогда все равно вы не получите желаемого иона.
Просто я подумал, что соль Au(NO3)3 не может существовать в водном растворе. Честно говоря, не видел нигде про неё упоминания. Только в википедии
-
Встретилось задание: надо получить нитрат золота из комплекса.
Реакция впрочем-то стандартная
Na[Au(OH)4] + HNO3 --> NaNO3 + Au(NO3)3 + H2O
Но известно, что
Au(OH)3 + 4HNO3 = H[Au(NO3)4] + 3H2O
т.е. в водном растворе в одной книге говорится, что не существует гидратированных ионов Au3+.
Собственно в этом и вопрос. Может ли протекать реакция выше по такой схеме? -
-
набухать-набухает, как и все полимеры в растворителях.Но мне кажется, что второй раз его нельзя использовать
-
Уважаемые форумчане,
Кто знает, можно ли восстановить силиконовый герметик засохший, залив его растворителем или ещё как-то?
-
Формула гидроксида бария Ba(OH)2
Эта химическая формула отображает структуру молекулы. Видно, что она состоит из 1 атома бария, 2 атомов кислорода и 2 атомов водорода. Если атом обозначить кружочком, то можете нарисовать молекулу эту.
Количество молекул Ba(OH)2 вычисляете по формуле
N = m*6.02*1023/ M
M - молярная (молекулярная) масса Ba(OH)2 . Найдите её сами
-
Преогромнейшее спасибо
Только кажется ошибочка. Или я туплю
K1 = [H+]1*[H2PO4-]/ [H3PO4]
[H+]1 = (K1C)0,5
K2 = [H+]2*[HPO42-]/ [H2PO4-]
Но, учитывая, что [H2PO4-] = [H+]1
K2 = [H+]22/ (K1C)0,5
[H+]2= (K2*(K1C)0,5)0,5
Просто [H+]2 = [H2PO4-] такого не может быть, ведь H2PO4- диссоциирует не полностью
-
в общем такой вопрос
-
Вычислил, получилось
K1 = [H+]*[PO43-]^4 / [H3PO4]*K3^2*K2
[PO43-] как можно выразить?
-
Помогите плиз,
H3PO4 надо вычислить рН, учитывая вторую и третью степени диссоциации.
Перечитал литературу, но везде учитывают только первую степень. Как рассчитывается рН многоосновных кислоты, если учитывать 2-ю и даже 3-ю степени -
-
Да и обычно их перемешивают экструдером с добавлением стабилизаторов. Так есть риск, что они окислятся воздухом
-
нет, не получится. Если у вас пластики близкие по составу, то их можно совместить: например, каучук и полиэтилен. Полиэтилен и полипропилен.
Но если полистирол с ПВХ или с полиэтиленом, то ерунда будет.
Важно подобрать температурный режим -
Супер, спасибо. Все сошлось.
Хотя теоретически там могут любые реакции идти. Например:
Na3PO4 + H2SO4 --> NaH2PO4 + Na2SO4
Na2SO4 + H3PO4
Да и Cu3(PO4)2 может реагировать с фосфорной кислотой
Реакция с Pb(NO3)2
в Решение заданий
Опубликовано · Изменено пользователем sergium
Марганец от 2+ до +7 азотная кислота вряд ли окислит. Нужны более сильные окислители.
Если нетрудно, скиньте источник
Так правдоподобнее
MnSO4 + PbO2 + HNO3 → HMnO4 + Pb(NO3)2 + PbSO4 + H2O