mrDIMAS
Пользователи-
Постов
30 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент mrDIMAS
-
Я не смог найти информации по 2-хлорэтилнитрату. Какие у него свойства (плотность, запах и т.д.), кроме взрывчатых и отравляющих?
-
Ну да, маслянистая жидкость, легче воды с запахом морковки и, естественно, с запахом азотки. Сложный такой запах, но 100% пахнет морковкой.
-
Трубка осталась прежней толщины, затвердела и покрылась пузырьками. А вот резиновая пробка вся в рытвинах и похудела с торца на 2-3 мм
-
Нужна была азотная кислота, соорудил простой перегонный аппарат, но вместо нормального холодильника взял ПВХ трубку, вставил ее в резиновую пробку, а пробкой заткнул коническую колбу со смесью конц H2SO4 и KNO3. Другой конец трубки опустил в колбу с ледяной водой, охлаждаемой водой со льдом. Через 15 минут перегонки в приемнике образовалась неизвестная жидкость не смешивающаяся с водой с четким запахом моркови. Что это может быть?
-
Не пробовал, пропитал парафином. Проведу электролиз и отпишусь о результатах. А вообще растительные масла устойчивы к действию хлора? А то не хочется дышать лакриматорами прочими непотребствами. Также есть паста КПД (кремнийорганическая), буду использовать ее для изоляции винтов и гаек, и оголенной части медного провода.
-
Есть вопрос по пропитке графитовых анодов. У меня очень быстро разрушается медь в месте контакта графита с медным проводом, который прижат нержавеющим винтом с гайкой. Происходит это из-за пористости графита и, конечно, из-за образования газообразного хлора. Чем можно пропитать графит в том месте, где он контачит с медью? В литературе ( Якименко. Электродные материалы в прикладной электрохимии) рекомендуют использовать льняное масло, однако достать его проблематично сейчас. Может парафин подойдет?
-
В реальности ток плавает в очень небольшом промежутке - около 0,5 А. Я специально интегрировал формулу Фарадея по току и считал выход при нарастающем токе - на первом часе электролиза (нарастает от 10 А до 15 А ). В итоге разница оказалась очень маленькой - порядка 10 г. Для большей стабильности параметров электролиза планирую сделать стабилизатор тока до 50 А. Как его соберу, сразу проведу два сравнительных электролиза - с добавками и без.
-
Ток по амперметру. В начале электролиза ток около 10 А, постепенно электролит нагревается (за 1 час) и ток вырастает до 15 А и более не увеличивается. Странный вопрос. Блок питания для электролиза это в самом простом случае трансформатор с выпрямителем, в более продвинутом случае добавляется еще и стабилизатор тока. Мой же блок питания самодельный: 800 Вт, 5 В - 30 А, 12 В - 30 А, 24 В - 15 А, а также выход со стабилизацией напряжения от 0 до 24 В при токе до 15 А. БП универсальный, для запитки самодельной электроники и сильноточного электролиза.
-
Наконец-то дошли руки сделать сравнительный анализ электролиза с добавками и без. В первом случае электролиз проводился без добавок. 475 г NaCl в 1,5 л воды (насыщенный раствор) подвергался электролизу в течении 8 часов при токе 15 А в 3-х ячейках включенных последовательно. Выход составил 54 г (23% от теоретических 241 г). Во втором случае добавкой был вольфрамат натрия. Электролиз проводился в тех же условиях что и в первом случае. Выход составил 120 г (51% от 241 г). В обоих случаях контроль и корректировка pH электролита не проводились. Вывод. Добавка вольфрамата натрия увеличивает выход хлората натрия по току в 2,2 раза. Следующий электролиз проведу с контролем pH электролита.
-
Немного покопавшись в литературе, узнал что вольфрам прекрасно растворяется в перекиси водорода. Взял 246 г пластин, залил их 35% перекисью водорода и оставил их на 2 дня в темном прохладном месте, затем слил раствор, промыл пластины, взвесил и оказалось 213 г - то есть 33 г вольфрама растворилось с образованием слегка зеленоватого вязкого тяжелого раствора, при этом объем раствора уменьшился вдвое. Что за соединение вольфрама образовалось?
-
Добрался я до осадка, выпарил и получил всего 10 г вольфрамовой кислоты - и это из 30 г пластины (после нового растворения остался огарок 10 г). Даже если принять % содержания вольфрама в 60%, то выход все равно маленький. Странный вольфрам в общем, очень странный.
-
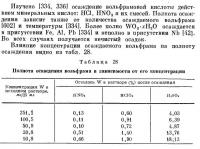
В общем я нашел инфу, почему вольфрамовая кислота не осадилась - я осаждал серной кислотой при большом разведении (60 г вольфрамата в 1000 мл воды), а в "Аналитической химии вольфрама", в разделе Гравиметрические методы есть такая табличка. Буду осаждать азотной кислотой. Update. И действительно, вольфрамовая кислота отлично осаждается азотной кислотой.
-
Вылил я этот раствор. Сегодня\завтра сделаю новый расплав. Как убрать нитрит из раствора\расплава?
-
Пластина это цилиндр, с размерами 2.3 мм толщиной и 40 мм диаметром, вес 40 г. По расчетам получается (в см) 0.23 * 22 * 3.14159 = 2.89 см3 при плотности вольфрама 19.25 г/см3 получается 57 г. Что не совпадает с известной массой, но довольно близко. Если бы был из никеля, то вес был бы 2.89 * 8.9 = 25.7 г. Из сплавов никеля тоже вес был бы в районе 25 г. Раствор бесцветный кстати. Update. Плотность материала пластины получается 13.84 г/см3. Но нужно учитывать, что эта пластина - диод, причем рабочий.
-
Растворил пластину из вольфрама (40 граммов) в расплаве NaOH (17 г.) + NaNO3 (55.7 г), растворилась полностью. Расплав имел изумрудно зеленый цвет - видимо примеси какие-то. Плав растворил в воде (500 мл), отфильтровал. Добавил 51 мл 35% H2SO4 и... ничего. Вольфрамовая кислота не вываливается в осадок. pH раствора около 2 по универсальному индикатору. В чем дело-то, может это что-то другое, а не вольфрам? Или для осаждения требуется сильно кислая среда - хотя вольфрамовая кислота не растворима в воде?
-
С осаждением вольфрамовой кислоты будет чище конечный продукт, а с плавиковой кислотой я стараюсь избегать контактов - не полюбили мы друг друга .
-
Как тогда убрать нитрит из получившейся смеси? Единственная мысль - выпарить, и растворить нитрит в этаноле, а вольфрамат останется в осадке.
-
Эх, реально оказался вольфрам. И он отлично горит в расплаве NaNO3+ NaOH . Так хорошо, что раскаляется до бела и начинает брызгаться расплавом - по дурости не надел перчатки и щелочь попала на запястье - результат мелкие белые точки ожогов. Однако вольфраматы тоже подойдут для моих целей. Как сделать вольфрамат тогда?
-
Имеются пластины из молибдена (подложки мощных диодов\тиристоров). С химией молибдена совсем не знаком. Как из него получить молибдат натрия? Мои действия такие. Кинуть пластину молибдена в смесь серной и азотной кислоты, осадить гидроксид молибдена, прокалить до MoO3, а затем его растворить в гидроксиде натрия. С чем могут быть проблемы?
-
Одно дело общетоксическое действие, другое канцерогенное. На неделе проведу сравнение между молибдатом и дихроматом в качестве добавок при контроле pH. Отпишусь о выходе.
-
В случае применения дихромата какие нужно соблюдать предосторожности? Электролизер у меня закрытого типа, с отведением газов в раствор соды.
-
Ищу замену дихромату, ибо меня печалит маленький выход (<50%) за вторую попытку электролиза. Поискав в интернете на эту тему (http://www.exploders.info/forum/3/28156.html автор ссылается на годную статью), нашел что дихромат можно заменить на молибдат натрия\калия. С контролем pH выход такой же как при использовании дихромата. Есть у кого-нибудь опыт его использования?
-
Восстановление хлората до хлорида? В некоторых источниках рекомендуют заменять дихромат на фториды калия\натрия, кто нибудь пробовал? Фториды всяко менее вредны чем, канцерогенный дихромат.
-
Хм. Вряд ли, ибо написано "выход 90 г". Что-то напутано в общем. Вчера сделал пробный электролиз 440 г NaCl (насыщенный раствор): 3 ячейки последовательно - аноды из графита, катоды из нержавейки, ток 15 А, время 11 часов. После электролиза раствор отфильтровал, упарил до появления кристаллизационной пленки, охладил - выпал лишний NaCl. По расчетам за это время должно было образоваться 244 г NaClO3 с учетом потерь тока на нагрев (кпд 86%), исходя из этой массы прилил раствор 132 г KOH, сразу же начал выпадать KClO3 . Далее раствор охладил до +4, и собрал весь осадок. Затем осадок растворил в минимально возможном количестве кипятка и поставил опять охлаждаться до +4. Собрал кристаллы, высушил, взвесил и получил всего лишь 127 г KClO3 из теоретических 275 г. Получается что эффективность ниже 50%. Какие у кого будут соображения? Где я мог потерять столько продукта (исключая стадию перекристаллизации - воды было около 140 мл, при +4 потери KClO3 в растворе всего 5 г)? Update. Просмотрел свои записи, и выяснилось, что в начале электролиза (вечер 23,00) ток был 8 А и под утро стал 15 А. В сети напряжение гуляет от 180 В вечером, до 225 утром. БП для электролиза простой трансформаторный с выпрямителем, поэтому ток скачет в такт изменениям напряжения в сети. Пересчитал со средним током 10 А и теоретически выход хлората калия должен быть 185 г, в таком случае выход тоже не соответствует ожиданиям. В следующий раз буду точнее следить за током.
-
Нет, дихромат не учитывал. Неужели 1 г дихромата так сильно повышает выход? Я не особо хочу связываться с канцерогенами. Графита у меня много, где-то 5-6 кг листов 5мм х 70мм х 50мм. Надоело отстаивать\фильтровать графитовую пыль. К тому же я ставлю 3 ячейки последовательно при напряжении 14 В в сумме.