
Eyems
-
Постов
23 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Eyems
-
-
Решаю задачу, а ответ мм... бредовый). Помогите пожалуйста! Мое решение прикрепляю фоткой
1. По известным значениям стандартных электродных потенциалов полуреакций
NO3– + H2O + 2e– = NO2– + 2OH– +0,01В
NO3– + 3H+ + 2e– = HNO2 + H2O +0,934 В
вычислите константу диссоциации азотистой кислоты HNO2.
Почему то не прикрепляется фотография. Ну суть решения - составить уранение диссоциации через два данных, найти Gдис-ии как разность G1 - G2, которые считаем по потенциалам (G = -nFE), через Gдис-ии вычисляем Kдис-ии. Я правильно понимаю?
-
В константу диссоциации подставляете новую концентрацию OH и находите концентрацию иона аммония
Там правда будет нужна концентрация аммиака. ее находите из рН для первого раствора, учтя, что [OH] = (KC)0,5
Спасибо вам еще раз. Второй раз за сегодня помогли! Я как-то все время сомневаюсь, где можно "пренебрегать". Ведь получается мы здесь оставили концентрацию аммиака из первого раствора неизменной и для второго?
-
Подскажите пожалуйста насчет задачи. Кажется, жестко туплю, но тем не менее.
К 1л р-ра аммиака (рН = 11.5) добавили 0.025 моль NaOH. Как изменилась степень диссоциации аммиака после добавления NaOH?
Понятно, что получить ответ можно, если отнести альфа1 к альфа2. Из pH можно найти равновесн. конц. OH- = NH4+ до добавления щелочи. Вроде можно концентрацию OH- после добавления принять равной конц. этой щелочи. Но откуда взять равновесн. конц. NH4+ после добавления NaOH? Как оценить смещение равновесия? Или надо вообще по другому решать?
-
Для начала определите концентрацию аммиака в полученных 1,2 л раствора. Исходные данные для этого расчета приведены в первой части задачи.Да
Да, спасибо. Это сообщение вообще случайно в эту тему отправилось. Про ур-е pV=nRT мне в Помощи уже напомнили. Но все равно спасибо!
-
1. pV=nRT - считаете число моль аммиака и С = n/V(раствора) - находите его молярную концентрацию
Ежкин кот... Как можно забыть о существовании этого ур-я?! Спасибо большое
 )
) -
Помогите пожалуйста решить! Не получается...
Через воду при t=18C и давлении 90.2кПа пропустили 5л гаозообразного аммиака и получили 1.2л раствора. Определите степень диссоциации аммиака в этом растворе и рН раствора? Кд nh3 = 1.8*10^(-5)
-
Помогите пожалуйста решить! Не получается...
Через воду при t=18C и давлении 90.2кПа пропустили 5л гаозообразного аммиака и получили 1.2л раствора. Определите степень диссоциации аммиака в этом растворе и рН раствора? Кд nh3 = 1.8*10^(-5)
-
Да
Спасибо за ответ!
-
-
Если очень условно записать реакцию гидролиза декстрина, то получится так:
Gx + (x-1)H2O = xG
где
G - обобщённый глюкозный остаток
х - количество глюкозных остатков (в среднем) в молекуле декстрина
Тогда соотношение количества глюкозы и воды, пошедшей на ея получение равно х/(х-1)
В растворе после реакции имеем 10 г серняги, 135 г глюкозы, остальное - вода, коей имеем 16.76%. Остюда масса воды после реакции составляет (10+135)/(1-0.1676)-(10+135) = 29.2 г
Исходно воды было 40 г. Дальше можете посчитать сами, или продолжить чтение.
Возвращаемся к нашей пропорции:
Количество глюкозы = 0.75
воды до = 40/18 = 2.22
воды после = 29.2/18 = 1.62
x/(1-x) = 0.75/(2.22-1.62) = 1.25
x = 1.25 - 1.25х
0.25х = 1.25
x = 5
Спасибо большое за помощь!
-
У меня не получается решить задачу,я посчитала все, что довольно примитивно находится из условия, а вот самое главное сделать не вышло! Помогите, пожалуйста. Номер 546.
Я прикрепляю условие и, заодно скажу, чтобы сократить ваше время, если вы решите помочь, что после р-ии масса глюкозы равна 135г, а к-во вещества 0.75,масса до реакции воды - 40г, а масса раствора серн. кты 10г. Каким то образом нужно выйти на соотношение кол. вва глюкозы и воды, прошедшей на реакцию - и все!:-))
-
Это вопрос такой, или часть задания? Напишите полностью задание.
Это вопрос лично мой, который возник при решении задачи. В задаче есть раствор сульфата железа 3 и сульфата никеля, к ним прибавляется Zn, которого на обе р-ии не достает. И так получается, что останется в растворе висеть сульфат никеля, да?
-
Подскажите пожалуйста, если у меня есть раствор 2х солей и к нему прибавляют Zn в недостатке для обеих р-й одновременно, то реакция пойдёт до конца с той солью, у которой константа диссоциации выше?
-
-
Спасибо большое,в коэффициентах то и была загвоздка, про co2 h2o - это ясно:-))
-
-
Некоторое кол-во органического в-ва, содержащего N и О, сожгли в 26,88л кислорода н.у.Образов. 9г воды и смесь газов, которую пропустили через избыток р-на Ba(OH)2, в раз-те выпало 275,8 г осадка и осталось 10,08л газовой смеси с плотностью 1,31г/л. Формула в ва - ??
В принципе все понятно, но я не могу "разделить" в расчетах непрореагировавший кислород и азот, которые с гидроксид. не взаимодействуют. Помогите пожалуйста!
-
-
Подтвердите или опровергните пожалуйста моё предположение, что в 1-фенилэтаноле-1 заместитель у бензольного ядра будет ориентантом второго рода (т.е. проявит отрицательный мезомерный эффект). Это чертовски важно уточнить!
 ))
)) -
Спасибо! Сам просматривал Википедию и самое важное место пропустил!
-
Кислотные свойства спиртов сильно слабеют, если увеличивается углеводородный радикал. Почему так происходит? У меня есть ощущение, что это весьма глупый вопрос, но всё-таки..
Ведь чем радикал длиннее, тем он, по логике, большую электронную плотность за счёт индуктивного эффекта собирает на кислороде. Т.е. связь O-H должна становиться ещё полярнее, кислотные свойства будут увеличиваться. Где ошибка в рассуждении? Помогите пожалуйста разобраться!
-
Помогите пожалуйста разобраться! При электрофильном замещении у 1,3,5-триметилбензола заместители могут отправиться только в одном направлении или может быть получается трибромпроизводное??
Для понятности сего запутанного на словах вопроса я прикрепляю картинку реакции.


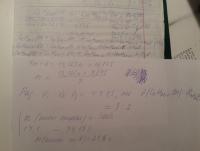
Найти концентрации ионов
в Решение заданий
Опубликовано
Не получается найти концентрации. Подскажите пожалуйста, как это сделать?
После того как в реакционном сосуде смешали 125 мл 2 М раствора HClO4, 135 мл 0,1 М раствора KMnO4и 270 мл 0,35 М раствораFeSO4 произошла реакция. Напишите уравнение этой реакции и определите концентрацию ионов Fe3+и Мn2+в полученном растворе.
Может выразить Mn2+ и Fe3+ через исх. конц. вещ-в? В общем, не получается(..