
CTAKPAT
-
Постов
18 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные CTAKPAT
-
-
Я не утверждаю, что она возможно, но весьма вероятна, т.к. NO2 сильный окислитель. NO2 растворяется в конц. азотной кислоте до 27%. Жидкого NO2 не бывает, при сжижении (охлаждении) NO2 образуется его димер N2O4. KNO2 в качестве электрода не годится, т.к. является изолятором.
Понял ошибку

Хотя интересно, ведь углерод также не поводит ток, а графит с другим строением кристаллической решетки проводит. Можно ли как-то "сплющить" KNO2 так чтобы он проводил ток?)
-
А почему не такая реакция KNO2+NO2=KNO3 + NO?
вторая реакция идет только при 400-500°С
Не думал что такая реакция возможно KNO2+NO2=KNO3 + NO.
На счет 2го спасибо - тем проще.
-
Всем доброго дня.
Допустим мы имеем смесь азотной кислоты HNO3 и жидкого оксида азота NO2 (конц) при 0oС в некоторой емкости и имеем твердый KNO2 в виде длинного стержня, а также графитовый стержень. По мере опускания стержней в емкость будет происходить ОВР реакции:(1) 2KNO2 + 2HNO3 = 2KNO3 + NO2 + NO + H2O(2) 2NO + C(графит) = N2 + CO2У меня такой вопрос. Насколько будет эффективен гальванический элемент на основе этой реакции? Где один из электродов стержень из KNO2, а другой из графита. По моим соображениям, если взять совсем немного HNO3 в растворе, то реакция будет не особо бурной, однако присутствие азотной кислоты в растворе превратит его в своего рода электролит. Ведь KNO2 не реагирует ни с чем кроме HNO3, а графит может прореагировать только с NO. А чтобы KNO2 не реагировал с кислородом емкость можно заполнить чистым азотом или тем же CO2. Теоретически это же возможно?
Мне интересна подобная схема тем что продукты реакции могут быть возвращены в исходное состояние только под воздействием температуры:
(1) 2KNO3 = 2KNO2 + O2(2) 2HNO2 + O2 = 2HNO3Разве что графит не так-то просто восстановить из CO2.
Если я где-то не прав буду рад если меня поправят.
-
Ну, можно попробовать из ДМСО. Есть ещё где-то про электрохимическое осаждение его из ЛАГа, но надо поискать, какой тут нужен растворитель.
Если можно, расшифруйте ДМСО и ЛАГ, я человек не сведущий в этих делах.
-
-
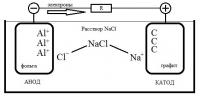
Здравствуйте, это моя вторая тема, которая на первый взгляд имеет мало общего с моей предыдущей темой "соленая батарейка". Дело вот в чем, в предыдущей теме я хотел разобраться, что происходит в гальваническом элементе, в котором электроды - алюминий (Al) и графит ©, а электролит - соленой раствор (NaCl). Выяснил, что в таком элементе расходным материалом является алюминий и вода. А продуктами ОВР являются Al(OH)3 и H2. Также понял, что для увеличения продолжительности работы "батарейки" можно воспользоваться перекисью водорода (H2O2), который устраняет водород осевший на катоде (С), который снижает напряжение.Итак, в этой теме меня интересует, как использовать отход Al(OH)3, который образуется в ходе работы моей "батарейки" для новой "батарейки"? То есть, как выделить чистый алюминий (Al) из Al(OH)3, чтобы снова использовать его в моем элементе. Просмотрев достаточно много интересных сайтов я остановился на довольно перспективном и не ординарном (для меня) методе - выращивании кристаллов металла. Почему на нем? Во первых, обычно, чтобы получить чистый алюминий нужно затратить большое количество энергии, и тут появляется вопрос - зачем мне использовать энергию для получения чистого алюминия, если он мне нужен для того же, с помощьью чего он был получен. =) А во вторых, меня это заинтересовало.Перейду непосредственно к теме. Вот мой вопрос: Как вырастить кристалл алюминия?Вот сайт на котором достаточно подробно рассказывается о выращивании металлов:
Там доходчиво рассказано, что и как делать, чтобы вырастить кристалл меди. Из примечаний, я понял, что подобным образом можно вырастить кристаллы серебра, висмута, сурьмы (то есть металлы с положительным потенциалом). А вот для выращивания кристаллов свинца и олова (металлы с отрицательным потенциалом) нужно взять подкисленный раствор соли одного из этих металлов малой концентрации.То есть: Pb(HSO4)2 и Sn(HSO4)2.Но сработает ли это для алюминия? Ведь он, кроме того, что расположен значительно левее в электрохимическом ряде активности металлов, но и имеет другую валентность.Если я не прав, то поправьте. Чтобы сделать подкисленный раствор соли алюминия, нужно:Al(OH)3 + 3H2SO4 = Al(HSO4)3 + 3H2OКислая соль - гидросульфат алюминия - получается при соотношении основания и кислоты 1:3.При условии, что я сумел очистить осадок Al(OH)3 от NaCl ( мне совсем не нужна такая реакция: NaCl + H2SO4 = NaHSO4 + HCl↑ ).Ожидаю критических отзывов и хоть каких нибудь ответов на вопрос.
-
Н2О2 не распадается на два иона ОН-.
В пластмассовой таре ведет себя нормально, у меня стоит в полиэтиленовой канистре.
Вот не знаю как она себя ведет, но на практике, даже несколько капель 3% H2O2 в соляной раствор значительно повышают продолжительность работы моей "батарейки". Вот уже два часа напряжение держит выше 0.55 вольт, хотя без перекиси за это время напряжение падает до 0.3 вольт.
Думаю это связано с тем, что перекись нейтрализует водород который образуется на графите с образованием воды. Хотя я наблюдаю небольшое количество пузырьков на аноде и катоде...
Самое интересное, что со временем, напряжение даже повышается, сейчас уже больше 0.6 вольт. Кстати, а кроме самой перекиси во флаконе который продается в аптеках есть что-то еще?
-
На счёт электролита - не важно, какие там соли. Лишь бы электричество нормально проводил, и способствовал растворению алюминия (не быстрому, но и не так, что алюминий месяц пролежит, а едва что-то сделается).
Я раньше экспериментировал - электролит КОН, электроды - алюминиевая проволока и медная фольга. Отдача по току была приличная. Но хватало "батарейки" всего на пару часов. А если брать фольгу алюминия, то дело уже стоит о минут
У меня появилась идея, а что если использовать вместо воды раствор перекиси водорода H2O2, хотя бы 30%. Водорода, тогда по идее, должно меньше выделиться? Ведь H2O2 в присутствии алюминия распадается на два иона OH- которые тут же крепятся к Al. Если это так, тогда у меня вопрос, насколько опасно будет использовать перекись с солью NaCl в качестве электролита? H2O2 и NaCl не вступают в реакцию, но меня волнует как себя поведет перекись большой концентрации скажем в пластмассовой таре.
-
У меня есть еще один вопрос на перспективу. Что если Соль NaCl заменить на хлорид алюминия AlCl3? В этом случае напряжение будет выше? Мне по уравнению Нернста не совсем понятно как учитывать катод (графит):
E = E0Me + (R • T / z • F) • ln [Mez+] = E0Me + (0,059 / z) • lg [Mez+],где E0Me – стандартный потенциал металла, ВR – универсальная газовая постоянная, Дж/моль•КT – температура, Кz – число электронов, принимающих участие в электродной реакцииF – число Фарадея, Кл/мольMez+ – концентрация катионов металла, моль/лЭДС = Екатода – Еанода. -
Электрон бежит по проводу. NaCl распадается и движется к электродам, тем самым создавая поле и все условия для движения электрона. Прочитайте про
потусторонние силы.Топливо, да, алюминий и вода, расходуются только они. Только ЭДС маловато, сделайте гальванический элемент Zn/Zn2+//Cu2+/Cu . Его ЭДС больше. Возьмите 2 стакана и налейте в один сульфат цинка, в другой - сульфат меди. В сульфат меди опустите медь, в сульфат цинка - цинк. Соедините стаканы солевым мостиком, тряпочкой, пропитанной NaCl например. Посчитайте потенциал электродов E = E0 + (0,059/n)lgСм и ЭДС ΔE = Екатод - Еанод и сравните с практическим результатом.
Не совсем понятно с NaCl, почему же тогда, если Na отделяется от молекулы он не вступает в реакцию с водой? Ну да ладно.
А что касается Zn/Zn2+//Cu2+/Cu, я видел много подобных элементов, но по мне лучше иметь один расходный метал, чем два

А алюминий использовал в силу его доступности...
-
На графите вода принимает электроны и образует OH(-) и H2. Алюминь отдает электроны и образует Al(3+), который встречается с OH(-) и выпадает в осадок. Что такое ток? Ток - это упорядоченное движение свободных заряженных частиц. Во внешней цепи это электрон по проводам бежит из алюминьки в графит, а в растворе - Na(+) и Cl(-). Они не отдают ничего и не принимают, они движутся и все, создавая ток в растворе, замыкая цепь. Если бы был дистиллят - тока бы не было, цепь не была бы замкнута. Может чего не понимаю, но Na[Al(OH)4] тут не при чем и хлору со щелочью там неоткуда взяться. Все связывается и среда остается как была. Если бы были электроды разделены по разным стаканам и между ними солевой мостик - тогда бы щелочь может и накапливалась в одном из них. Поправьте.
Нет, у меня оба электрода в одном стакане и ни чем не разделены.
То есть грубо говоря, молекула NaCl не распадается, а играет роль мостика по которому бежит электрон от катода (графит) к аноду (алюминька)? Тогда получается, что в этом элементе топливом играет роль вода и алюминий?

-
То есть я бы прав, что натрий реагирует с водой с образованием щелочи? Но ведь и она продолжает реагировать с анодом:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2↑
и с тем, что на аноде выделилось:
Al(OH)3 + NaOH = Na[Al(OH)4]
То есть в итоге, на аноде мы получаем Na[Al(OH)4] в осадке и водород, а на катоде, если обойтись без MnO2, только водород. Значит в ходе работы эта батарейка образует H2 и в осадке Na[Al(OH)4]?
Только вот похоже, что Na[Al(OH)4] не оседает а лежит на стенках анода...
А что же с хлором происходит? он так же как и водород "улетает"?
-
-
Я хочу понять физику процесса. Я правильно понял, что в результате реакции:
Al + 3H2O = Al(OH)3 + 3/2H2
на аноде возникает положительный заряд.
И соль NaCl разделяется на два иона Na+ и Cl-. Хлор отдает электрон аноду, то есть становиться электронейтральным... А ион натрия, в свою очередь, "бежит к катоду", чтобы забрать у него электрон.
Возможно ли что именно натрий и осаждается на катоде (графите)? -
Э нет! Дистиллированной водой не обойтись! NaCl в вашей системе - это фоновый электролит, обеспечивающий перенос электронов. А дистиллировка тока практически не проводит.
Электроны перемещаются по внешней цепи от анода к катоду. Но для постоянного тока их нужно по электролиту обратно доставить - тут ионы, на которые в растворе распадается NaCl, и выполняют эту работу.
Кроме того, хлорид-ион выполняет ещё одну важную миссию - он активирует поверхность алюминия. Если заменить на сульфат натрия, например, то батарейка станет хуже работать.
Ну это я знал, но не знал, что вода играет какую-то роль в этом процессе... Спасибо.
Но все равно, получается, что на графите что-то оседает, а потом если разорвать цепь и подождать, то напряжение повыситься, так же как если бы протереть графит...
-
Нет там ни натрия, ни хлора. Всё сводится к растворению алюминия в воде:
Al + 3H2O = Al(OH)3 + 3/2H2
На аноде (алюминий):
Al - 3e- = Al3+
На катоде:
3H2O + 3e- = 3OH- + 3/2H2
На аноде идёт мгновенный гидролиз по катиону, и осаждается гидроксид алюминия, поэтому напряжение падает. А что касается остальных эффектов - то это уже какая-то механика, очистка анода.
То есть получается можно обойтись просто дистиллированной водой? Не думал что вода способна так просто растворить алюминий)
-
Заранее извиняюсь, я не химик по профессии, так что не будьте строги.Я тут заинтересовался самодельными батарейками. И занялся конструированием самой простой с солевым раствором в качестве электролита.Меня интересует какие химические продукты выделяющиеся в гальваническом элементе состоящим из соляного раствора NaCl•H2O и электродов из алюминия (фольга) и графита.Могу предположить следующее:
2. Либо...Далее натрий осевший на катоде реагирует с водой:4Na + O2 +2H2O = 4NaOHИ щелочь NaOH реагирует с алюминием (что мне кажется маловероятно):2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2↑Или хлором, который осел на катод (что мне кажется более вероятным):2NaOH + Cl2 = NaClO + NaCl + H2OА хлор, частично, вступает в реакцию с алюминием и в результате AlCl3 выпадает в осадок.И далее, AlCl3 реагирует со щелочью:AlCl3 + 3NaOH = Al(OH)3↓ + 3NaClМой элемент длительное время способен выдавать напряжение в 0.3 вольта,но если периодически протирать графит, то напряжение возрастает примерно в двое, до 0.6 вольт, но очень скоро падает до 0.5. А через час, после протирания, падает до 0.3 вольт. Правда это все без нагрузки (если не считать сопротивление старенького вольтметра). При том, что если протирать фольгу, то особого подъема напряжения я не заметил.Далее, я заметил, что можно и не протирать катод, а сделать два катода соединенного одним проводом.При этом в то время как первый катод находится в растворе, второй сушится на воздухе. Когда напряжение падает до 0.3 то, если их поменять местами, вижу, что напряжение возрастает до 0.5, но в течении пары минут падает до 0.4. И если каждый раз так менять катоды с периодом в семь минут, то напряжение меньше 0.35 вольт не упадет. Я так подумал, а что если катодов будет не два а пять, к примеру, то время смены можно уменьшить, а среднее напряжение возрастет.Про это я сумел найти только то, что при прерывистом разряде большими и средними токами работоспособность батареек заметно увеличивается по сравнению с непрерывным режимом работы.С тем же эффектом можно второй катод и не вынимать из раствора, а лишь провод коннектить то с одним, то с другим катодом... То есть если сделать некий электронный прерыватель работающий на той же батарейке которую он и регулирует, который переключатся между катодами, то напряжение можно усреднить и до 0.5 вольт. Я не физик, и не так хорошо знаком с электроникой, но мне кажется это очень интересным Итак, мои вопросы:1. Почему так происходит с двумя катодами?2. Какие все же реакции протекают в таком элементе?
Итак, мои вопросы:1. Почему так происходит с двумя катодами?2. Какие все же реакции протекают в таком элементе?
HNO3+NO2+KNO2=?
в Неорганическая химия
Опубликовано
Ладно...
Изначально я думал о чистом калии как о электроде, но он очень уж бурно реагирует со всеми электролитами...