
Олег74
-
Постов
68 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Олег74
-
-
Осуществима ли данная цепочка превращений? Если осуществима, то какие растворители и катализаторы необходимо использовать?
-
В Кишинёве в институте химии в Советское время широко занимались индольной тематикой,наработано множество монографий и кандидатских. Г. Жунгиету был лучшим и можно найти его литературу
Спасибо!
-
Подскажите способы получения N-метилиндол-3-карбоновой кислоты, желательно с хорошим выходом. Можно ли получить данную кислоту по реакции Фишера?
-
Насколько реален синтез С3H8NO5Р по следующей схеме "(OH)2P(O)CH2NH2 + CL2CH2COONa ----> HOOCCH2NHCH2NHCH2P(O)(OH)2"? Может быть кто - нибудь проводил подобный синтез, каким образом?
А данное вещество не относится к ФОВ ?
-
Конечно, т.к. известно, что индолы в кислой среде нестабильны.
А зачем это делать, что хотите в итоге получить?
да провёл реакцию, просто выпал твёрдый нерастворимый осадок фиолетового цвета. Вот и захотелось узнать что это.
-
Будет ли реагировать индол-3-карбинол с соляной кислотой? Если реакция возможна, то будет ли растворяться продукт реакции(в чём лучше)?
-
Растворитель, тот в котором делали реактив Гриньяра обычно эфир либо тгф, температура, обычно чтобы избежать побочных реакций ее понижают до минус 78 градусов ( эту температуру дает сухой лед).
Какие могут быть продукты реакции?
-
Помогите определить условия проведения реакции. Нужен ли растворитель, если да, то какой и какая должны быть температура?
-
Всем доброго времени суток. Интересует вопрос о защите нитрогруппы в реактиве Гриньяра. Если можно защитить нитрогруппу в Гриньяре, то как это сделать и как снять защиту?
-
3-хлор-2-метоксифенил - это для меня просто радикал. Он может быть, может не быть. Суть в том, что диизопропиламид лития - сильное основание, с заторможенной нуклеофильностью. Роль его здесь может сводиться только к катализу конденсации сложного эфира с нитроолефином. Охлаждение до -50С предотвращает сложноэфирную самоконденсацию.
Если хотите, то в общем виде это так будет:
Такое моё ИМХО

Теперь точно ясно, спасибо)
-
Спасибо, там эфир немного другой, но механизм я понял) Я так понял, что реакция не пойдёт, если убрать 3-хлор-2-метоксифенил?
-
11,1 мл (17,8 ммоль) 1,6М н-бутиллития в гексане добавили порциями к 20 мл раствора 2,5 мл (17,8 ммоль) диизопропиламина в тетрагидрофуране при перемешивании в условиях охлаждения смесью сухой лед/ацетон. Через 15 мин после завершения добавления к смеси порциями при -50оС или ниже добавили 30 мл раствора 4,13 г (17 ммоль) сложного эфира, полученного в вышеуказанной стадии 4, в тетрагидрофуране. Смесь перемешивали при такой же температуре в течение 10 мин и к смеси порциями добавили 100 мл раствора 3,55 г (17 ммоль) нитроолефина в тетрагидрофуране. Смесь перемешивали в течение 30 мин и к реакционной смеси добавили воду. Полученную смесь подкисляли 2н. раствором соляной кислоты и экстрагировали метиленхлоридом. Фазу метиленхлорида промывали соляным раствором и сушили над безводным сульфатом магния. Эфир полученный в стадии 4 Этил-3-хлор-2-метоксифенилпропионат. Спасибо за помощь.
-
Всем доброго времени суток. Подскажите пожалуйста возможные методы синтеза 2-оксо-1-пирролидинметил-4-этаналя.
-
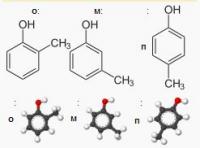
Какая у него структурная формула, подскажите пожалуйста.
-
из Химическая технология органических веществ (Дьячкова, 2007)
Но обычно, диизопропиловый эфир получают прогонкой пропилена над Ca3(PO4)2 при 260-319 С с конверсией 7-33%, т.к. при дегидратации изопропанола и высших спиртов идет побочная реакция образования олефинов
Спасибо, исчерпывающий ответ!)
-
Всем доброго времени суток, подскажите пожалуйста при какой температуре лучше синтезировать диизопропиловый эфир, путём дегидратации с серной кислотой?
-
Я полагаю, его налили из баночки.
Да, я не так прочитал.
-
там где прочитал про этот метод реакция шла 3 часа, потом добавлялся водный раствор поваренной соли, потом экстракция эфиром. потом опять промывка солевым раствором и потом уже отделение из эфира более менее чистого...
подробнее так
Общая процедура: смесь 557 мг бензилового спирта, 0.15 mL HBR (48 %) и 5 mL DMSO перемешивали на масляной бане при 100C. Реакция закончилась через 3 часа. К реакционной массе добавили 5 мл морской воды (раствор натрия хлористого), и потом экстарагировали 30 мл диэтилового эфира. Эфирный слой был промыл соленой водой (4x5 мл). Выпарив эфир и остаток перегоняем получив 530 мг бензальдегида с выходом 95 %.
там же было еще про метод окисления нитратом железа(3) в водно-этилацетатной(ацетоновой) смеси.
оффлайновая копия ныне выпиленного сайта.
как там диэтиловый эфир появился?
-
С чего это вы взяли? Йодистоводородная кислота - одна из самых сильных кислот, а винная
ей в подметки не годитсягораздо слабее.Ладно, спасибо.
-
Столько реактивов зря загубили. Ну, окислился чуток KI кислородом воздуха, от того и смесь кислоты и соли немного покоричневела и окраску дает на крахмал, так это для KI обычное дело, а так, не было реакции никакой.
Но винная кислота сильнее чем йодоводородная, должен был НI образоваться и пройодировать ОН-группу?
-
Реакция проводилась следующим образом: 150 грамм винной кислоты растворил в кипящей воде, затем, при перемешивании добавил 332 грамма йодида калия. Далее выпарил воду. В итоге получилась светло коричневая соль, без запаха. Раствор крахмала окрашивался в фиолетовый цвет (как йодом). Какие продукты получились?
-
При каких условиях протекает реакция? Должен быть спиртовой раствор?
-
будет и без пергидроля
А полимеризоваться не будет?
-
При взаимодействии пропиоловой кислоты и бромоводородной кислоты в пергидроле будет образовываться β-бромакриловая кислота?
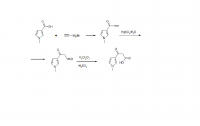
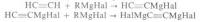
Цепочка превращений
в Органическая химия
Опубликовано
По идее там будет получаться смесь кетона и альдегида, т.к. там уже есть альдольная группа, которая является электроноакцепторной группой.
Мысли читаете) Но меня больше интересует температура реакции Гриньяра и можно ли использовать диизопропиловый эфир?