-
Постов
24 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Lapitskaya
-
-
Aversun, как быть с цинком и фосфорной кислотой,
Т.е. реакций пойдет, до образования защитной солевой пленки?
-
Но реакция свинца с серной не идет.
-
-
ДМФА растрогается в испарителе и отсекается. Его не видно. Он не причем.
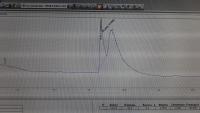
Обновили сообщение. Вижу хроматограмму. Она плохая. Удлините колонку.
Читала когда-то, что уменьшение длины колонки на 1-2 м на анализ не сильно влияет. Видимо я уже больше наотрезала) ну да колонка давно работает. Т.е. Вы имеете ввиду ставить новую колонку? А может тут с НЖФ что-то?
-
-
Может быть ДФМА?
-
День добрый!Значит у вас два соединения на выходе. Стерины не колол, но терпены колол. Был случай, когда вещество (функционализированный дитерпен) разлагалось на два в испарителе, что давало два сигнала далеко друг от друга. У вас как, я понял, сигналы близко. Это означает, что у вас изначально было два похожих соединения; так себя ведут диастереомеры.
Может кто-то сталкивался с такой проблемой. Анализ стеринов на ПИД хроматограф Agilent 7890A. Пик холестерина начал раздваиваться. Как это устранить? Заранее спасибо за помощь.
-
приму к сведению, как надо выкладывать.
спасибо, что откликнулись
да, просчиталась ,там получается не стирол, а этилбензол.
-
-
да
спасибо!!!)
-
поняла все
 спасибо
спасибо -
я поняла : ) большое спасибо)
-
-
Уважаемые химики. Не откажите в помощи, посмотрите задачу:
Вычислить нормальность раствора щелочи NaOH, если 100гр 60% раствора щёлочи разбавили водой до 500мл
нормальноcть вычиляется по формуле: Cн=n/(f*V)
m(NaOH)=w(NaOH) * m(p-pa NaOH) = 0.6*100 = 60 г - растворенного вещества
n(NaOH)=m/M = 60/40 = 1.5 моля
теперь расчитаем массовую долю гидроксида натрия после прибавления 0,5 л воды
w(NaOH) = 60/600 = 0.1 или 10%
в принципе плотность можно принять равно единице, так как раствор разбавленый, но все таки
в справочнике В.А. Рабиновича нашла, что при массовой доле 10,10% плотность равна 1,110 г/см3
нужно найти объем раствора
V(p-pa)=m/p = 600/1,110 = 540, 54 см3 (или мл) = 0,54 л
осталось вычислить нормальность
Сн = 1,5/0,54=2,78 н
Верно ли?
Заранее спасибо : )
-
наконец-то добралась до этой задачи.
CnH2n-2 +2Br2 = CnH2n-2Br4
получается, что алкина 0,2 моля
х - количество вещества алкина, у - количество вещ. пентана
m(алкина)=0,2(14n-2), а масса пентана 72у, тогда 0,2(14n-2) + 72у = 11,6
теперь второе уравнение
СnH2n-2 + (n-1)/2 O2 = nCO2 + (n-1)H2O
C5H12+ 8O2 = 5CO2 + 6H2O
до этого вычислила количество вещества углекислого газа n(CO2)=0.85 моля, значит
nx + 5y = 0.85
выразим отсюда y: y = (0.85-0.2n)/5
и подставим в первое уравнение:
2.8n - 0.4 +72y = 11.6
2.8n - 0.4 + 72* [(0.85-0.2n)/5] = 11.6
решая относительно n, получила
n=3 - значит это пропин C3H4
значит y = 0.05 моля, а х=0,2 моля
соответствующие массы исходных веществ будут: m(C3H4)=8 г, m(C5H12) = 3.6 г
Уважаемые химики, верно ли мое решение?
-
верно ли, что титан в с.о. +4 проявляет амфотерные свойства?
верны ли следующие реакции:
Ti(OH)4 + 4HNO3 = Ti(NO3)4 + 4H2O - здесь гидроксид титана (IV) должен быть свежеприготовленным?
TiCl4 + 4NaOH = Ti(OH)4 + 4NaCl
TiO2 + 4HNO3 = Ti(NO3)4 + 2H2O
Подскажите, пожалуйста, на какие вещества может разложиться четыреххлористый титан (и при каких условиях)
TiCl4 = ?
какие продукты могут образоваться при такой реакции:
Ti(OH)4 + NaOH = ?
заранее спасибо.
-
эл. конфигурация самария [Xe]6s24f6
т.е в невозбужденном состоянии самарий может образовывать 6 связей, а в возб. получается восемь. Возможно ли, что электрон с 6s -подуровня спрыгнет на 4f? может ли все шесть неспаренных электронов быть валентными?
хотя для самария характерны +2 и +3 степени окисления.
а для железа характерны +2 и +3 степени окисления, но железо же может в комплексах образовывать 6 связей
Подскажите, как будет. Заранее спасибо!
-
Реакция с бромом неверна, учтите, что там тройная связь
как-то странно находили массу р-ра NaOH через массу р-ра NaOH
тем не менее с n(CO2) можно согласиться
Далее надо принять количество пентана за х моль и
количество алкина найти через количество брома
и составить два алгебраических уравнения с двумя неизвестными х и n (в формуле алкина)
В смысле реакция с бромом неверна, там ничего не меняется, кроме того, что бром присоединяется
-
-
-
Все правильно кроме последней реакции, там в продукте будет не NO2, а ONO2
да! там сложный эфир будет
-
C6H12O6 = 2C2H5OH + 2CO2 (спиртовое брожение глюкозы)
C2H5OH + HBr = C2H5Br + H2O
C2H5Br + KOH (c2h5oh) = C2H4 + KBr + H2O
3 C2H4 + 2KMnO4 + 4H2O = 3 CH2 - CH2 + 2MnO2 + 2KOH
| |
OH OH (этиленгликоль)
CH2 - CH2 + 2HNO3 = CH2 - CH2 + 2H2O
| | | |
OH OH ONO2 ONO2 (нитрогликоль)
-
11,6 г смеси алкина с пентаном может присоединить 64 г брома. Для полной
нейтрализации углекислого газа, полученного при сгорании этой смеси, потребовалось 355.6 мл 17%-ного раствора едкого натра, плотность которого равна 1,125 г/мл. Определить качественный и количественный состав исходной смеси
Жду помощи!







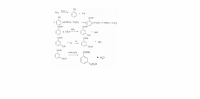
Ме+кислота
в Решение заданий
Опубликовано · Изменено пользователем Lapitskaya
Aversun, т.е. это актуально только со свинцом и серной кислотой?