-
Постов
26 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные kap100
-
-
Спасибо! Можете ли подсказать источник, таблицу вероятностей захватов атомами разных элементов нейтронов?
-
p.s. вероятность захвата для быстрого нейтрона: Н - 0,08; D - 0,12; а для теплового H - 0,33; D - 0,00057
Испускается гамма-квант и результирующее ядро тоже получает некую дополнительную энергию
Получается, что дейтерий с большей вероятностью захватит быстрый нейтрон?
Все ли элементы таблицы Менделеева могут захватывать нейтроны, увеличивая массовое число не единицу?
-
В обеих реакциях захват сопровождается выделением энергии в ~2 МеВ
Уточните (я не химик) что значит "выделением энергии в ~2 МеВ"? Она выделяется в виде гамма-квантов или в виде кинетической энергии?
-
-
Во-первых, не 15, а 12.
Во-первых, не 12, а 887,7 сек, что равно 14,795 мин. Читайте научные статьи - http://arxiv.org/pdf/1309.2623v2.pdf . Хотя, даже в Википедии написано 15 мин. А период полураспада равен 611 сек, что тоже НЕ равно 12 мин.
-
-
Ерунду пишут в этих учебниках. Читайте правильные учебники. Это ядерные реакции. Да и идут они в условиях, когда нейтральные атомы просто не могут существовать.
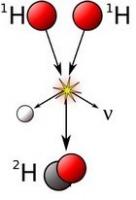
Реакцию в "атомном" виде я нарисовал выше. Электрон никуда не пропадает, он с позитроном реагирует. Впрочем, если хотите, можно и так нарисовать:
H + H = D + v + e- + e+
Утверждается, что β+ распад не может происходить ВНЕ ядра. Протон захватывает один орбитальный электрон, превращаясь в нейтрон (электронный захват). А схема протон-протонного цикла показывает как два отдельных протона, без электронных оболочек, сталкиваются и один из них превращается в нейтрон, без участия в столкновении электрона. При этом тот же нейтрон в свободном состоянии распадается с выделением электрона. В протон-протонном коллайдере столкновение протонов никогда не приводит к образованию нейтронов, а лишь к адронизации. Встречается ли где-то ещё образование нейтрона от столкновения двух протонов, кроме теории протон-протонного цикла?
-
-
Непонятная у вас арифметика. Было два плюса, стало два плюса. Ничего никуда не пропало.
Повторяю вопрос - А заряд отрицательный куда делся?
-
В описании протон-протонного цикла слияния двух атомов водорода и образование гелия, не понятен следующий момент - После столкновения атомов водорода получается атом дейтерия, позитрон и нейтрино. Позитрон уносит положительный заряд одного из столкнувшихся протонов, ставшего, в результате бета+ распада нейтроном. Если позитрон уносит положительный заряд протона то куда делся отрицательный заряд поглощённого электрона? Поглощение электрона приводит к изменению одного из кварков протона с "u" на "d". А заряд отрицательный куда делся?
-
Есть такой способ казни - .......
А по существу вопроса что-то есть?
-
В Вольтах. Относительно электролита. Будет катод под напряжением, достаточным для выделения железа из раствора железного купороса- выделится железо, несмотря на то, что водороду выделиться проще.
Что значит "относительно электролита"? Мы говорим о приближении отрицательного электрона к отрицательному катоду. По-вашему получается, что можно сравнить напряжение единичного электрона с напряжением на катоде. И, в зависимости от разности напряжений (раз в вольтах) электрон определяет приближаться ли ему к катоду или нет? (пост 23).
-
Еще более отрицательный потенциал источника питания.
В чём измеряется более или менее отрицательность катода источника питания?
-
Аккумулятор играет роль насоса, который гонит воду по трубе.
А можно подробнее насчёт аккумулятора и его роли как насоса? Электрон на аноде, полученный от аниона, бежит по цепи в сторону положительного полюса (давайте возьмём не аккумулятор, чтобы не примешивать химические реакции в аккумуляторе, а трансформатор от сети с выпрямителем), пробегает по вторичной обмотке трансформатора (или делает круг до электростанции и обратно), тянется к отрицательному полюсу (отрицательный электрон?), проходит через нагрузку (лампочку), зажигая её, и идёт к отрицательному (опять же) катоду. Не совсем понятно какие силы заставляют отрицательный электрон приблизиться к отрицательному катоду?
-
По-моему,объясняя процессы в электролите,вы не ответили на вопрос ТС. Насколько я понял ему не ясно,что электрон разрядившегося аниона и бежит через проводник,который зажигает лампочку,а прибежав через лампочку к противоположенному электроду,садится на катион,и разряжает его.
Правильно ли я понял — электрон аниона попадает на анод и идёт по цепи через лампочку, аккумулятор и приходит к катоду, тем самым перенося заряд от анода к катоду? Тогда пару вопросов — какой заряд у катода, если к нему бежит отрицательный электрон? И какую роль играет аккумулятор в цепи?
-
Нет, это происходит в химических источниках тока (батарейки, аккумуляторы). При электролизе именно разряжаются на электродах.
Чтобы "разрядиться" необходимо этот заряд где-то взять. Есть два варианта: 1 - получить заряд на противоположном электроде, 2 - зарядиться в момент диссоциации, когда одна половинка диполя получает положительный заряд, а вторая отрицательный. Первый вариант отметается схемой электролиза по современным представлениям. А второй вариант - это схема выработки собственного тока... Какой из них правильный?
-
Нет, процесс диссоциации идет в любом случае, а вот протекание тока объясняется разрядом анионов и катионов на электродах.
Получается, что анионы и катионы являются источниками тока, раз они разряжают собственные заряды на электродах, а не берут эти заряды с противоположного электрода.
-
Заряды от одного электрода к другому не переносятся.
Тогда получается, что процесс диссоциации является процессом выработки тока? Раз ионы приносят собственные заряды на электроды.
-
Переносчиком являются катионы и анионы, когда их не остается проводимость прекращается. В вашей схеме когда кончится хлор, начнется электролиз воды, а вот когда кончится вода, ток прекратится.
То, что переносчиками являются катионы и анионы, я слышал не раз. Хотелось бы подробнее узнать о схеме переноса заряда от одного электрода к другому.
-
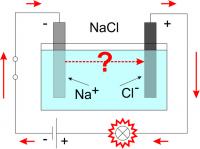
Не могу понять как протекает ток в электролите при электролизе. Например, в растворе соли молекула NaCl делится на два иона - катион и анион. Катион уходит к катоду, а анион, соответственно, к аноду. При внешнем источнике тока, чтобы лампочка загорелась, мы должны замкнуть цепь. Как известно соль проводит ток и лампочка горит. Но процессы не совсем понятны. Если катион и анион из раствора расходятся к электродам в разные стороны то что является переносчиком тока от одного электрода к другому? Показываемая во всех учебниках схема это схема батарейки, когда катион и анион сами являются источниками тока. А в данной схеме у нас есть внешний источник тока, ток которого просто надо передать от одного электрода к другому.
-
В процессе изучения химии (самостоятельно) возник вопрос по соответствию разных её частей единой концепции. При объяснении строения атома и распределения электронов по уровням используют планетарную (орбитальную) модель. Насколько известно, планетарная модель Бора строения атома считается устаревшей. Вместо электронных орбит, распределяющих электроны послойно (по орбитам), используется термин "орбиталь", обозначающий зону, в пределах которой электрон может находиться с определённой долей вероятности. Орбитали имеют разную форму, размеры и ориентацию относительно друг друга. Уравнение Шрёдингера говорит о вероятности нахождения электрона в конкретной точке в конкретный момент. То есть, электрон, перемещаясь внутри своей орбитали, в разный момент времени, может находиться на разном удалении от ядра (в пределах своей орбитали). Следовательно, электроны уровня s в какой-то момент могут находиться выше (дальше) валентных электронов, например, уровня p. Тогда возникает вопрос - чем доказано, что химическая связь образуется именно внешними (?) валентными электронами, если они находятся на расстоянии от ядра с такой же вероятностью как и электроны других орбиталей?
-
В газовой фазе ионы ведут вполне самостоятельное существование. Это, собственно, и в жидкости возможно, если отвлечься от того факта, что в жидкости ионы сольватированы, т.е. взаимодействуют с молекулами растворителя.
Получить ион можно разными способами, но исходником всегда будет нейтральный атом (нейтральная молекула или кристалл). Можно получить в каком-то объёме плазму - смесь катионов и анионов, но в целом этот объём будет нейтральным. Можно из этого объёма удалить часть ионов одного знака, тогда этот объём будет заряжен, но удалённые противоионы надо куда-то деть, где-то их держать. Можно удалить их хоть за орбиту Плутона, но разделение зарядов останется, ибо Вселенная наша электрически нейтральна, а электрический заряд не может исчезнуть, благодаря фундаментальному закону сохранения заряда.
В результате - у каждого иона где-то в мире болтается противоион.
Разобрался немного в плазме и свободных ионах. Понял, что свободный ион в плазме это атом потерявший электрон и ставший, в результате этого, положительным ионом.
Но вопрос остался, только более точный - Может ли свободный атом (либо в плазме, либо ещё где-то) иметь ЛИШНИЙ электрон? Повторяю, атом не связанный в молекуле, а ОТДЕЛЬНЫЙ атом с лишним электроном.
-
Возник новый вопрос. Может ли ион быть отдельным САМОСТОЯТЕЛЬНЫМ атомом, с количеством электронов, не соответствующим количеству протонов? Или ион это атом, контактирующий с другим атомом, у которого он либо отбирает электрон, становясь анионом, либо отдаёт свой, становясь катионом? В результате чего в данной группе количество электронов всё-равно остаётся равным количеству протонов. Интересует именно ОТДЕЛЬНЫЙ атом, а не группа атомов (молекула).
-


Нейтронный захват
в Физическая химия
Опубликовано
Супер! Я нашёл его по адресу http://www.iaea.org/inis/collection/NCLCollectionStore/_Public/27/030/27030255.pdf Ещё раз спасибо!