-
Постов
42 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Серафима Авер
-
-
В лаборатории проводили калориметрический опыт. Определяли теплоту окисления щавелевой кислоты перманганатом калия. Расчетное значение из опыта получилось 347 кДж/моль. Известно, что теплота процесса сгорания щавелевой кислоты приблизительно равна 246 кДж/моль. Интересует такой вопрос: а может ли она совпадать с теплотой окисления, измеренной в опыте?
-
Не знаю, как решать номера 4 и 5. Объясните, пожалуйста))
-
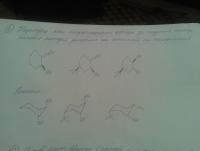
Решала задания по органической химии. Однако преподаватель зачел не все. Посмотрите, пожалуйста, где у меня ошибки в заданиях? Что нужно исправить? Нужно мнение профессионалов
 Заранее спасибо)
Заранее спасибо) -
Закон Бугера-Ламберта-Беера
По закону A=elC, значит, е=А/lC. но если мы проводим измерения относительно раствора сравнения, то как посчитать е?
-
Не понимаю, как решить такую задачу((
 знаю, что не сложная, но ума все равно не хватает, помогите пожалуйста
знаю, что не сложная, но ума все равно не хватает, помогите пожалуйста  Определите молярный коэффициент поглощения K2CrO4, еслиотносительная оптическая плотность 2,65×10–3 М раствора, измереннаяпри l = 372 нм в кювете с l = 2,3 мм, по отношению к раствору сравнения,содержащему 10–3 моль/дм3 K2CrO4, оказалась равной 1,380.
Определите молярный коэффициент поглощения K2CrO4, еслиотносительная оптическая плотность 2,65×10–3 М раствора, измереннаяпри l = 372 нм в кювете с l = 2,3 мм, по отношению к раствору сравнения,содержащему 10–3 моль/дм3 K2CrO4, оказалась равной 1,380.
-
Ах, да, пардон, я не учел константу равновесия. Сейчас попытаюсь исправиться

Условия задачи приведены полностью. Я несколько раз пересчитала, у меня либо 100 процентов выход получался, либо абсолютно другие числа, но 92 ни разу не вышло. Так как я только начала осваивать эту тему, уверенности в решениях нет никакой =( Спасибо за ответ, попробую порешать что-то еще.
-
-
Может, не сульфатной, а серной? 0,6 л и того, и другого
-
Для реакции A+B=D+E, константа равновесия которой равна 6, взято 2л 3М раствора вещества А и 3л 5М раствора вещества В. Определить выход вещества D.
-
Что образуется в результате этих реакций?
(NH4)2MoO4+KI+H2SO4 =
Na2WO4+KI+H2SO4=
как называется данное соединение: MoO3*Mo2O5?
Как изменяется окислительная активность соединений в высшей степени окисления при переходе от хрома к вольфраму?
-
Помогите ответить на вопросы в методичке:
Реакция гидролиза хромита натрия - ?
Что гидролизовано сильнее: хромит натрия или хлорид хрома (III)?
-
а) Выделяется очень много газа
б) У этой реакции весьма нехилый ΔG
Спасибо
-
Почему реакция разложения дихромата аммония проходит очень бурно?
-
-
Какой из гидроксидов цинка – обычный Zn(OH)2 или комплексный [Zn(NH3)4](OH)2 – и почему является более сильным основанием?
-
Я воду оказывается не учла, вот почему не получалось написать уравнение рекции. Спасибо!Уж настолько известная реакция
можно конечно написать так
2MnSO4 + 8HNO3 + 8H2O + 5K2S2O8 = 2KMnO4 + 8KNO3 + 12H2SO4
но я бы азотную вообще не учитывал, потому что это только среда
2MnSO4 + 8H2O + 5K2S2O8 = 2KMnO4 + 4K2SO4 + 8H2SO4
-
Поместили в пробирку немного кристаллов пероксодисульфата аммония (NH4)2S2O8, 2 мл 2н HNO3 и 10 капель AgNO3, нагрели пробирку почти до кипения и добавили 1 каплю раствора MnSO4.
Наблюдали сначала помутнение раствора, затем при нагревании раствор стал розовым, при добавлении сульфата марганца раствор посветлел.
Нужны уравнения реакций, помогите пожалуйста )
-
ну ни как вам не удается написать правильно формулу, это, похоже, уже тенденция
Подождите-ка, осадок коричневый, не сиреневый? А точно с желтой кровяной солью, а не с красной?
Чего-то я запутался, вроде сначала в заголовке была желтая соль?
Если с красной, то вы написали уравнение правильно, а результат будет таким
MnCl2 + K3[Fe(CN)6] = K[MnFe(CN)6] ↓ + 2KCl
коричневый осадок
А вот если с желтой, тогда осадок фиолетовый
2MnCl2 + K4[Fe(CN)6] = Mn2[Fe(CN)6] ↓ + 4KCl
да, мне красная кровяная соль и нужна. Теперь всё сходится. Спасибо большое!
-
4[Fe( CN)6]·3H2O это желтая кровяная соль...
А предыдущая формула, значит, красная соль...
всё, я поняла. Извините, запуталась.
Значит, мне нужна реакция с красной кровяной солью.
quote name="aversun" post="935537" timestamp="1432658158"]сначала формулу желтой кровяной соли напишите
-
у нас на лабораторке только такая штука была :Dэто не желтая кровяная соль
Тогда как с ней будет хлорид марганца реагировать? Какие продукты реакции? У нас получился коричневый осадок.
-
MnCl2+K3[Fe(CN)6]→?
-
-
-





Теплота сгорания и теплота окисления
в Решение заданий
Опубликовано
Спасибо за ваши ответы)