-
Постов
117 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные 777schenok777
-
-
полученное не стал выкидывать, а убрал в плотно закрытый полиэтиленовый пакет, вещество превращается в рыхлую белую массу, по всей видимости в бензойную кислоту.
-
В чём смысл данной темы? Показывать форумчанам картинки из википедии и химической энциклопедии?
смысл создания темы заключается в изыскании методов получения альдегидов и кетонов, тема уже проработана, просто она пока сюда не выложена, кроме того является недоработанной, так же сюда планировалось писать о протонных и апротонных растворителях и возможности присоединения их молекулярной структуры, или её части во время синтеза к конечному продукту, а так же о апротонных нитрующих агентах, возможно эти темы будут объединены в отдельную ветку, просто не было времени этим заниматься и тема получилась не интересной, позднее я всё это исправлю, тему можно удалить по вашему желанию и потом попробовать переписать более интересным языком и более доходчиво, мне самому не понравилось такая размытость и уход от химии в сторону вытяжек из растений и тому подобных вещей взятых из википедии.

-
И что? Полученный при этом Cu(HSO4)2 не будет растворяться в H2SO4?
ты прав хотя бы потому, что таким "лёгким путём" ни кто не поступает, а поступают перегоняя азеотроп и измеряя температуру испарений в месте входа испарений в холодильник, ну или как парень фото выкладывал в начале - через дефлегматор, но моё личное мнение(может быть и ошибочное) заключается в том, что через дефлегматор или вертикально установленную стеклянную трубку (ТС, кварц) наполненную битым стеклом(тот же самый дефлегматор) гнать опасно, серку вообще гнать опасно, она склонна к перегреву, в литературе в сети я читал, что серка может перегреться как раз из-за того, что дефлегматор установлен вертикально и работает как обратный холодильник, при перегреве серка стрельнет через этот дефлегматор в потолок, возможно такое или нет я не знаю, не проверял, но сам считаю, что логика в этом есть, так что и температуру в этом случае требуется отслеживать или выставлять температуру самой плитки так, что бы перегрев был исключён, то есь нужно знать свою плитку.
-
Надо найти в сети и скачать Плющев В.Е., Степин Б. Д., Химия и технология лития, рубидия и цезия, М., 1970
Нагрев требуется, если разность теплот образования (энтальпий) конечных и исходных не шибко отрицательная. Тогда заметной экзотермической реакции не будет.
Но если один из продуктов летуч (например магний и щел. металлы кипят в районе тысячи градусов), то его можно отгонять (при атмосферном давлении, в вакууме или с потоком газов).
Для Al2O3 энтальпия образования −1675,7 кДж/моль
Для MgO -601,8 КДж /моль
2Al + 3MgO = Al2O3 + 3Mg
-1675 -(-3x602) = 131 кДж/моль - реакция эндотермическая, надо греть для смещения равновесия вправо.
Al + 2KOH = KAlO2 + К + H2
KAlO2 -1109
KOH -426
-1109-(-2х426)= - 257 кДж/моль - заметная экзотермическая реакция, рост энтропии.
ok спс
-
как то пару лет назад делал я это следующим образом, долго искал, но в консэ консов попалась таки мне 6-ти литровая термостойкая колба, пошёл я на автозаправку, заглянул в прилежащий магазин сопутствующих товаров, да и купил там две 5-ти литровые канистры элека, стоил он тогда аж 180 целковых, таки да. А на следующий день я пошёл в соседнюю близлежащую автозаправку и купил там ещё две канистры точно такого же электролита, за те же самые деньги.
---------------------------------
Как я парил элек:-
предварительно прочитав массу разной литературы и прийдя к выводу, что 99.9% серка мне ни к чему, так как на все известные мне синтезы хватает и 94-96% H2SO4, в редких случаях правда из-за такой серки падает выход, но тут ужо ничего не поделаешь. И решил я - сто рублей не деньги, поставил на балконе квадратный пластмассовый тазик с песком, положил на него доску, сверху поставил плитку, наверх водрузил 6-ти литровую колбу, залил в неё первую 5-ти литровую канистру электролита плотностью 1.28, да и упарил её вчетверо немного недопаривая, так как после выключения плитки серка продолжает улетать вместе с водой ещё 15-20-ть минут, сам процесс очень долог, занимает целый день, так как колба стоит не на банях-шманях, на которых серку выпаривать вообще невозможно, во всяком случае на моей плитке, а прямо на рабочей поверхности плиты, большую часть времени занимает сам нагрев, так как если сразу поставить температуру на 4-5-6 то стекло может лопнуть, что происходило у меня далеко не раз с французскими термостойкими стеклянными чайниками, гусятницами и посудой для микроволновок, благо в те разы там не находился литр конц. серки разогретой до 330-ти градусов, но было очень неприятно, особенно когда залило серкой плиту на кухне, эмаль покрывается чёрной сажей, но к счастью эмаль качественная, удалось оттереть без последствий. Постепенный нагрев 6-ти литровой колбы занимает 2-3 часа, ну а дальше всё само парится, надо только начало процесса заметить, что бы сильно не стреляло и кипелок никаких не надо, так как через 1-2 часа работы они захлёбываются, а парить целый день, кипелки использовались из битой керамической пасуды, работают хорошо, но только первые 2, максимум 3 часа, а парить целый день как уже и писал, далее присматриваешь краем глаза, в случае экстренной ситуации всё окажется в тазике с песком, особо напуганные могут перемешать песок с содой, но вряд ли от этого станет лучше в случае ЧП. Таким образом за три дня я и напарил себе канистру кислоты, остатками которой пользуюсь до сих пор. Пробовал ли я пользоваться холодильниками? Да пробовал и скажу что это всё лишний геморой, если отогнать вам надо 200грамм, то это можно понять, а если перегонять 2-3 литра вы проклянёте всё пока перегоните необходимое количество, воду подключать к холодильнику нельзя, так как со временем он начнёт разогреваться и станет таким же горячим как колба - 300 градусов, а ТС стекло выдерживает перепад температур только в 200 градусов, - вывод прост, холодильнику придёт конец, далее холодильник без воды нормально конденсирует только первое время, когда его температура сравняется с температурой колбы он точно так же начнёт выплёвывать зловонные белые пары. Варианты с дефлегматором не проверял, возможно это и имеет смысл, но в любом случае, на такое количество вы потратите месяц времени - ах-хах-хах-хах-хах - весело, - хотите это проверить? - удачи))) У меня на всё про всё ушло 4 дня, парил я не каждый день, поэтому потратил неделю, при том возле плитки находился короткий промежуток времени, всё гналось(парилось) само(!).
-
 1
1
-
-
Монохлоруксусная кислота
СН3СООН СН2СlСООН над стрелкой Cl+, под стрелкой HCl- соответственно
СН2СlСООН над стрелкой Cl+, под стрелкой HCl- соответственно
Исходные материалы
Уксусная кислота (ледяная) - 120,0г.
Фосфор красный - 10,0г.
Хлор (в бомбе)Посуда
Колба круглодонная (250)
с обратным холодильником
Колба Вюрца (250)
Воронка Бюхнера
Колба (500)
Продолжительность 2—3 дня
В круглодонной колбе, снабженной обратным холодильником, нагревают
на водяной бане смесь из 120 г ледяной уксусной кислоты и 10 г
красного фосфора и затем при освещении, лучше всего на ярком солнечном
свету, пропускают из бомбы ток хлора, промытого H2S04 (1,84) и высушенного
над СаСl2. Скорость пропускания регулируют так, чтобы через
склянку с H2S04 проходило 3—4 пузырька газа в 1 сек. Выделяющийся HCl
отводят при помощи изогнутой трубки, соединенной с верхним концом
холодильника, в поглотительный сосуд с водой (конец трубки не должен
касаться воды). Хлорирование 'продолжают до тех пор, пока взятая проба,
смешанная с небольшим количеством ледяной воды, не начнет застывать.
Скорость процесса хлорирования зависит главным образом от интенсивности
освещения.
Продукт реакции фракционируют, собирают фракцию, кипящую от 150
до 200°, и охлаждают ее до 0°. Хлоруксусная кислота закристаллизовывается,
и ее быстро отсасывают. Маточник вторично перегоняют и получают еще
некоторое количество кристаллов хлоруксусной кислоты. Обычно полученную
кислоту перегоняют повторно. Т. к. 185—186°; т. п. 63°.
В ы х о д : колеблется между 66,5—100 г (32—52%). -
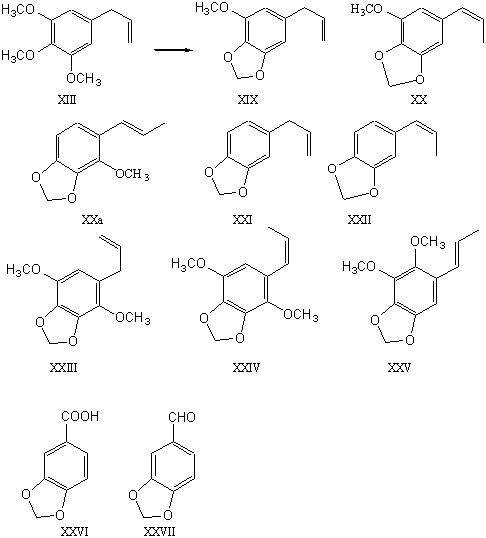
Сафрол и изосафрол тоже вроде бы в списках прекурсоров и купить какое-либо сырьё с ним вряд ли просто.
А вот пиперин из чёрного перца доступен всем, тут даже тема была.
Окисляется он также, разве что для удобства, может, лучше сначала гидролизовать его до пипериновой кислоты щелочью (в спиртах или гликолях).
Китайцы пиперин предлагают по 30000р за кг. Если его в перце 5 %, то на кг надо где-то под 30 кг перца.
Ещё ванилин похож.

Надо его как-то деметилировать (йодоводородом в уксусной?), потом метиленировать (дибром- или дийодметаном в апротонном растворителе с щёлочью).
хорошо, если тут действительно есть люди увлекающиеся именно теоретической химией, а не сплетнями, позже я допишу начатое. Сейчас у меня нет времени.
-
Сильное прокаливание Ba(NO3)2, BaCO3 или Ba(OH)2 в токе воздуха в присутствии следов воды даёт продукт именуемый перекись бария BaO2.
Взаимодействует с серной кислотой, образует нерастворимый сульфат бария и пероксид водорода:

всем пиротехникам хорошо известно горение нитрата бария с алюминиевой пудрой, нитрат бария относительно не дорог, зачем же заморачиваться с нитратом бария, если перекись водорода и так продают совершенно свободно? Дело в том, что интересен сам пероксид бария, а так же оксид бария, как и при каких температурах их получить, я вижу, что прокаливанием, но при какой температуре? Хватит ли газовой(бензиновой) горелки, паяльной лампы? Скорее всего хватит, но каковы особенности процесса, до каких температур греть и как долго? Как собрать соответствующую установку, кто, что посоветует?
-
восстановление металлов из их оксидов и других солей.
а так же магнийтермия(!)
известный, очень популярный в советские времена промышленный способ, вернее способов этих было много, почему то в сети никаких пояснений не даётся, у кого есть ссылки на подходящую литературу, а так же прочая информация - прошу делиться.
-----------------------------------------------------------------------------------------------------------------------------------
Вопрос - Возможно ли восстановление из оксидов и(или) других солей щелочноземельных металлов с помощью данной технологии, и если это возможно, то как и в каких условиях это осуществляется?(например натрия)
Алюмотермия - какие оксиды реагируют наиболее активно и почему? Какие не реагируют? Какие существуют исключения и какие закономерности в этих процессах?!!!!!!!!!!!!!!!!!!!!!!!!!!
В общем пишем-собираем любую информацию по алюмотермии.
От себя могу добавить - только что нашёл в сети, точнее на этом самом сайте и не только про восстановление натрия из его оксида, оксид натрия получается прокаливанием пищевой соды, предположительно делается это следующим образом, берётся металлическая трубка, заглушается с одной стороны цементом, далее вносим туда соль и прокаливаем до 1000 градусов бензиновой(возможно и газовой) горелкой или бензиновой паяльной лампой, возможно лучше изготовить тигель, думаю как вариант из металлической поварёшки. Таким образом мы получим искомый Na2O
далее(взято с этого сайта вот отсюда http://forum.xumuk.ru/index.php?showtopic=14382)
Понадобится: оксид хрома (3), бихромат калия, алюминиевая пудра и порошок алюминия ( напильником наточить ), тигель большой, банка с песком, лента магниевая.
Методика. Готовится 2 смеси.
1-я: 28 граммов Cr2O3 и 10 граммов алюминиевого порошка. Все перемешать и немного спрессовать.
Нельзя использовать серебрянку для этой смеси!!!! В ней слишком много примесей!!!
2-я: 25 граммов дихромата калия и 10 граммов серебрянки ( алюминиевой пудры).
1-ю и 2-ю смесь перемешать, причем очень хорошо!!!
Все помещается в тигель ( можно использовать горшок цветочный без дырки внизу или заткнуть дырку оксидом магния, асбестом или еще чем-нибудь огнеупорным ). Тигель или горшок помещается в банку с песком до уровня смеси в тигле.
Запал для этой смеси нужен довольно сильный - пара магниевых лент или та же смесь серебрянки с бихроматом ( только ей надо посыпать сверху смесь слоем в 5 мм )- она поджигается спичками или проселитрованной бумажкой.
Реагирует интенсивно, выделяется много дыма и пыли. Лучше всего проводить реакцию на открытом воздухе!!!!!!!! И даже не пытайтесь провести такое дома!!! Пожар и сильное задымление обеспечены!!!
Вынуть остатки из тигля ( разбить нафиг ), удалить шлак.
Хром получается в виде слитка. Его можно разбить молотком, но придется постараться - кусок довольно прочный.
Примечания.
Первое. Песок в банке, тигель ( горшок ), а так же все реактивы должны быть сухими!!!!
Второе. Рекомендую увеличить количество смеси вдвое, это для лучшего проплавления шихты. С количествами меньше указанных опыт не получается - слишком большие теплопотери.
Третье. Рекомендую накрыть тигель крышкой при начале реакции - меньше тепла уходит.
И еще. Не смотрите на раскаленную смесь - она светит в УФ области, можно обжечь сетчатку глаза! Используйте кусок толстого оконного стекла ( не меньше 6 мм ) или темное стекло для фотографии.
Полученный хром довольно чист, содержит до 1-3% алюминия и все примеси из алюминия ( медь, марганец, железо). В кислотах растворяется с трудом, в соляной - лучше всего, азотная пассивирует в любой концетрации, серная медленно реагирует.можно ли восстановить барий, прокаливанием его нитрата и запустив процесс алюминотермии с его оксидом и как это должно осуществляться на практике?
-
 1
1
-
-
С теми, с которыми термодинамика обещает выделение энергии.
Там где реакция не экзотермическая (или не очень), можно смещать равновесие, удаляя один из продуктов в виде паров, понижая давление.
Например, магний и натрий можно отогнать при пониженном давлении.
если можно то поподробнее, я уже прочёл, что для некоторых реакций восстановления требуется разогрев в печи, так как процессы не идут самостоятельно, а вот про отгонку натрия слышу впервые, как это происходит на практике, где об этом можно узнать?

-
Гелиотропин производится двумя основными путями:
1. изосафрол. - окислительное расщепление изосафрола путь применим в промышленном масштабе. Примеры окислителей, которые дают хорошие выходы гелиотропина являются соли хрома(6), кислород и озон.


Метод по-прежнему используется в настоящее время - сафрол (исходный материал для изосафрола) может быть выделен из эфирных масел относительно недорого и в достаточном количестве.
Сафрол Растворим в этаноле (1:3 — в 95%-м), минеральных маслах и органических растворителях; плохо растворим в пропиленгликоле и глицерине; нерастворим в воде (образует азеотропную смесь — 7,7% по массе сафрола).
При нагревании со щелочами изомеризуется в изосафрол.


Сафрол Содержится более чем в 70 эфирных маслах, главный компонент сассафрасового масла (≈80%) и масла звездчатого аниса.
-
в чём там суть проблемы не могу понять, с одними оксидами этот процесс возможен, с другими нет, с какими возможен, а с какими нет и от чего это зависит?
ну например, можно ли получить натрий таким образом - некоторые утверждают, что можно, это как это интересно?
-------
смотрим самый первый ответ http://forum.xumuk.ru/index.php?showtopic=14382
как это он натрий алюмотермией получал интересно мне знать?
как это он натрий получал алюмотермией?
из чего?
-
Цель создания данной темы - обмен информацией.
Таким методом получил довольно много металлов - натрий, железо ( ыыы ), медь, хром, никель, марганец, кремний, бор ( точнее В12Аl ), сплавы железа ( нержавейка "домашней" выделки ).
Иногда возникают трудности. Например с ванадием. Извел кучу реактивов, дефицитного оксида ванадия (5), ванадата аммония - но ничего толком не получил. А вот сплав с железом получается прекрасно!!
У кого что есть - пишите! Сам могу осведомить о некоторых тонкостях.
Не стесняемся, спрашиваем и делимся своей информацией! Снег стаял, пора выплавлять металлы!!!
объясни более абстоятельно - каким образом и из чего ты получил натрий
-
где синтез то
я пока думаю, как только возникнут идеи что-нибудь напишу, ну а так вполне обычный вариант, выделение соответствующего альдегида путём перегонки с паром из тех растений, в которых он содержится, ну например в некоторых китайских и индийских приправах такие растения активно используются, всё это указывается в википедии, но меня интересует не получение как такового альдегида, а сам химический синтез альдегидов и кетонов.
-
интересно во всяком случае, а попробуй - патом отпишись))
-
суровый русский анекдот
пьяный полицейский, торгующий гидролизным спиртом и проститутками в подворотне подходит к бабушке-пенсионерке с больным сердцем и спрашивает:-
-вы подозрительно заторможены, чем это от вас так нехорошо пахнет?
-а, это корвалол внучёк.
-корвалол? - транквилизатор? -наркотик? -на, получи дубинкой скотина, надеть наручники, будем оформлять штраф за нарушение общественных норм, хождение по улицам в неадекватном, пьяном виде и употребление психоактивных веществ.
не смешно?
за то про войну.
-
 2
2
-
-
1.в некоторых источниках указывается что это возможно сделать сульфатом магния, в чём я лично сильно сомневаюсь, как вы считаете, возможно ли сконцентрировать 72-75% азотную кислоту, хотя бы до 85% сульфатом магния?
2.есть вариант с дегидратацией азотной кислоты фосфорным ангидридом, а так же пропись получения этого ангидрида, дегидратацией получают оксид азота N2O5, в связи с чем логично возникает вопрос, если у меня этого ангидрида мешок и мне его девать больше некуда, смогу ли я им сконцентрировать азотную кислоту?
-
-
-
Если стаканчик мерный из полиэтилена, полипропилена, ПЭТ, то ничего не будет. А, если из полистирола, то стаканчик вам больше не будет служить)))
точно так, стаканщик аказался из полистирола судя по всему, сразу покрылся белым налётом, в наше время вся эта продукция благо стоит копейки

-
Решил развести димексид (он же диметилсульфоксид). Неподумавши взял пластиковую тарелочку. Переклинило чёт, по жизни только в стекле разводили всегда. Вылил столовую ложку концентрата - видимых изменений нет, стал разбавлять горячей водой - как результат: дно тарелочки в белом налёте неизвестного состава, который не оттирается механически, не реагирует на аммиак и уксусную кислоту. Интересно стало, что это такое выпало и главное, как это что-то теперь оттирать, может кто подскажет?)
На посудине стоит маркировка 7 - прочие пластмассы, что значительно усложняет правильную постановку диагноза.
тоже самое произойдёт и в том случае, если в пластмассовый мерный стаканчик налить ацетон
-
отбеливатели и их упаривание не рассматриваем - пробовали - либо выхода вообще нет, либо он очень мал.
хлорат в домашних условиях можно получить двумя способами.
если не заморачиваясь, то берёте любой блок питания и ведёте электролиз раствора поваренной соли в течении недели, потом фильтруете чёрную жижу и перекристаллизовываете.
пример:
https://www.youtube.com/watch?v=DpC-QP2cdo0
https://www.youtube.com/watch?v=B3ZC571LrJk
второй вариант - в видео, как вы можете видеть, этот парень отводит хлор в банку с водой, а способ заключается в том, что хлор отводится в банку с раствором NaOH или KOH, в результате в этой банке точно так же получается хлорат.
-
берёжь бАлшую банку, или бутыль, наливаешь туда на донышко талуол, сверху пробку(крышку), в крышку шланчик, испаряешь толуол на солнечном свету на плитке на бане, допустим песчаной, в это время вводишь хлор в реактор через шланчик, много не получишь, но для опытов может и хватит, если вообще что то получится, а вообще пару пятисоток(лампочек) для освещения видимо не помешает. хлор можно получить добавлением серной кислоты в белизну и проганяя его через небольшую ёмкость с серной кислотой, толуол из 646-го растворителя, отмывкой его в воде и просушкой сульфатом натрия или чем вы там это делаете?
-

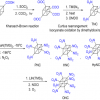
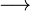 СН2СlСООН над стрелкой Cl+, под стрелкой HCl- соответственно
СН2СlСООН над стрелкой Cl+, под стрелкой HCl- соответственно





Алюмотермия
в Химическая технология
Опубликовано
может необходим нагрев? или что то ещё?