
knilol
-
Постов
30 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные knilol
-
-
Три раза готовил, но результат всегда тот же, склоняюсь к тому что упаковка бракованная
-
На титрование уходит в 2 раза больше трилона Б чем обычно, для приготовления раствора использовался фиксонал, фиксонал из одной упаковки, не просрочен, титруемый раствор тот же самый
-
Какой из разбавителей лучше подойдёт для антикоррозионного покрытия?
Триглицидиловый эфир полиоксипропилентриола
О-крезил глицидиловый эфир
Диглицидиловый эфир 1,4 бутандиола
Диглицидиловый эфир 1,6 гександиола
Триглицидиловый эфир триметилпропана
2,3 эпоксипропил неодеканоат
Смолы: DER 351, DER 352
-
нужен какой-нибудь практикум для проведения гидрогалогенирования
-
Да тут надо в несколько стадий отщепить сн3 и прицепить в другое положение
-
из 4-метилпиридина получить 2-метилпиридин
-
-
-
Нужно приготовить насыщенный раствор йодида калия в спирте (этиловом)
-
. "Так природа захотела... Почему? - Не наше дело.
. Для чего? - Не нам судить..."
. (Б.Ш. Окуджава)
. Азот в степени окисления +3, содержащийся в нитрит-ионе, окисляет азот в с.о. -3 из катиона аммония. Т.о. происходит внутримолекулярная конмутация (окислительно-восстановительный процесс), где и окисленной формой восстановителя, и восстановленной формой окислителя является элементный азот. А как бы Вы хотели иначе "провернуть" эту реакцию, даже интересно?!
. Вторая реакция протекает аналогично, только вместо молекулярного азота образуется его закись.
. С уважением
в этом и заключается главный вопрос, почему реакция идет именно так? почему она больше не может идти никак иначе? NH4NO3 может разлагаться при разных температурах по разному, а NH4NO2 только так, почему?
-
NH4NO2 -> N2 + H2O , почему реакция идет так, а не как иначе? и как тогда пойдет реакция NH4NO3 ->
-
Это что, по отношению к чему-то конкретному? Или вообще, т.е. переписать сюда учебник.
прошу прощения забыл картинку прикрепить
-
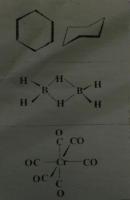
Определить все элементы симметрии, установить точечные группы, определить полярность и хиральность.
-
напишите уравнения реакции 1,4-дибромпентана, 1,2 дибромпентана, 1,3 дибромпропана, п-дибромбензола, м-,бромбензилбромида с магнием
-
Лучше наоборот
Не лучше
Восстановление кислоты с помощью LiAlH4 до этанола, затем превращение в бромэтан и, наконец, реакция Вюрца с образованием бутана.
Спасибо
-
CH3COOH->C4H10
-
4HAuCl4 + 12H2O2 + 16KOH = 4Au + 16KCl + 22H2O + 9O2
Во.
спасибо, у меня почему-то неполучалось уравнять
-
Н [АuCl4] + Н2О2 + КОН =
-
Ну вот, теперь можно решать.
Алгебраический метод. Пусть октагидрата взяли х моль
По уравнению реакции (которое так и осталось недописанным) видно, что при этом прореагирует х моль кислоты и образуется х моль сульфата бария.
Найдем массы этих веществ по формуле m=M*n:
m(к-ты) = 98 х, m(окт) = 315 х, m(BaSO4) = 233 х,
Найдем массу полученного раствора: m(p2)= m(p1) + m(окт) - m(BaSO4) = 130+315х-233х
Поскольку полученный раствор должен быть 10%-ным, то в нем должно остаться кислоты: (130+315х-233х)*0,1
Но с другой стороны кислоты было 52 г, а израсходовано 98х, значит осталось 52-98х
Приравниваем два эти выражения:
52-98х = (130+315х-233х)*0,1 - получаем уравнение с одним неизвестным,
находим х, m(окт) = 315х,
и радуемся, что задача решена.
уххуху, спасибо огромное, (Ba(OH)2*8H20+H2SO4=BaSO4+10H2O вроде так), я вас сперва не понял
-
Что надо делать я тебе подсказываю.
Но ты видимо не хочешь сам ударить пальцем о палец, и хочешь чтоб кто-то за тебя щелкал кнопками калькулятора.
Если так - то это не я.
о господи да пожалуйста m(H2SO4)=52г, M(кристаллогидрата)=315, M(H2SO4)=98,M(BaSO4)=233, m(р-ра) H2SO4= 130г, это всё я и без ваших подсказок знаю
-
Пока я не вижу, что ты рассчитал, я не могу развеять твои сомнения.
издеваетесь чтоль? я прошу вас решить если вы на все 100% уверены, что знаете как это решать,у меня еще большая куча однотипных задач, вы можете дать на 100% правильное решение с ответом, чтобы я смог понять механизм решения?
-
И что помешало дописать? получится сульфат бария (в осадок) и вода.
Теперь надо рассчитать массу 100мл раствора серной кислоты, используя плотность 1,30г∙см-3
и найти сколько там самой кислоты, раз уж этот раствор 40%-ный
И надо посчитать молярные массы октагидрата, серной кислоты, и сульфата бария - пригодятся
все,что вы написал,я уже знал,можно увидеть решение и ответ? я сегодня видел несколько разных решений и несколько разных ответов и сомнения меня уже замучили
-
Но формулу то гидроксида бария можете написать?
Ba(OH)2*8H20+H2SO4=
-
пишите формулу октагидрата и уравнение реакции
это всё что есть


сернокислое цинкование ленты
в Электрохимия
Опубликовано
Подскажите пожалуйста, из-за чего гребенки могут забиваться цинком? Большую часть времени все идет нормально, но время от времени цинк начинает сдираться на гребенках