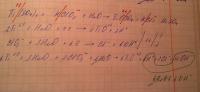-
Постов
25 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент thaisofathens
-
Добрый день. Готовилась к ЕГЭ и заметила, что ОВР 8KI + 9H2SO4 → 8KHSO4 + 4I2 + H2S + 4H2O пишут исключительно с кислой солью. Но может ведь образоваться средняя, если будет достаточно иодида, так? Или я не учитываю какую-то взаимосвязь между тем, какой образуется продукт восстановления серы, и какая получается соль - кислая или средняя? Но странность в том, что ОВР CuI2 + 2H2SO4 → CuSO4 + I2 + SO2 + 2H2O никогда не пишут с кислой солью. Хотя казалось бы, они очень похожи. Собственно, вопрос: то, какая соль получается, зависит чисто от удобства расстановки коэффициентов в условиях получения разных продуктов восстановления окислителей? Или есть какая-то еще причина на получение в первом случае кислой соли, а во втором - средней?
-
Как понять, что получится, хромат или дихромат? CrO3 + 2NaOH → Na2CrO4 + H2O Rb2CO3 + 2CrO3 → Rb2Cr2O7 + CO2 Почему в одном случае так, в другом иначе? Степень окисления одна, как выбрать непонятно. То есть если бы мне дали реакции, я бы в обоих случаях хромат написала. Есть какой-то критерий, по которому можно понять, что получится?
-
Здравствуйте. Помогите пожалуйста решить задачи. Попались на контрольной - не смогла решить. 1. Водный раствор насыщен при 22 С карбонатом бария (ПР = 4.65 . 10-9) и карбонатом кальция (ПР = 1.2 . 10-8). Рассчитайте равновесные концентрации ионов в растворе. Как я пыталась решить: записала ПР, считая, что концентрации карбонат-ионов равны. 4.65 . 10-9 = С(Ba 2+)*C(СО3 2-) 1.2 . 10-8 = С(Сa 2+)*C(СО3 2-) И дальше тупик. Три неизвестных в системе из двух уравнений. Понимаю, что должно быть что-то еще, чего я не учла, но что - уже второй день не доходит. 2. Рассчитайте ЭДС гальванического элемента Pt, H2 | 0.02 M HN3 || 0.5 M NH2OH | H2, Pt если Ka (HN3) = 2.6 . 10-5, Кв (NH2OH) = 9.33 . 10-9, Кw = 1 . 10-14, стандартный электродный потенциал реакции Н2 - 2 е- = 2Н+ Ео = 0 В. Как я не то чтобы пыталась решить, скорее ничего не понимала: Судя по опыту решения задач на практических занятиях, надо было записать полуреакции на аноде и катоде, и для анода и катода уравнения Нернста. Только вот рекация то там везде одна, с водородом? То есть ЭДС, которая есть разность потенциалов на катоде и аноде получается равной нулю. Не может быть так все просто, следовательно, я в корне неверно рассуждаю, а как верно - непонятно. 3. Рассчитайте рН раствора, в 5 л которого содержится 20 г хлорида аммония, если Кв = 1.8 . 10-5, Кw = 1 . 10-14 Как решать - вообще непонятно, откуда брать ионы H+ или ОН- непонятно... 4. Составьте кинетическое уравнение реакции образования фосгена CO (г) + Cl2 (г) = COCl2 (г), если уменьшение парциального давления СО в 3 раза приводит к уменьшению скорости реакций в 3 раза, а увеличение парциального давления Cl2 в 4 раза приводит к ускорению реакции в 8 раз. Рассчитайте общий порядок реакции. Как я поняла, кинетическое уравнение выглядит так: u=k*C(CO)*C(Cl2), и смысл в том, чтобы найти коэффициент. Искать его надо из уравнения Аррениуса. А как, если в нем есть некий предэкспоненциальный множитель, которого я не знаю?
-
к сожалению, не МГУ, а глухой ННГУ, и в нашем деканата о помощи студентам не слышали. Кроме того, на каком курсе вы пошли в ИОХ? То есть если я в местное НИИ Химии заявлюсь, вряд ли они мне обрадуются - первый курс, ничего не умею, и кто за меня ответственность нести будет, если кого-то серной кислотой окачу?
-
Простите, что не совсем в тему, но как мне кажется, это наиболее терпимый к не очень умным людям раздел форума. Учусь на первом курсе химфака, пока не научили ничему полезному, и, кажется, не собираются. Дают чисто знания по теории, которые нужны для кругозора и для того, чтобы блеснуть при редком удобном случае. Недавно услышала как два однокурсника обсуждали какой-то синтез, что получили они примесь какую-то, как же ее отделить от нужного вещества. А я максимально близко к практике бываю когда прихожу на лабы, и все, что я делаю ограничивается строгим следованием инструкции и прямо скажем, ничему кроме отмывания пробирок не учит. В общем, вопрос: есть ли вероятность, что студентку первого курса возьмут куда-то на работу, где я смогу получить практические знания по химии, которые мне пригодятся. Естественно, зарплата тут роли не играет, смысл в том, какие слова вбить в гугл, чтобы найти нужную вакансию, пусть и неоплачиваемую? Как это должно называться? "лаборант", или как-то еще? Где искать?
-
Есть ли какая-то принципиальная разница между гидридами лития и натрия? Ищу информацию - вроде бы и свойства похожи, и строение одинаковое, и получение.
-
спасибо. А в каком виде выделится йод?
-
в первой реакции очевидно будут сульфаты натрия и калия, вода и йод, но вот что будет с бором не знаю, и информация найти не могу. Может, B2O3 получится, а может сам бор, а может и очередное соединение натрия с бором, хотя я склоняюсь к первому варианту. со второй сложнее, тут уже ни в чем не уверена. Думаю, будет вода, хлорид натрия и Na2CrO4, но вообще в том, куда пойдет хром не очень уверена, как и в том, что будет с бором
-
помогите пожалуйста написать продукты реакций: 1. Na2[b2(O2)2(OH)4] + H2SO4 + KI 2. Na2[b2(O2)2(OH)4] + CrCl3 + NaOH
-
Из знаний элементарной химии я могу сказать, что раствор покраснеет, этого недостаточно. Например, когда я в ацетат натрия капнула фенолфталеин, то сначала он остался сверху в виде белой нерастворимой фазы, при нагревании же смешался с ацетатом и покраснел. Именно об этом я и спрашиваю. Согласно тем же элементарным знаниям, метиловый красный плохо растворим в воде, значит, возможно, должен вести себя так же, как фенолфталеин в вышеописанной ситуации, но быть может, он поведёт себя иначе, например, напротив потеряет окраску при нагревании. Эту информацию искать очень долго, потому я и спрашиваю, и такой ответ мне нужен, а не то что в кислой среде индикатор станет красным
-
В лабораторной работе есть задание добавить к раствору сульфат цинка метиловый красный и нагреть. К сожалению, сделать работу нет возможности, а отчет писать надо. Подскажите пожалуйста, что будет при добавлении и какие изменения произойдут при нагревании.
-
-
Помогите пожалуйста написать продукты реакции. Сама реакция на фото. Искала в интернете, нашла только в нейтральной среде. Во-первых, не пойму, что получается из S2O8. Пробовала SO4, но когда начинаю уравнивать, в балансе получается, что кислородов одинаково, и никуда не припишешь ни H ни OH. Значит, получится SO2? Во-вторых, не знаю, что получится из Na и K. Если взять для обоих металлов сульфаты, не уравнивается ничего.
-
Помогите пожалуйста. Начала делать цепочку. Что в первой реакции получается понятно. А вот дальше... С чем из H2O, NO2 и Cu(NO3)2 будет реагировать NO?
-
Здравствуйте) Недавно поняла, что для расширения кругозора и будущих возможностей стажировки или работы за границей надо учить английский. В общем и целом проблем с ним нет, уровень В2, но очевидно, что для занятий химией мне нужно будет знание специальной терминологии. Закапываться в словари очень уж не хочется, и просто зубрить слова - тоже. Поэтому хочу почитать какие-нибудь статьи или журналы по химии на английском. Посоветуйте пожалуйста что-нибудь не очень сложное (ясно, что я не пойму людей, всю жизнь занимающихся узкой областью химии, и пишущих статьи на волнующие их темы, даже школы не окончив, да еще и не на своем языке), и если можно - не русских ученых. Потому что переводить на русский то, что написали на английском русские ученые намного проще, а мне все же важно подтянуть язык.
-
Определила, если делать с (+3) то 17 электронов, и в итоге количество h не равно количеству no3, так что не понятно какой коэффициент к кислоте ставить. А если делать с (+2), то все получается, хотя и пришлось кислоту дополнительно умножить
-
Спасибо огромное, все уровнялось))) Только не могли бы вы объяснить, почему вы сказали, что у Fe(+3)? И еще мне пришлось поменять коэффициент перед кислотой, потому что количества N,O и Н было справа больше на 1,75. аа, понятно У меня в итоге K2SO4 остался без коэффициента, поэтом ничего не уравнивается. Простите если я уже достала, но не понимаю, как это делать)
-
А почему у железа(+3) в Fe(NO3)2, если у (NO3) (-1), и их две, то есть (-2)?
-
Спасибо большое, а как разделить на ионы CuFeS2? И в правой части потом писать Cu(NO3)2 или Fe(NO3)2?
-
1. Вроде бы делала как учительница сказала, если среда нейтральная, то слева везде h2o, а справа - там где есть кислород, приписать oh, где нет кислорода, приписать h.Только в итоге у меня справа осталась oh, и куда ее девать не знаю. 2. Не понимаю в чем проблема. Все уравнялось кроме азота и кислорода. 3. С хромом все получилось, а что писать в правой части с NCS не знаю. Думала, может, приписать туда SO2, co2, no2. Попробовала, не получилось. Значит, неправильно. Что там писать? 4. Не знаю, какие ионы в CuFeS, поэтому и вторую реакцию не могу написать. А первая - не уравнивается.
-
слева получилось 12 N, а справа - 14 и так же с кислородом - слева 38, справа - 40. В чем проблема не пойму( TiOSO4 не пойму как разделить, вроде бы TiO/SO4, чтобы SO4 было отдельно, но как-то странно это, чтобы металл был с кислородом. А в д, там как то непонятно, слева пишу NCS, а справа что? В е не пойму как быть с CuFeS2, и еще что из азота получится, там же три вещества его в правой части содержат. В общем не сильна я в химии. Объясните пожалуйста как там делать)
-
Помогите пожалуйста уровнять методом полуреакций. Первые два я вроде бы сделала, но коэффициенты не подходят, а в чем ошибка понять не могу. А последние даже как делить на ионы не понятно(
-
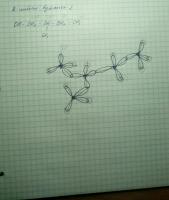
Я рисовала изображение 2-метилбутанола-1 в пространстве - с гибридизацией, и поняла, что не знаю, как пририсовать кислород. Помогите пожалуйста, как он там выглядит?
- 1 ответ
-
- гибридизация
- кислород
-
(и ещё 1 )
C тегом: