
Wannecca
-
Постов
25 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Wannecca
-
-
А учебник не пробовал открывать по пропущенному уроку?
Хотя бы здесь http://orgchem.ru/chem2/index2.htm
В учебнике для 10 класса, только химические и физические свойства (каучук, бензол, нефть). Там не написано про превращения ни слова!
Помогите хоть с первым звеном.
-
. А собственные соображения?!
. С уважением
C2H5Br + ? = C2H4 + ? - Это лишь первый шаг. А какое надо соединение добавить, чтобы получить C2H4 я не знаю. Помогите
Помогите!!!
-
Здравствуйте, помогите с цепочкой превращений. Я заболел и урок пропустил я не знаю как это делают вообще.
Осуществить превращения. Указать условия проведения реакций: C2H5Br → C2H4 →C2H2→C6H6 → CH3-COH
Благодарю
-
Тот подсажет. Нужно начинать с водородного ансамбля. Метан – 4 водорода - 4 атомные обитали – 4 обитали ансамбля: ++++, ++--, 00+-; +-00 – три последние вырождены. Ансамбль возбуждает, обитали углерода, и возбуждается сам. s, px, py, pz соответственно. Для этана тоже самое, но в ансамбле только три водорода. Так получите орбитали метельного радикала и спаривайте их.
Что? У нас в учебнике такого нет. Какие ансамбли? Какой метельный радикал?
Думаю, под этим понимается следующее:
а - структурная, б - электронная формула метана
"Электронная формула показывает, что атом углерода в молекуле метана имеет устойчивую восьмиэлектронную внешнюю оболочку (электронный октет), а атомы водорода — устойчивую двухэлектронную оболочку (электронный дублет)."
Вы оказались правы!
А почему именно 2 точки стоит около углерода?
-
Думаю, под этим понимается следующее:

а - структурная, б - электронная формула метана
"Электронная формула показывает, что атом углерода в молекуле метана имеет устойчивую восьмиэлектронную внешнюю оболочку (электронный октет), а атомы водорода — устойчивую двухэлектронную оболочку (электронный дублет)."
Думаю, под этим понимается следующее:

а - структурная, б - электронная формула метана
"Электронная формула показывает, что атом углерода в молекуле метана имеет устойчивую восьмиэлектронную внешнюю оболочку (электронный октет), а атомы водорода — устойчивую двухэлектронную оболочку (электронный дублет)."
Не думаю... Мне кажется электронную формулу по орбиталям.
-
Степень окисления - формальная величина, определяемая соотношением электроотрицательности элементов, образующих связь. Естественно, что в молекулах О2, F2 и т.п. она равна нулю. Так же, как у отдельных свободных атомов
А в O3, О4, О5 - тоже ноль?
-
-
Здравствуйте, подвис на простом. Вот смотрите, у кислорода степень окисления -2. Вопрос: а в отдельной молекуле кислорода (О) какая степень окисления? 0? -2?
У фтора -1, а в отдельной молекуле?
Я не понимаю в соединениях всегда степень окисления -2 (у кислорода) или даже в отдельной молекуле?
Или именно в соединениях?
-
Не всегда. По таблице можно определить максимальную степень окисления и минимальную
У азота V группа, степени окисления макс: +5 и мин: -3
Но у него есть и другие степени окисления
И сколько электронов он будет принимать/отдавать зависит от конкретных веществ: исходных и продуктов.
Например: НNO3 => NO2
Это так: N+5 + 1e => N+4
Но если NH3 => N2
То по другому: N-3 - 3e => N0
Короче: для определения числа отданных/принятых электронов надо уметь определять степень окисления атомов в соединениях.
Я умею определять степени окисления в соединениях. Понял!
Надо после знака равно определить степени окисления элементов и написать сколько передалось электронов из первой части.
-
Периодическая система вам в помощь. Повторите тему Строение атома и периодический закон
Можно по учебнику 8 класса. Или здесь: http://www.hemi.nsu.ru/ucheb142.htm
Значит можно определить по таблице число электронов для передачи?
-
Вы меня уж простите великодушно, но, судя по всему, Вы, как минимум, классе в 10-м. Соответственно, не знать, что такое электрон хотя бы на примитивном уровне, не вдаваясь в тонкости квантово-волнового дуализма и "дебри" квантовой механики, это, извините, моветон.
Ещё один немаловажный, на мой взгляд, аспект... Если учитель "плавает" в подобных вопросах, что лично мне весьма сомнительно, т.к. подобные вещи должен знать не только специалист, но и всякий мало-мальски образованный человек, то Вам (Вашим родителям) прямая дорога к администрации школы с постановкой вопроса о профпригодности данного педагога (учтите, что все факты непрофессионализма нужно будет предметно доказать). Но, повторюсь, моё мнение таково, что Вы, уважаемый Waneссa, пытаетесь прикрыть свои, что называется, "косяки" (может быть, просто пробелы в знаниях) бестолковостью и безразличием учителя, что, согласитесь, и не совсем честно, и не совсем по-взрослому.
В конце концов, даже, если допустить, что в Вашей школе один и то "несознательный" учитель химии, почему Вы к преподавателю физики не обратились за помощью и разъяснениями?! Уж он-то (или она) точно должен быть в курсе, что такое элементарные частицы и "с чем их едят", да и с электронным балансом, я уверен, помог бы. Не боги, как говорится, горшки обжигают...
С уважением.
Я не говорил, что она "несознательная". Просто я ее побаиваюсь, я боюсь ее спрашивать, она как посмотрит... ужас.
Так что я пока тут поспрашиваю. Это у меня пробелы большие (я это знаю и признаю) и я их сейчас заполняю
Будет так: 2Na - 2e = 2Na+1
Было два атома натрия, каждый отдал по 1е (действительно зависит от того сколько электронов на энергетическом уровне, только не на первом, а на внешнем, у натрия это третий уровень)
- и получилось 2 атома натрия, но уже в степени окисления +1
Значит надо определить валентность элемента и это будет числом передачи электронов?
P.S. Я откуда знаю сколько электронов на энергетическом уровне у натрия?
-
Значит количество электронов зависит от валентности? Мне сказали, что от энергетического уровня (сколько на первом уровне, столько и передаётся электронами).
2Na + S значит будет 2Na - 2e- = Na+2 (степень окисления).
-
Помогите с этим. Я не понимаю почему 4е-, почему именно 4? Что такое е?
Помогите! Училка от этого вопроса отныривает.
-
-
Эти числа обозначают число атомов водорода присоединенных к данному атому углерода. Когда индекса нет, значит индекс равен единице. Валентность углерода 4, водорода 1, если соеденились углероды по одной связи, то они использовали 1 свою валентность, осталось 3, а если по двойной или тройной, то 2 и 1 соответственно.
По этому формула этана H3C-CH3, этилена H2C=CH2, ацетилена HC≡CH
А как понять по какой связи соединились углероды?
И еще, почему СН3 нельзя прикрепить к СН2 последнему (под 4 цифрой)?
Эти числа обозначают число атомов водорода присоединенных к данному атому углерода. Когда индекса нет, значит индекс равен единице. Валентность углерода 4, водорода 1, если соеденились углероды по одной связи, то они использовали 1 свою валентность, осталось 3, а если по двойной или тройной, то 2 и 1 соответственно.
По этому формула этана H3C-CH3, этилена H2C=CH2, ацетилена HC≡CH
По палочкам посчитать (связям)? Только что придумал
Если около соединения 2 палки (связи), то будет СН2 (4-2=2)! Правильно ли я думаю?
-
Почему у СН сначала идет индекс у водорода 3, а потом 2, где-то вообще нет индекса у водорода? Почему? До меня не доходит, что-то с валентностью связано. Благодарю за помощь. Фото прикрепил.

Я просто на уроке не понял. (Цитирую химичку: "Раз, два, три пишем три. Раз, два пишем два индекса, вот и всё").
-
А я по валентности элементов определеляю. Потом валентности перемножаю.Ну если упрощённо то давайте я буду говорить образно:
В общем все атомы имеют степень окисления равную 0 то есть в них присутствует равное количество протонов р+ и электронов е-), но взаимодействуя друг с другом они могут менять свою степень окисления отдавая или принимая электроны. Так вот металлы имеют тенденцию к отдаче электронов (восстановители) а неметаллы наоборот принимают электроны (окислители). В вашем случае металл это натрий Na а неметалл сера S. Так вот чтобы вам было понятнее все атомы химических элементов стремятся приобрести наиболее устойчивую конфигурацию из 8 электронов на внешнем энергетическом уровне. Давай те посмотрим по таблице сколько электронов у натрия на внешнем энергетическом уровне? Верно 1. А у серы? Верно 6. Так сколько электронов нужно сере забрать у натрия для того чтобы у неё их стало 8? Конечно же 2. И соответственно натрий как и положено порядочному металлу (восстановитель) отдал свой электрон неметаллу (окислитель) сере. Но сере нужно 2 электрона а у одного атома натрия только 1 электрон на внешнем электронном слое ну тут подключается второй атом натрия и тоже отдаёт свой электрон. Соответственно сера "отжала" 2 электрона у 2 атомов натрия образовав с ними ковалентную полярную связь. Na2S. В итоге все довольны у натрия 8 электронов на внешнем энергетическом уровне и у серы тоже 8 электронов на внешнем электронном слое.
Это я так в довольно вольном изложении всё написал. Почитайте лучше учебник.
-
Да азов я не знаю на это есть причины.Если нормально, это придется главу из учебника сюда переписать. Я дал ссылку на СО.
Такое впечатление, что вы совершенно не знаете азов.
-
Не понял. Вы бы не могли нормально обяснить. Причем здесь степени окисления натрия и серы? Как написать электронный баланс?Подумайте о степенях окисления натрия и серы в Na2S и то, что они до этого имели степень окисления 0
Электронный баланс напишите.
А как определить степени окисления натрия и серы?
-
Не надо фоток, просто напишите.
Там без фотки не понятно. Вот от 2Na идет стрелка к S, сверху этой стрелки написано 2е-. 1)Что означает 2е- ? 2) Почему именно 2е- ? 3) Откуда 2е- берется?
2Na + S И стрелка от натрия к сере.
Откуда 2е- берется?
-
Нет это я знал. 2е- = 2 электрона, 4е- = 4 электрона. Я фотку скину, как с компа буду. Там вот просто я не понимаю откуда!И вы только сейчас это заметили
2e- означает 2 электрона
-
А где фото?
Сорри просто нокиа аша не грузит.
-
это степень окисления, почитайте учебник для начала
Хорошо. С 0 разобрались.
Что означает 2e- на фото?
И почему именно 2е-? А не 4е- например.
-
Здравствуйте всем! По химии у меня не очень, так-что вопросов будет много.
Вот уравнение реакции: 2Na + S --> Na2S. В книге над Na и S стоит 0 что это означает?

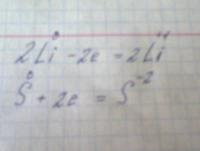
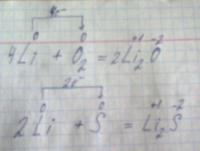


Электроны на энергетических уровнях
в Учеба
Опубликовано · Изменено пользователем Wannecca
Добавил благодарность.
Здравствуйте, химический элемент Te имеет пять энергетических уровней. Вопрос: почему на четвертом уровне у этого элемента имеется всего 18 электронов, а не 32 (по формуле N=2n^2)? Второй вопрос: почему энергетические уровни не заполняются полностью? Спасибо.