-
Постов
608 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Весь контент Loiso Pondohva
-
Да, понял. Сейчас проверил, как во всякой школьной литературе пишут как раз. Любопытно, что там вбрасывается здравое зерно, что если вода, как кислота сильнее спирта, то и Na будет сначала реагировать со всем избытком воды и только потом с этанолом(упрощённо). Но не рассматривается эта цепочка дальше(и обратимость так-то). Для абсолютирования это дело и правда не годится.
-
Хм вот тут они его продают вроде и аналоги. https://www.trc-canada.com/product-detail/?CatNum=O239940; https://www.trc-canada.com/product-detail/?CatNum=O239945 ; И у них есть References. Проблема в том, что или референсы кривые, или я просто с телефона, поэтому ничего толкового из представленных не находится.
-
А, всё, я сначала просто не понял формулировки. Извините, облажался.
-
Кстати, а почему? Ни разу не приходилось руками делать(или уже абсолютный был, или сушки до медицинского/или собственно имеющегося в наличии было достаточно), но вроде запомнилось, что такая очень мейнстримная, чуть ли не среднешкольская штука. Лош пиз*ёш и провокация?)
-
Кстати да, как гласят PubChem и PubMed вся органика - это ирритант и почти вся не органика с исключением изотонического р-ра водички хД А если серьёзно, то многие соединения правда действуют на слизистые не очень, просто у кого-то это выражено больше, у кого-то меньше. По опыту работы с более "безопасными" (хах, оксюморон) фторидами, пыль фторида калия в принципе может слегка жечь, хотя не выражено, на вкус резко солёная, фторид цинка вызывает прям выраженное чихание и острое неприятие слизистыми. Так что отрицать нельзя. Но и не бромацетон точно. (Если что, всё обошлось без отравлений, просто мелкодисперсная пыль в ненадлежащей упаковке имеет свойство очень легко разлетаться).
-
Пока не уверен, но если что. Куда готовы пересылать, и откуда (чтобы по цене можно было посчитать).
-
Гемолиз и прочая, ага. Это из острых последствий. Головная боль, тошнота, утомление. Ну и как следствие анемия, гемолизная желтуха, печень-почки и прочее, если доживёте. Это из острых и очень опасных последствий. Из хронических - могут быть опасны твёрдые продукты окисления кислородом воздуха, забивающие альвеолы. Штука очень неприятная. Благо, запах очень характерный и противный, отравиться случайно не почувствовав - сложно.
-
Надеюсь не оффтоп. В общем, если адрес у вас сохранился и найти правда хочется/требуется можете чекнуть прошлые состояния "снесённой" страницы тут http://web.archive.org/ . Хороший инструмент для доступа к закрытым и изменившимся сайтам, иногда выручает, один минус - количество сохранённых состояний страниц зависит от рандома (бот же сохраняет) и популярности страницы (логично). Вот.
-
Если есть ссылка-можно попробовать восстановить через веб-архив... (Или мне кидайте и я гляну, или я просто кину ссылку на сервис).
-
На первой стадии первичный амин превращается во вторичный с выделением HCl. То есть по сути происходит алкилирование. Дальше в нейтральной среде получалась бы аммониевая соль, но щёлочь забирает выделившийся HCl на себя. Будет у вас N-пропилпропан-1-амин. Проблема в том, что эти реакции на самом деле весьма противные и сложноконтролируемые, поэтому на выходе будет смесь вторичного, третичного амина, алкиламмониевой соли (в зависимости от избытка-недостатка реактивов).
-
Осаждает? Лоури? Вы наверное хотели сказать обнаруживает? Поскольку оба пигмента имеют белковую составляющую, то совершенно точно реакция будет идти и обнаруживать белок. Посчитать концентрацию пигмента можно будет с помощью колориметра на 660нм (ну или на глаз, если вы хотите просто обнаружить качественно). Проблем может быть 3: а) Препарат недостаточно очищен от примесей, поэтому реактив будет реагировать не только на пигмент, но и на другие белки в р-ре. б)Небелковая составляющая пигментов имеет восстановительные свойства и будет также реагировать с реактивом (маловероятно, но возможно). в)Сами пигменты имеют линию на 660нм и тогда будут проблемы с измерениями. Но это вряд ли, хотя у фикоцианина лучше проверить, я что-то помню у него линию на 650нм.
-
Здравствуйте. Такой вопрос. Представим, что мы хотим получить полутяжёлый водород или полутяжёлую воду высокой чистоты из чистого дейтерия, не прибегая к физическим методам разделения. Допустим, у нас есть дейтерий. Мы делаем из него гидрид (дейтерид) лития, LiD (нет, не для бомб). После чего, производим реакцию гидролиза. Исходя из механизма, получается что: LiD + H-OH = LiOH + H-D ? Будет ли полученный полутяжёлый водород достаточно чистым? И будет ли при его дальнейшем сжигании в кислороде получаться полутяжёлая вода? /Да, я знаю об изотопных метках для определений механизмов реакций и превращений веществ, и что это всё прекрасно работает. Скорее интересен данный частный случай. Насколько это соотношение будет правда постоянным? Есть сомнения по поводу горения, механизм всё-таки цепной радикальный...
-
Из дешево-сердито можно использовать безводный CuSO4 (стоит копейки, если купить кристаллогидрат - достаточно прожечь хорошо и получить безводный). Регенерируется довольно просто, воды вбирает достаточно, до 94-96% довести точно можно, если постараться. Там спирт будет очень охотно сосать влагу из воздуха, не уверен получится ли довести до 99%. Там скорее надо уже использовать щелочные металлы, которые будут реагировать сначала с остатками воды, и сразу закрывать это дело плотно (обкладывая силикагелем в эксикаторе, хах).
-
Соглашусь с комментатором выше. Если не быть дураком, работать можно. Но стоит заметить несколько важных вещей. Оба нитрата - соединения ртути растворимые в воде, поэтому очень токсичнее (НАМНОГО токсичнее чистой ртути или её нерастворимых солей). Нитрат (I) восстановитель, который ещё и с охотой разлагается. Нитрат (II) сильный окислитель. Так что действительно нужны все меры предосторожности, включая вытяжной шкаф и проч. Также ртуть кумулятивный яд, то есть имеет свойство накапливаться в организме. Так что стоит избегать попадания даже небольших доз, если не хотите стать "As mad as Hatter". А с другой стороны это не органортуть, которая даже через перчатки может "сделать вас героем".
- 2 ответа
-
- 1
-

-
Ну если владеете английским, то довольно много информации по токсичности на ПабХеме https://pubchem.ncbi.nlm.nih.gov/compound/Octreotide#section=Biologic-Description LD50 есть здесь https://www.medsafe.govt.nz/Profs/Datasheet/d/dblOctreotideinj.pdf (фото) ИМХО, могу сказать, что примесь нежелательная (как вообще этот пептид может быть примесью где-то?), с достаточно сильной биологической активностью, но в целом (для пептида) не очень высокой токсичностью. ___________ Кстати, это вроде нигде не написано, но по-моему вполне очевидно, что нигде особо не описано его биологическое действие или токсичность при пероральном приёме, в силу того, что это пептид и в желудке/кишечнике большая его часть распадается на аминокислоты. Так что в таком виде он точно не опасен.
-
Сама реакция - внутримолекулярная дегидратация спирта (ну точнее гидроксокарбоновой кислоты). Температура - 180°C, уходит вода. Катализатор - H2SO4 (иногда другие водоотнимающие агенты). В реальности на самом деле побочными продуктами могут быть всякие сложные эфиры, но реакция имеет право жить. C3H6O3 -> C3H4O2 + H2O
-
Да, благодарю. Конечно, если делать не в одну стадию, то оно очень даже можно. Гриньяр, пожалуй, самый приятный душе и презентабельный вариант из лабораторных (промышленный конечно выгоднее будет галогенирование и H2, Pt, T ). Комментарий про 100->2 грамма позабавил, потому что чистая правда, хах)
-
В водном р-ре кетоспирт и NaBr, да. В спиртовом же будет алкен с кумулированными двойными связями.
-
Я не уверен, скорее всего сильно зависит от условий проведения реакции. На свету будет получаться смесь продуктов, но вероятнее раскрытие поочерёдно циклов с такими вот производными в финале (картинка). Дальнейшее бромирование никто не отменял, оно уже преимущественно пойдёт по 3 и 5 атомам, т.к они вторичные и уже замещённые). Не понятно возможна ли реакция с катализом кислотами Льюиса. По идее электрофильное замещение характерно больше для аренов... ___ UPD я ошибся с зарядами на ночь глядя и бред написал сначала. Поправил.
- 3 ответа
-
- 1
-

-
Здравствуйте. Насколько вообще возможно восстановить фенол до бензола или нафтол до нафталина? Понятно, что на бумаге-это довольно просто, но интересна скорее практическая сторона вопроса. Получатся ли хоть какие-то ощутимые выходы без использования сверхсильных восстановителей по типу алюмогидрида лития, диборана и подобных? Нашёл достаточно старые литературные данные о перегонке фенола с цинковой пылью, но если честно, не особенно верится в это.
-
А не будут гидроксилазы дальше добавлять OH- группу в ароматическое кольцо с превращением в дофамин? Или катехол-О-метилтрансфераза вводить метильную группу, как с биогенными аминами обычно бывает? По-моему также возможные пути в данном случае. ___ UPD 1:50. Извиняюсь, стоило посмотреть сразу в литературу. Да, это всё возможные пути метаболизма через цитохромы и прочие, метилирование дальнейшее туда же. Но само "обезвреживание" за счёт МАОа и МАОб, и это, собственно, преимущественный путь.
-
Здравствуйте. Внезапно, не по рабочим нуждам, а скорее из любопытства назрел вопрос. Достаточно известный факт, что Mg в кислороде горит очень-очень ярко :3 Чуть менее известный, но тоже довольно книжный факт, что при горении он также неплохо так светит ближним UV диапазоном. Вопрос такой "а почему? Каков механизм данного явления? Какие ещё аналогичные примеры существуют и почему так ярко?". Лично я сначала подумал, что дело банально в высокой температуре горения и спектре излучения чёрного тела. Ну вот высокая температура, быстрое окисление и разогрев, вот и светит. А поскольку температура правда большая, то ощутимая часть излучения заезжает в ультрафиолет. Но тогда это явление должно быть не исключительным и не уникальным? И при горении какого-нибудь C4N2 с температурой горения в 5013 °C это явление должно быть ещё более выраженным и заметным. Тогда вопрос, почему обычно в таком контексте пишется про магний? Или это связано как-то с его спецификой, электронными переходами или чем-то ещё? /Заранее простите, если вопрос покажется глупым. В данной области я недостаточно компетентен.

(1).png.e123e264b2c43ab342e27956649d5627.png)
(2).png.4cdffead22ffecef8bb8e49a51cab3fb.png)
(3).png.b2e06a2f32f52e2b208a43fb7ddad75b.png)

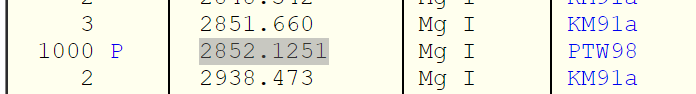

.png.0374e303e2b27fec0f4fbfd726cf6f2b.png)