Angry_Biotechnologist
Пользователи-
Постов
285 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Angry_Biotechnologist
-
Добрый день Подскажите параметры фильтрации? Размер пор, какой процес (постоянный/непостоянный), что собствено вы фильтруете (продукт)? Пока что ясно что проблема в явлении которое за бугром называется fouling (см фотку) - поры фильтра закрываются слоем материала. Решается в зависимости от вида процеса на производстве. Нп для нутч-фильтра можна дать лопасти для перемешивания. Создание правильной турбулентности будет поднимать фракцию над фильтром. Какие лопасти и какая мощность перемешивания зависит от параметров пульпы и от параметров фильтрационого апарата пэр се. Квалифицированый биотехнолог вам все посчитает и подскажет что будет лучше именно вам.
-
Солей много какой был воопрос такой был и ответ Вариант №1 - очень опасный Сначала приготовте царскую водку (75% + 25%) из чистых реагентов далей маленькими порциями добавляете золото (пропорция золото:к-та 1:5) при необходимости нагрей р-р до 85С (не больше!) нагревай аж все испарится до состояния "сиропа" - это хлорид золота Остудить и получить кристалы. Добавить чучуть воды что-бы растворить хлорид приготовь 30мл амиака в 100мл воды. Добавляй р-р амиака пока кислотность не выйдет 8 Получится осадок - это фульминат золота (гремучее золото). Не дай Бог ему высохнуть - сильное ВВ Осадок надо промыть водой (лучше дистилированой) аж кислотность будет 7 насыщеный р-р цианистого калия МЕДЛЕНО заливаем в промытый осадок и легонько, круговыми движениями посуды перемешиваем. Добавлять пока весь осадок не растворится. Получается маточный раствор Маточный раствор нагревай до 65С - нагревать до тех пор пока не перестанет вонять амиаком под вакумом сушим на 3/4 объема. Останавливаем процес, собираем осадок (остаток маточного р-ра можна еще раз использовать на следущий раствор) осадок досушиваем под вакумом в процесе создаете ВВ - поетому делать на ваш страх и риск. Вариант №2 - просто опасный травим золото в царской водке по надобности греем до 85С не более аж получится маточный раствор В маточный раствор запускаем сильную кислоту - цианистое золото выйдет в осадок. Замешиваем осадок в раствор цианистого калия. Будет много очень токсичных и вонючих паров - на свой страх и риск П.С. если вам надо для золочения, то просто купите уже готовый дицианоаурат. П.П.С. не спешите делать, тут есть химики по опытнее. Вот как Аркадий например вам советует
-
Зависит от того какую соль. Но впринципе золотая стружка + кислота (в маленьких порциях). Вытяжка обязательно. Или же работай на улице, подальше от населения и с маской/противогазом. Вдыхать пары что-то вообще не улыбается. Еще рекомендую дождатся других коментов, может что-то поинтересней предложат
-
Я в Польше закончил биотехнологию бакалавра в УМЦС (Люблин) - могу порекомендовать и универ и направление. Образование там достадочно неплохого уровня + биотех это очень универсальная специальность. Я например не знал что я хочу делать больше - медицину или пищпром, но на магистре уже определился и закончил с упором на тзв белую биотехнологию. Но много моих колег пошли по пути красной биотехнологии - сейчас или при больницах или на универе как pracownik wydziału
-
Азотобактер (и ему подобные) также наращивают биомассу + вязка азота в контексте МО задача достадочно трудоемкая (см изображение). Можно конешно, ензиматическую технологию применить. Тобиш взять соответствующие ферменты и закрепить их на адсорбенте, который помещается в колону. Потом через нее пропускается раствор. На конце должна быть фильтрационая система (ультра фильтрация как минимум) - класический устрой биоректора с постоянным током. Но ИМО бактерии per se будут проще и более "стабильные" (их тяжелее вымыть, они не требуют сильно сложного сервиса и они все таки являются биологическим материалом - едой). Микробная маса как еда вкусом отличатся не будет - это очевидно, поетому сильно выбирать какие МО есть, а какие нет - безсмыслено. Единствено что можна взять во внимание это пищевая ценность, поэтому я дал пример спирулины - https://ru.wikipedia.org/wiki/Arthrospira. Плюс это цианобактерия - дай ей свет, углекислый газ и получиш О2 и еду. Причем, учитывая что света на марсе меньше (в сравнении с землей, солнечная активность слабее), можно вообще использовать искуственое освещение - что душе угодно как говорится
- 795 ответов
-
Интересная тема, производство микробной массы может иметь вполне себе норм кпд. Ставим фотобиореактор, начинаем выращивать какую-небудь спирулину. Для удовлетворения потребностей в азоте можно создать симбиоз с каким небудь азотобактером. Можно еще покрутиться с ген инженерией и создать вариант спирулины который будет производить екзополисахариды. С ними дальше работать химически.
- 795 ответов
-
Это рибоза. А это лактоза. Найди 10 отличий и получи ответ почему рибозу нельзя заменить лактозой.
-
Ензиматическая кинетика (уравнение Михаелиса-Ментен)
Angry_Biotechnologist опубликовал тема в Биохимия
Добрый день! Подскажите каким образом были собраны формулы в разделе 2.5 https://www.sciencedirect.com/science/article/pii/S0008621504004288?via%3Dihub Я понимаю что это все происходит от уравнения Ментен, но как они пришли к такому сложеному формату - увы. Заранее спасибо -
дровами ничего "тугоплавкого" (типа железа) не расплавите в жизни. Для этого нужно совсем другое устройство печи и совсем другое время плавки. Вот вам видосик - посмотрите и заканчивайте на этом. Не жгите дрова попусту
-
я бы попробовал в центрифугу это запихнуть. Авось разделится =D
-
Окей чисто по физиологии - сначало белок переваривается пепсином (неспецифическая гидролаза) на пептиды (фрагменты белка) в желудке (кислотность примерно 1-2). Потом пептиды с желудочным соком проходят в 12палую кишку, куда также попадает желч, которая делает пх на примерно 9. С желчью поступает доза ферментов из поджелудочной (еще неспецифические гидролазы: аминопептидаза, трипсин и еще несколько). Они разбивают пептиды на аминокислотные содержащие которые потом всасываются через стенку кищечника с помощью натриевых каналов на ентероцитах (см фотку). В ентероциты также попадают очень маленькие пептиды (2-5 аминокислотные) которые там же и проходят финальный гидролиз. Из выше сказаного следует что катаболиз белка происходит почти на всем его пути через жкх, от попадания в желудок до его всасывания в кровоток. Это отвечает на ваш воопрос? П.С. если нельзя большинство жиров то надо помнить про достаточное потребление холестерина - он нужен для клеточных мембран.
-
яйцо в утке а в яйце иголка а аминокислоты в белках, готовка пищи повышает доступность (из-за частичного разложение белка на составляющие), но основной грузоподъем - ферменты пептидазы, они выделяются уже в желудке. Как выше было сказано, спортпит делают из молока (я бы даже сказал в основном из отходов молочного производства нп сыворотка). Если можете сказать как называется недуг, то можна будет больше сказать.
-
Стандартный белок в нейральной среде - взаимодействует с водой и в ус не дует (значит растворяется). Добавляем кислоту - в кислой среде, тот базильён груп приобретают новые заряды, что ведет к связям белок-белок (творожение). Тоесть смотрите: Кислотность ниже изоел пункта - белок несет заряд (общий заряд позитивный). Кислотность выше изоел пункта- белок несет заряд (негативный). Как написал Ятчех кристализация с зарядом - очень трудно, а вот кристализация без заряда (читай в из пункте) - очень просто. Думаю при мариновании шашлыка имеет место быть дифузия- концентрированый (относительно мяса) р-р соли и кислоты все-таки.
-
Добрый день, Может у кого-то есть опыт с моделирование ферм. реакций (конкретно синтез олигосахаридов трансглюкозидазами) и можете поделится с какой стороны вообще подойти к данному вопросу. Интересует все: литература, практические аспекты, советы етс. Буду очень признателен за дискусс в любой форме Заранее спасибо
-
А в чем воопрос то? Вам колона нужна или метод? От чего очищать хотите? Какой апарат у Вас? Какой детектор?
-
Держи рядом деревянные палочки от мороженого, или жувачки купи твердые (Big Red Cinnamon - забугорные, но жевать можно целый день). Сам так делаю - помогает концетрироватся.
-
Кофакторы - общее название для компонентов котрый позволяют ензиму катализ. Сдесь есть и органика (нп витамины) и неорганика (нп йоны металов). Апоензим + кофактор = активный ензим (другое название холоензим) Коензимы - небелковый компонент который цепляется к ензиму (часто в области активного места) но только на время самого катализа - подтип кофакторов Простетическая група - перманентно (ковалентная или координационая связь) подключается к активному центру ензима. - подтип кофакторов Это фундаментальная разница. Отдельно взятая ПГ или отдельно взятый коенз с разным апоензимом может вести себя по разному гем в каталазе - простетическая група. Кофактором является манган (Mn)
- 3 ответа
-
- 2
-

-

-
Знаете, мы на лабах с микробиологии проверяли свойства чеснока китайского и польского (тк это в Польще было) ингибировать рост бактерий. Так нам колонии прям на китайском чесноке выросли, а контрольный польский - воокруг чесночных зубчиков все было чисто.
-
Провел реакцию с роданидом амония на выпареной (на 3/4 объема) пробе воды - на нормальную желто-оранжевую окраску накладывается еле заметный легко красный оттенок. Думаю можно пробу считать позитивной. Может катализирует что-то? В интернетах нашел информацию что фиолетовый цвет в такой реакции - результат вхождения в процес нафталена. Тоесть разных субстанций там много сделалось.
-
Фенол-сернокислый метод на анализ сахаров
Angry_Biotechnologist опубликовал тема в Аналитическая химия
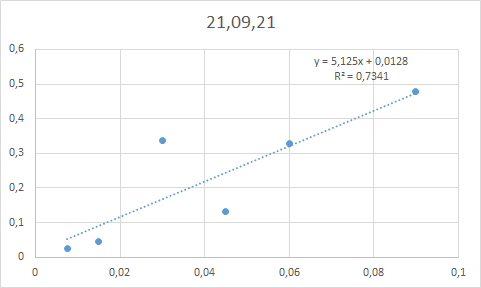
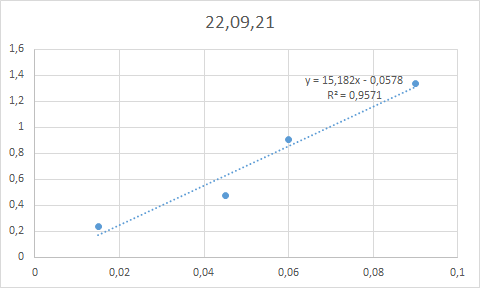
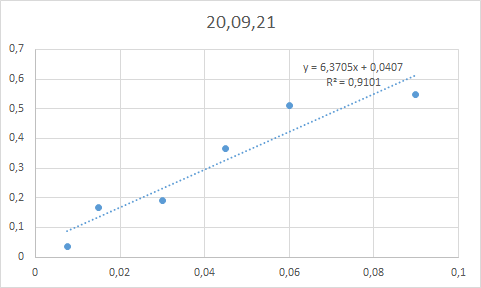
Добрый день, Пытаюсь провести опыт на анализ лактозы модифицированым методом Дюбоиса (Dubois method). Первая попытка заключалась в следующем: 80% м\м фенол 20мкл + 0.4мл анализируемого р-ра (0.095г\л и менее) + 1.2мл 96% H2SO4. Вторая попытка: 1мл р-ра + 1мл 5% фенола + 5мл кислоты. Третяя попытка: 1мл р-ра + 5мл кислоты - нагрев до 90°С в течении часа + фенол. Результаты очень странные - первый раз в пробирке получились все цвета радуги, разделенные на фазы (легко красный - оранжевый - филетовый потом градация из фиолетового в голубой и зеленый)ю При смешивании фаз получался темный синий цвет или какой-то отенок зеленого. Второй раз - получилось тоже самое только на больший объем. Третий же раз - все растворы вышли синими. для всех растворов используется деминерализованая вода. Фенол - новая банка, открыта мной, но срок годности прошел в 2020. Кислота - новая Пробирки - епендорф или обычные стекляные. Результаты - в общем и целом анализировать не возможно (все что удалось собрать показано в приложении). Те числа что видно на графике: отобраны из разных паралелей измерения так чтобы максимально подходить для создания кривой (одним словом - результаты ненадежны). Пробирки с 3ей попытки синий цвет постепенно потеряли - через 1-2 дня его уже небыло в большинстве растворов. Смешивание чистых кислоты и фенола дает яркий бирюзовый цвет. Фенол + кислота + вода - темный синий цвет. Добавление меньшего количества фенола иногда помагает - раствор становится легко оранжевым/желтым, но в основном получается зеленый раствор. Спасибо за внимание, -
Фенол-сернокислый метод на анализ сахаров
Angry_Biotechnologist опубликовал тема в Органическая химия
Добрый день, Пытаюсь провести опыт на анализ лактозы модифицированым методом Дюбоиса (Dubois method). Первая попытка заключалась в следующем: 80% м\м фенол 20мкл + 0.4мл анализируемого р-ра (0.095г\л и менее) + 1.2мл 96% H2SO4. Вторая попытка: 1мл р-ра + 1мл 5% фенола + 5мл кислоты. Третяя попытка: 1мл р-ра + 5мл кислоты - нагрев до 90°С в течении часа + фенол. Результаты очень странные - первый раз в пробирке получились все цвета радуги, разделенные на фазы (легко красный - оранжевый - филетовый потом градация из фиолетового в голубой и зеленый)ю При смешивании фаз получался темный синий цвет или какой-то отенок зеленого. Второй раз - получилось тоже самое только на больший объем. Третий же раз - все растворы вышли синими. для всех растворов используется деминерализованая вода. Фенол - новая банка, открыта мной, но срок годности прошел в 2020. Кислота - новая Пробирки - епендорф или обычные стекляные. Результаты - в общем и целом анализировать не возможно (все что удалось собрать показано в приложении). Те числа что видно на графике: отобраны из разных паралелей измерения так чтобы максимально подходить для создания кривой (одним словом - результаты ненадежны). Пробирки с 3ей попытки синий цвет постепенно потеряли - через 1-2 дня его уже небыло в большинстве растворов. Смешивание чистых кислоты и фенола дает яркий бирюзовый цвет. Фенол + кислота + вода - темный синий цвет. Добавление меньшего количества фенола иногда помагает - раствор становится легко оранжевым/желтым, но в основном получается зеленый раствор. Спасибо за внимание,