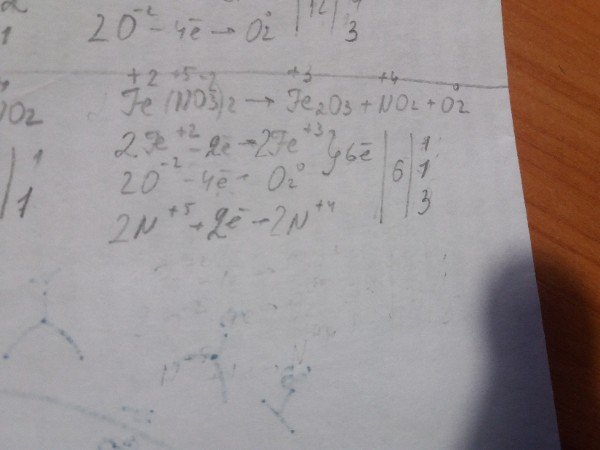-
Постов
96 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Никита Пастернак
-
Если да, то приведите примеры. И еще вопрос: свойство щелочей - реакция с солями амфотерных металлов. Если амф. металлы только лишь Be, Al и Zn, то получается, что реакция щелочи с FeCl3 не пойдет?
-
Я имею в виду, если брать электрохимический ряд неразвернутый, который в школьных учебниках дается
-
Я правильно понимаю, что в них входят: 1. Щелочные 2. Щел-зем 3. Мg, Al
-
Да нуу. Ведь азотистой к-те соответствует N2O3, а азотной -N2O5
-
Увидел тут такую штуку, хотя до сих пор считал, что у бурого газа нет соответствующих ему кислотных гидроксидов
-
Мне кажется, что d. И еще: Lu и Lr - это же f -элементы? И еще вопрос: La2O3 - это основный оксид?
-
Я понимаю, о чем вы. То есть, вы вообще хотите сказать, что лучше всегда записывать электронный баланс так, чтобы было видно сразу, если отнимаем 4 электрона у кислорода, то надо прибавить именно 4 электрона к азоту и никак иначе? Тогда понятно, что первое уравнение действительно нужно умножить на два и тогда получится 4N^+5 +4e = 4N^+4. Вы хотите сказать, что моя запись, где я передал 2 электрона, а не 4, считается неверной?
-
посмотрите на первое сообщение аль де барана : "Во-вторых, при определении коэффициента при O вы не учли, что окисляются не все атомы O, а большая их часть переходит в продукты ОВР (Fe2O3 и NO2) без изменения степени окисления, поэтому после удвоения формулы Fe(NO3)2 надо подсчитать общее число атомов O, а потом вычесть из него число атомов O, не изменивших степень окисления. Эта разность и будет коэффициент при O. В данном случае этот коэффициент получается равным единице (12 - 3 - 8), но поскольку молекула O2 образуется из двух атомов O, то надо ещё раз удвоить все коэффициенты."
-
Но ведь общее число атомов O 13, да и откуда вы взяли 8? Получится, что 13-3-2=8 Да и баланс кислорода я правильно написал, нет разве? И непонятно, откуда вы взяли именно 4Fe?? То есть хотите сказать, что всегда сумма отнятых и прибавленных электронов должна быть нулю? Но при электронном балансе разложения нитрата магния получается, что 2-4=-2 электрона, а не ноль.
-
-
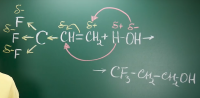
c2h4+k2cr2o7+h2o=
-

Может и тупые вопросы, но мне над знать очень :)
Никита Пастернак опубликовал тема в Решение заданий
1) Что значит эта точка в двойном оксиде feo·fe2o3? 2) Какая степень окисления кислорода в озоне? 3) Реально ли возможна реакция hno3+p2o5=n2o5+hpo3? 4) na+o2=na2o(20%)+na2o2(80%)? 5) Супероксиды и надпероксиды это одно и то же? Если нет, то в чем различия? 6) cro3=cr2o3+o2 Идет ли в обратную сторону? 7) Амфотерные оксиды друг с другом реагируют? 8) p2o5+h2o=образуется либо метафосфорная, либо ортофосфорная кислоты? -

Не могу запомнить реакцию, потому что не понимаю
Никита Пастернак опубликовал тема в Решение заданий
-
Какой объём кислорода требуется для сжигания газовой смеси, состоящей из водорода и метана с плотностью по гелию 1,2, если взяли: а)100л газовой смеси; б) 100г газовой смеси? Ответ: 80л; 358л
-
Черт, я дура Спасибо