
Alex_Raven
-
Постов
18 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Alex_Raven
-
-
Э.д.с. элемента Cd|CdCl2|AgCl|Ag при 298 К равна 0,625 В, а температурный коэффициент э.д.с. равен -6,5*10^-4 В/К.
1) Напишите уравнение реакции, протекающей в єлементе;
2) Рассчитайте dG, dS, dH для этой реакции при 298 К
-
Разложение вещества является реакцией 2 порядка с энергией активации 23,1 кДж/моль. При 300К разложение проходит на 90% за час. Вычислить температуру, при которой вещество разлагается со скоростью 75% в минуту. (Начальные концентрации одинаковы).
-
-
-
Для некоторой реакции dH = -100 кДж/моль, dU = -95 кДж/моль. Для повышения равновесного выхода продуктов необходимо:
а) увеличить Т и Р
б) снизить Т и Р
в) снизить Р и увеличить Т
г) увеличить Р и снизить Т
Ответ агрументировать
-
При какой температуре закипит раствор 1 моля Na2CO3 в 1,5 л уксусной кислоты?
-
-
(CH3)2C-C≡CH + (ДЦГ)2B-H ----> (CH3)2C-CH=C-B(ДЦГ)2 --(H2O2, NaOH, -NaOB(ДЦГ)2)--> [(CH3)2C-CH=CH-OH] ----> (CH3)2C-CH2-CHO
(CH3)2C-CH2-CHO + NaHSO3 ----> (CH3)2C-CH2-CH(OH)-SO3Na
(ДЦГ)2B-H - это дициклогексилборан
Спасибо
-
-
Хотя бы наведи пример вещества
-
Однако!
"метилуксусная кислота" - это пропионовая?
"имид кислоты" - это что?
В точном смысле слова "имид карбоновой кислоты" - это вещество вида R-C(=NH)-OH. Но это ничто иное, как протомер амида кислоты (R-CO-NH2), очень нестабильная молекула, мгновенно превращающаяся в амид.
Поэтому синтезировать "имид метилуксусной кислоты" просто невозможно, как невозможно "синтезировать" виниловый спирт.
Уточните вопрос.
Я знаю, что звучит глупо, но это вопрос на экзамене, и преподу не скажешь, что такого не может быть
-
-
C6H6 --(HNO3, H2SO4)--> C6H5-NO2 --(Fe, HCl)--> C6H5-NH2 --(NaNO2, HCl)--> [C6H5-N2]+Cl- --(NaHSO3)--> C6H5-NH-NH2
C6H6 --(CH3COCl, AlCl3)--> C6H5-CO-CH3 --(CH3Cl, AlCl3)--> CH3-C6H4-CO-CH3 (мета-изомер)
На самом деле последняя реакция не идёт, но все школьные учебники этот факт упорно игнорируют.
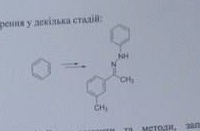
CH3-C6H4-CO-CH3 + C6H5-NH-NH2 --(-H2O)--> CH3-C6H4-C(CH3)=N-NH-C6H5
Спасибо
-
Нужно синтезировать вещество в несколько стадий
-
Как из оксобензола получить нитробензол?
-
2-метил-4-пропилгекс-1-ен
-


Потенциометрическое титрование. Определить концентрацию Na2S используя один из двух методов
в Решение заданий
Опубликовано
Определить концентрацию Na2S используя один из двух методов:
1. Выбрать 2 титранта и 1 электрод
2. Выбрать 1 титрант и 2 электрода