
Makaev Zaynutdin
-
Постов
41 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Makaev Zaynutdin
-
-
Окисление - это тип реакции.
Механизм реакции это другое.
На приведенных примерах - просто окисление-
 1
1
-
-
https://yadi.sk/i/Y39IrZb6eql5_g
Пройди по ссылки - скачай.
Тут как то по дурацки все сделано, нельзя загружать больше 0,2 мБ фото.-
 1
1
-
-
03.04.2020 в 15:10, Максим0 сказал:
Если эти вещества адски сложные, то бегите в военкомат - там вас спасут из ада! Это лучший выход чем учить ТФКП, тензорный анализ да урматфиз... а на старших курсах вообще вычислять какой-нибудь кошмар типа расчёта спектра атомарного оганессона - бывают и такие преподаватели-извращенцы.
А пока расслабьтесь, у вас элементарная ароматика, даже не конденсированная, это не 119 зарядов в атоме оганессона.

...Если не сведут с ума
Римляне и греки,
Сочинившие тома
Для библиотеки.
Если те профессора,
Что студентов учат,
Горемыку школяра
Насмерть не замучат,...
Ты идиот ? Хул676555и ты выебы888888ваешься то придурок ? Помощь можешь оказать - оказывай, не можешь проходи дальше
-
Все правильно Чех написал.
Реакция идет при 20-25 градусах при а.д. ? Да
Какой ее там тепловой эффект - это уже дело 15 е -
На самом то деле, не совсем понятно, зачем что то выдумывать если - руки с мылом? d ntxtybb 20-3- ctreyl - помогает 100 %
-
-
Смит, Дильман: Основы современного органического синтеза
-
5 минут назад, yatcheh сказал:
При ацилировании связывается хлор
CH3-CO+[AlCl4]-
Механизм образования каталитического комплекса с BF3 такой же, как и с AlCl3.
NF3 вообще никаких акцепторных свойств не проявляет.
Но ведь вопрос в другом был....
-
Да вроде все в порядке..
-
16 часов назад, Иван1978 сказал:
Кинетика, идет но МЕДЛЕННО
-
1 час назад, davidwagner012 сказал:
возможно ли восстановление оксидов Ca0 и Ag2O газообразным водородом при стандартных условиях(известны величины энергий Гиббса(ΔGf) для оксидов и продуктов восстановления)
CaO + H2 = Ca +H2O
ΔGf кДж/моль -603.46 0 0 -273.23
Ag2O + H2 =2Ag +H2O
ΔGf кДж/моль -10.90 0 0 -273.23
Как предложено автором выше, нужно найти разницу энергий обр. Гиббса продуктов реакции и исходных веществ, в итоге получите что, первая реакция не пойдет, вторая пойдет в обычных условиях.
-
 1
1
-
-
1 час назад, andrey1999 сказал:
Как в данном случае выяснить термодинамическую возможность протекания реакций между растворами КМnO4 и Na2SO3 в: 1) кислой; 2) щелочной; 3) нейтральной среде? На фото полуреакции. И в какой среде окислительные свойства MnO4^- выражены сильнее?
Необходимо узнать ЭДС, путем нахождения разницы окислительно-восстановительных потенциалов, каждой из полуреакции. Затем по формуле из значения ЭДС, находишь энергию Гиббса. Если значение отрицательное, то реакция термодинамически - возможна, если положительное - значит- невозможна.
-
 1
1
-
-
-
9 минут назад, ChemProfi сказал:
Ну, если разобраться, эта задача вообще перебор, как заметил ув. yatcheh - неприличный анекдот

Но за вариант спасибо
Да уж, анекдот так анекдот....
-
-
22 часа назад, Nemo_78 сказал:
. Попробуйте не пугать учителя вот таким нехитрым способом, и тоже в три стадии:
1) полное дегидрогалогенирование 1,1-ДХЭ избытком спиртовой щёлочи => ацетилен;
2) частичное гидрирование ацетилена на платине до этилена;
3) классическая реакция Вагнера (окисление этилена 1%-ным водным перманганатом на холоду) => искомый этиленгликоль.
. С уважением
Не, ну дегидрогалогенирование до ацетилена - это уже совсем перебор
Мой вариант:
1) щелочной гидролиз до ацетальдегида.
2) восстановление до этилового спирта3)дегидрирование этанола - до этилена ( в среде фосфорной кислоты)
4)этилен - реакция Вагнера (взаимодействие с раствором перманганата калия) - получение этилен гликоля.
-
-
В 06.11.2018 в 21:21, yatcheh сказал:
Бро, там две задачи, это ответ на вторую.
Присоединение чего к чему?
Для меня это загадочная реакция... И субстрат такой затейливый.
Нет, понятно, что окислить можно всё, что угодно и куда угодно. Но, как-то трудно сделать выбор...

-
8 часов назад, sima4832 сказал:
CH3-CH2-CH(C2H5)-CH2-CH3 + HNO3 = СH3-CH2-C-(C2H5)(NO2)-CH2-CH3 + H2O
образуется 2-нитро-2-этилпентан и вода, условия температура 140 градусов и давление. И всё???
Ну какая то часть продукта реакции будет вторичным нитро производным
-
 1
1
-
-
"Промываете" под этим скорее всего подразумевается - экстракция этими растворами, после отделения нужной Вам части ( водную часть в одну колбочку, органическую в другую) в колбу с органической фазой засыпаете ну где то треть чайной ложки этого прокаленного поташа, слегка взболтнуть можно. Время здесь не принципиально, в том плане что если Вы подержите 50 минут, ничего страшного не случится.
-
-
Не будет он взаимодействовать с ним конечно же, так как в самом хлороформе дохера и больше соляной кислоты, которая образуется из самого хлороформа.
Что значит "сильные растворители" ? чем определяется сила не совсем понятно.. -
Ну если Вы имеете ввиду под "карбидным методом" получение из карбида кальция, то можно пойти таким путем : !)гидролиз карбида кальция до ацетилена, затем обработка последнего амидом калия, полученный ацетиленид натрия, подвергнуть взаимодействию с пропил йодидом например, с получение Пентина -1.
-
19 часов назад, Бекки сказал:
Рассчитать рН группового растворения карбонатов меди (II), цинка и кальция
Мои рассчеты, привели к ответу pH=6,579.
Все эти 3 карбоната - мало растворимые соединения, узнав ПР каждого из них, вычислил равновесную концентрацию карбонат аниона, в воде (т.к. МАЛОрастворимы, но РАСТВОРИМЫ и в растворе есть и катионы и анионы).
Получил 3 значения концентрации карбонат анионов.
Растворение будет происходить при образовании гидрокарбонатов данных металлов т.е. на каждый карбонат анион будет приходится 1 протон водорода, следовательно их концентрации равны (сколько одного, столько и другого). Затем просуммировав концентрации карбонат анионов от трех соединений, нашел их общую концентрацию, которая равна концентрации протонов водорода, затем взял отрицательный десятичный логарифм этого числа, получил pH=4,091.
Минимальная pH растворения равна 6.579
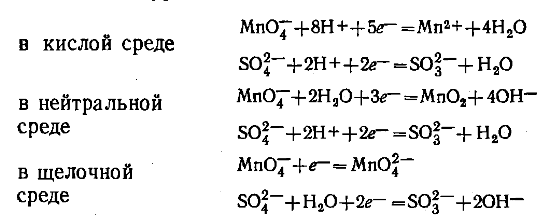

Кислотность органических соединений и малоновый эфир
в Решение заданий
Опубликовано · Изменено пользователем Makaev Zaynutdin
Алкилирование в данных случаях - это нуклеофильное замещение по сути дела.
А уходящие группы, при sp2 гибридизованном атоме углерода, очень плохо вступают в реакции нуклеофильного замещения.
В случае с 1 примером - в принципе оно возможно, но во первых здесь стерические затруднения, во вторых возможно протекание побочного элиминирования.