
Тинаева
-
Постов
60 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Тинаева
-
-
Может поможет http://www.chem.msu.su/rus/teaching/levanov/levanov.pdf
да видела) но это немного не то(
-
как применяется метод квазиравновесных концентраций в теории активированного комплекса?
-
смотрите в википедии - BN - гексагональная решетка - это шестигранная призма, что сложного?
http://dssp.petrsu.ru/p/tutorial/ftt/Part1_/part1_6.htm - вюрцит, сфалерит.
да я это все видела) ладно, спасибо

-
с этим то понятно

-
сначала вы рисуете ячейку, потом делите граничащие атомы на количество ячеек в которых они участвуют и затем суммируете внутренние атомы с долями внешних атомов. А что там за проблема? как ячейку построить?
нет, не пойму как рассчитать именно.
например в хлориде цезия число атомов рассчитывается : 8*1/8 =1
1*1=1
а в этих типах запуталась , можете помочь ?
-
-
Константа равновесия реакции Н2 + I2 = 2HI при 633 К равна 61,6, а при 718 К – 41,7. Сравнить среднее значение теплового эффекта и сродство этой реакции при температуре 718 К. Вычислить изменение энтропии.
Для того чтобы найти тепловой эффект воспользуемся формулой : ln(kp1/kp2) = H * ( T2- T1) / T1*T2
в итоге ответ получается -2085 и измеряется в К. Как решать эту задачу? -
-
всё верно, тогда далее по пунктам.
2) PОБЩ= nRT/V, n - это равновесное число моль компонентов смеси?
P = 37160
Используя закон Дальтона pi= xi*p получим : pi= 37160 * 0.35= 13204 , но почему то не сходится ответ
по сути незачем, там объём красивый потому в этой задаче она смысла особого не имеет, но в Кс оперируют концентрациями.
да, где n - число моль всех веществ, R, T и V даны в условиях задачи.
все поняла, спасибо большое! я похоже м3 не перевела в л
-
Как Вы n(HI) находили?
1) Объём дан для расчета концентраций реагирующих веществ H2 и I2, концентрацию HI находите решая уравнение.
2) По уравнению Менделеева-Клапейрона находите общее давление в системе
3) Зная моль веществ, несложно найти их мольные доли и парциальные давления.
Нашла сначала число моль n(I2)=0,005 и n( H2)= 0,01. Пусть изначально в системе было 0,005 моль йода и 0.01 моль водорода, тогда образовалось 2х моль HI , а прореагировало 0,005-x и 0.01-x. Cоставляем уравнение Кр= 4х2 / (0.005-х)* ( 0.01-х)
Как Вы n(HI) находили?
1) Объём дан для расчета концентраций реагирующих веществ H2 и I2, концентрацию HI находите решая уравнение.
2) По уравнению Менделеева-Клапейрона находите общее давление в системе
3) Зная моль веществ, несложно найти их мольные доли и парциальные давления.
А концентрацию для чего находить?
-
Константа равновесия реакции H2 + I2 = 2HI при 718 К равна 50. Сколько моль HI получится, если нагреть до этой температуры 1,27 г йода и 0,02 г водорода? Чему будут равны парциальные давления всех газов, если объем равновесной смеси равен 0,001 м3 ?
Число моль HI я нашла, n= 0,0934. Как найти парциальные давления? И что делать с объемом?) -
-
А в чем сложность-то? Вы же нашли давление СО?
Углерод - твёрдый. В константу равновесия его давление не входит. Давление водорода равно давлению СО. Давление Н2О вычисляется из константы.
я просто сомневалась немного, что давление СО равно давлению H2
если это так, то спасибо большое!
-
С(прореаг) = С(исх)-С(равн)= 0,02-0,007=0,013 моль/л
Кс = (0.013 * 0.013)/ 0.007 = 0.024 моль/л
-
Определить равновесный состав газовой фазы под общим давлением 101325 Па для реакции С+Н2О=СО+Н2, если Kp=285573 Па.
Если я воспользуюсь выражением Pco= 1/2 *( -Kp+[( Kp)^2+ 4* Kp* p]^1/2 ) = 79303 Па, тоxco= 79303/101325= 0,79
А как мне найти состав оставшихся компонентов ? -
-
И константа равновесия то неизвестно какая: константа образования или константа диссоциации?
я думаю, что константа образования дана
-
Я их беру n, эта буковка вылезает за скобку
да это я поняла) просто продукты у вас идут 1/2n
-
Условия задачи, мягко говоря... Начальные количества обоих компонентов неизвестны. Можно предположить, что:
1. Йод взят в избытке; 2. Он остается твердым при 718 К

Тогда в газовой фазе - только HI и можно как-то реально посчитать его диссоциацию.
2HI = H2 + I2 - число молей газа на первый взгляд не меняется, и давление действительно должно сократиться. Но! Не забывайте, что мы знаем: йод остается твердым при 718 К! Вот так! Тогда давления, связанного с йодом, нет. Остается:
парциальное давление HI: {n(1-a)/[n(1-a)+1/2*na]}p = {n(1-a)/[n(1-1/2*a)]}p
парциальное давление H2: {1/2*na/[n(1-1/2*a)]}p
где n - исходное число молей HI, p - давление
1/2*na*[n(1-1/2*a)]p a-1/2*a2
Константа равновесия: К = -------------------------- = 1/2*р*-----------
n2(1-a)2 (1-a)2
У Вас там плюсы, а не минусы в скобках с двойкой - не учли диссоциацию HI. Дальше - сами... Я, честно, не знаю, как тут быть без твердого йода.
а почему изначально вы берете число моль 1?
-
В сосуд, содержащий некоторое количество твердого йода, введен водород. Определить степень диссоциации HI при температуре 718K, если константа равновесия равна 50.
Какое уравнение будет? K= [n^2*a^2/(a+2)^2] * p^2 / [ 4n^2*p^2] / (a+2)^2, где а- степень диссоциации
если так решать, то у меня сокращается давление и выходит неверный ответ. Подскажите, как правильно записать -
-
В сосуд, содержащий некоторое количество твердого йода, введен водород. Сосуд запаян и нагрет до 718 К. После наступления равновесия газовая смесь содержала 62,33% (объемн.) HI; 35,48% (объемн.) Н2 и 2,19% (объемн.) I2. Определить константу равновесия реакции H2 + I2 =2HI и степень диссоциации HI при этой температуре.
-
Да ,это в ответах) но в ответах тоже могут быть ошибки)
127 Дж/г -это в правильных ответах дано?Да, это в ответах) но в ответах тоже могут быть ошибки)
-
Формулы бывают разные. И если в формулу входит молярная масса бензола, то и энтальпия там тоже молярная.
Вот вам такая формула:

Буквой Лямбда здесь обозначено то, что вы ищите - удельная теплота плавления (Дж/г)
Все равно не получается, энтальпия 79 приблизительно выходит, а должна 127

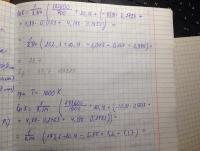




Баланс
в Решение заданий
Опубликовано
Bi2O5+HCL= BiCl3+Cl2+H2O
Как сделать методом полуреакций?