
alex_dnt9
-
Постов
40 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные alex_dnt9
-
-
Даже не знаю
-
-
а не могли бы помочь с объяснением интенсивности коррозии? эдс ведь это разность потенциалов, и я не могу в двух случаях понять какие разности брать
-
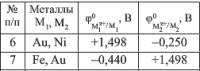
Определите, к какому типу относится покрытие, нанесенное на сталь (потенциал стали примите равным стандартному потенциалу железа φ(Fe(2+) /Fe) = -0,440 В). Напишите уравнения процессов, возникающих в случае разрушения покрытия: а) в морской воде, pH = 8; б) в воде системы отопления (деаэрированная среда). В какой среде коррозия протекает интенсивнее? Ответ подтвердите расчетом ЭДС коррозионного элемента,приняв активность ионов корродирующего металла равной 10^(‒6).
к какому же типу покрытия будет относиться Сu нанесенная на Fe
-
В системе СИ надо брать концентрацию в моль/м3, тогда бе�ез всякого деления на 1000 получите давление в Па
Если вы берете концентрацию в моль/л, то давление сразу получаете в кПа,
т.е. ваш ответ 1110 кПа
Порядок величины можно прикинуть так:
при н.у. (это давление 100 кПа) в 1 л находится 1/22,4= 0,045 моль вещества
У вас в 5 раз больше, да еще изотонический коэффициент почти 2,
таким образом давление должно быть в 10 раз больше нормального, около 1000 кПа
Что и имеем.
Большое спасибо
-
Зависит от концентрации, но обычно значение уже в сотнях кПа
смотрите какие у меня данные
m=34,21г
V=1л
M=146г/моль
T=298K
посчитал молярную концентрацию, она равно 0,23 моль/л
посчитал изотонический коэффициент, он равен 1,95.
и дальше давление
P=1,95*0,23*8,31*298=1110(ну а тут я поделил на 1000 и получил в обозначениях Дж/м^3- а это вроде как паскали, или все-таки нет?)
-
подскажите пожалуйста. задача на определение осмотического давления водного раствора электрлита. посчитал и получил 1,1 Па это норма? имею в виду не слишком ли маленькое?
-
такая вот штука у меня, дано Al(OH)3-->Al(3+)+OH-, это малорастворимое соединение. если я знаю общую молярную концентрацию ве-ва, то как найти концентраци Al(3+) и OH-? они же будут меньше общей концентрации, тк это малорастворимое соединение, верно?
-
А вы как думаете? Делийская железная колонна 100500 лет стоит, а в Долине Царей в Гизе ни о одного золотого предмета не осталось.
шутку понял, но не могли бы вы объяснить для чего нам даны потенциалы, ведь чтобы написать анодное и катодное уравнение они вроде как не нужы?
-
если Fe нанесен Au
-
если на Fe нанесен Au. Какой из металлов корродирует в атмосферных условиях при нарушении сплошности покрытия, приведите уравнения анодного и катодного процессов. данные по 7му варианту
-
где бы нормальную таблицу стандартных электродных потенциалов смотреть. В Википедии у галогенов 0 вольт стандартный электродный потенциал пишут у кислорода тоже, что есть неправда. У кислорода стандартный электродный потенциал должен быть равен ЭДС водородно-кислородного элемента 1.229 вольт. Вроде так.
Тогда ЭДС свинцово кислородного элемента без учета активностей будет 1.229-(-0.126)=1.355 вольт.
а для чего нам тогда кислотность дана? а если с учетом активностей, то куда ее "впихнуть"?
Второй электрод - как бы кислородный.
нашел вот такую формулу для потенциала, где Z число электронов участвующих в реакции, но не могу понять в моем случае от что один?
-
Что-то как-то вы сильно замудрили)
Ещё из аналитики помню таблицу для р расчёта pH разных растворов. Для расчёта pH сильной кислоты исходим из того, что концентрация ионов водорода будет равна концентрации.
Значит, pH=-lg(c )
pH= -lg(7*10^-2)
pH= 1,1549.. или 1,16
только что прочитал в методичке что pH=-lg(a(H+)), т.е. логарифм от активности ионов. а чтобы их найти нужно применить ионную силу
-
вычислить электродный потенциал металла корродирующего во влажной аэрированной среде при температре 298 К и электродвижущую силу коррозионного элемента при извнстных значения активности металла
дано Pb
фо=-0,126 В
а(Mz+)=0,0002 моль\дм^3 активность ионов металла
pH=2,9
подскажите пожалуйста ход решения с формулами, если можно объясните что к чему, не хочу просто списывать, хочу хоть емного разобраться, за ранее спасибо))
-
нет.
Начать с того, что формула вещества записано неверно
Формула для ПР записана неверно
Концентрация гидроксид-ионов не найдена.
Так что и расчет - ни о чем
а если так, Al(OH)3
ПР=[Al3+]*[OH-]^3? а как найти концентрацию гидроксид-ионов?
-
дано
Al(OH2)
молярная концентрация насыщенного раствора 6,78*10^-9
ПР=[Al3+]*3[OH-]=6,78*3*6,78=137,9. правильно ли использовал молярные концентрации? и вообще решение правильно?
-
дано
ионное произведение воды K(H2O)=1*10^-14
электролит HCLO4
молярная концентрация водного раствора 7*10^-2 моль\дм^3
исходя их того что вычитал в интернете получилось небольшое решение
исходя из уравнения диссоциации делаем вывод что концентрации иона водорода и самого электролита равны, поэтому
рН=-lg(H+)=-lg(C(H+)*(сигма)) где сигма - находится по таблице. чтобы ее найти нужно найти ионную силу ионов водорода, ее я нашел она у мня равно 0,07, а дальше не могу найти подходящую таблицу, в каких то таблица значения коэффициента ближе к единице, в каких то ближе к нулю. не могу разобраться. может кто-нибудь помочь и заодно проверить решение? буду очень признателен))
-
dB/dt = kB*A2
A = A0 - B*2
dA/dt = -2*dB/dt = -2*kB*A2 = kA*A2
kA = -2*kB = -2*(2.4*10-3) = -4.8*10-3
, где A и B - концентрации
kB - константа скорости по B
kA - константа скорости по A
Вот так
это получается нам известна константа равновесия, а как газофазная реакция как же?
-
определите скорость газофазной реакции по каждому компоненту, если известна скорость образования r какого-либо продукта
реакция 2А-->В продукт В r, моль / (л ⋅ с) -- 2,4⋅10^-3
подскажите пожалуйста, как определить скорость, есть какая-нибудь формула, гугл не спасает
-
Ясен пень, что если от А и С ничего не зависит, то в уравнении им делать нечего.
ну само уравнение правильно составлено?
-
дана гетерогенная реакция A+B+C-->продукты известно что, если увеличть концентрации вещества в 2 раза, то скоростьреакции возрастет 2,83 раза, а при увеличении концентрации реагентов А и С скорость реакции не изменяется(все протекает при постоянной температуре)
если при изменении концентрации веществ А и С, скорость реакции не изменяется, то в кинетическом уравнении их по идее вообще быть не должно? и подскажите как определить константу скорости в этом случае. или может есть какой то своеобразный ход решения?
приблизительное уравнение верно?
v=k*C^1.5 так? или можно еще как то найти константу?
-
сейчас зарплаты только так и повышают
-
рассчитать, во сколько изменится скорость реакции после того как прореагирует 70% N2O, если исходная концентрация этого вещества равна 2 моль/дм^2
проверьте решение пожалуйста
дано уравнение 2N2O-->2N2+O2
скорость реакции равна V=k*C[A]^2 так как прореагирует 70% вещества, то концентрация увеличится в 0,3 раза, следовательно скорость реакци увеличится в 0,09 раз, правильно?
-
1 - равновесие, остальное - догадайтесь.
А почему равновесие?
1 - равновесие, остальное - догадайтесь.
а разве не в 4-ом случае равновесие получается?
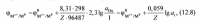
гидролиз
в Решение заданий
Опубликовано
Так?