-
Постов
78 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные vitaliusik
-
-
Здравствуйте! Помогите решить задачу по аналитической химии, мне уже скоро сдавать нужно, время на раздумья дали мало.
ЦитатаТочную массу сульфаниловой кислоты ( 0,001 моль) растворяют в мерной колбе вместимостью 100 мл, добавляя вначале 10 мл воды и 10 мл 2N соляной кислоты, а затем доводят дистиллированной водой до метки. В коническую колбу для титрования вносят 10 мл приготовленного раствора, добавляют 30 мл дистиллированной воды, 10 мл 2N соляной кислоты, 5 мл 20%-ного бромида калия, 3 капли 0,15%-ого раствора индикатора - нейтрального красного . Титруют 0,1 N раствором NaNO2, приливая в начале титрования по 1 -2 мл, а в конце - по каплям. Сколько мл титранта идет на титрование аликвоты препарата?
-
В четыре пробирки налейте небольшие объемы растворов иодида,
бромида, хлорида и фторида калия. Во все пробирки прибавьте немного (2-3
капли) раствора нитрата серебра. Отметьте цвет образующихся осадков.
Повторите опыт, предварительно наполнив пробирки на ¾ водой, добавив в
каждую пробирку с соответствующими галогенидами калия 2-3 капли
нитрата серебра. Можно ли теперь по цвету осадков определить, какой
галогенид образуется? После опытов содержимое пробирок вылить в
специальную банку для серебряных отходов.Как добавление воды повлияет на цвет осадка?
-
Доброго времени суток, помогите пожалуйста решить задачу, мое неверное решение прикрепил. Ответ: 6,3*10^2
Давление насыщенного водяного пара при нормальной температуре кипения воды (373К) равно 1,013*10^5 Па. Рассчитайте, насколько ниже давление пара на 1% раствором хлорида натрия при 373К, предполагая, что этот раствор является идеальным.
-
-
Вычислите тепловой эффект реакции

если теплоты образования этилена, водяного пара и газообразного этанола соответственно равны 52,28 кДж/моль; –241,8 кДж/моль; –235,3 кДж/моль.
Ответ:

При вычислении теплового эффекта по следствию из уравнения Гесса не сходится с ответом. Для решения методом термохим уравнений нужны промежуточные реакции. Подскажите, пожалуйста, как выйти из ситуации.
-
Помогите пожалуйста!
Текст задачи: В два раствора серной кислоты добавили одинаковые количества цинка. В одном растворе выделилась сера, в другом - сероводород. После завершения всех реакций массы растворов оказались равны. Сравните массы и концентрации исходных растворов.
Моё решение:
-
Текст задачи: В два раствора серной кислоты добавили одинаковые количества цинка. В одном растворе выделилась сера, в другом - сероводород. После завершения всех реакций массы растворов оказались равны.Сравните массы и концентрации исходных растворов.
Не получается решить, кто как думает?
-
Не понимаю как такое решать, подскажите пожалуйста.
Текст задачи: Для полного гидролиза сложного эфира, образованного насыщенной одноосновной кислотой и насыщенным одноатомным спиртом, требуется 9,9 г воды. При сгорании такого же количества сложного эфира образуется CO2 объемом 86,24 дм3 (н. у.). Укажите максимально возможную разницу молярных масс (г/моль) продуктов гидролиза.
-
Нужно без промежуточных стадий осуществить данное превращение.
Помогите пожалуйста.
NaCl --> ZnCl2
-
HBrO3 + 5HBr = 3H2O + 3Br2
K = n(H2O)3 + n(Br2)3 / n(HBrO3) * n(HBr)5n = m/M
Не хватает масс веществ в условии?
-
Всем огромное спасибо!
-
Спасибо всем огромнейшее!
-
-
Как такое дело обстоит с неизвестными газами?
Текст задачи: В смеси газов А и Б массовая доля газа А равна 48%, а его объемная доля - 18,75%. Укажите относительную площадь газа А по газу Б. -
У вас С = 0, 0022 моль/см куб. , разве не так?
И что такое 200 * 0,08 / 0,05 ? Что-то я гляжу и никак не понимаю...
Мне кажется, что должно быть такое уравнение :
200 + 1,04*Х/0,0022 = Х*143,32 + 20*(16 - Х*169,87)
Это строчка 1) в том сообщении выше.
А после того, как найдёте Х, сможете найти ответ : Х/С в см куб. Ответ надо округлить до запятой, т.е. до целого значения.
Я правильно вас понял: по закону сохранения массы расписываем m(AgNO3)+m(HCl)=m(AgCl)+m(оставшегося AgNO3)
Где масса HCl=n*p/C=p*V (ню*плотность:молярную концентрацю=плотность*объём=масса раствора HCl). Дальше что такое 20*(16-х*169,87)? 16-х*169,87 - масса оставшегося AgNO3. А что такое 20? Должно же быть m(р-ра)=m(в-ва)/w, где w-массовая доля нового 5%-ного раствора. То есть должно быть +(16-х*169,87)/0,05
А ещё почему мы не учитываем массу HNO3? Почему уравнение составляется не по такой схеме: m(AgNO3)+m(HCl)=m(AgCl)+m(HNO3)+m(оставшегося AgNO3)?
-
-
Не учли, что нитрата серебра тоже стало меньше (в числителе)
Не учли, что если объем равен х,
то для нахождения массы добавленного раствора надо использовать плотность раствора (в знаменателе)
Как использовать плотность раствора для нахождения этой массы?
Так?
Они все равны в молях - судя по уравнению реакции.
Проще написать всё решение, собраться с силами.
Если писать по указанному сценарию, то :
1 )масса раствора хлороводорода + 200г = масса нового раствора + масса осадка AgCl
2 ) масса осадка = х * М ( AgCl )
3) масса р-ра HCl = Плотность * х / С ( молярная конц-я )
4 ) масса нового р-ра = (100% / 5%) * ( 16г - х*М(AgNO3)
Вроде так, но я сильно не думал и могу снова ошибиться..
Четвёртое действие не понимаю
Как молярную концентрацию использовать для нахождения объема?
-
-
Значит количества вещества HCl через объем вы найдете
Потом посмотрите на уравнение реакции и выразите количество вещества AgCl
Потом вспомните его молярную массу и выразите массу АgCl
А как найти объем? Что-то до меня не доходит
-
А что такое молярная концентрация? Формулу, пожалуйста?
На сколько мне известно, это формула - C=n/v
-
Как через объём HCl выразить массу AgCl, используя молярную концентрацию и плотность хлороводорода?
-
HCl получается в недостатке?
-
Если массовая доля определяется так : 8% в 200г раствора = 16г соли, то нам нужно осадить 8%-5% = 6г соли.
Делим 6г соли на молярную массу - получаем количество молей хлороводорода...
6г. нитрата серебра делить на молярную массу нитрата серебра = количество молей хлороводорода.
Как получили 6 грамм? Не понимаю
-
Замечания есть : вам зачем объём хлороводорода? Вообще, смотрите чему равен объём одного моля любого газа при н.у..
У вас в условиях на фото записаны 5 %, а в тексте - 5,9%.
И далее : вам нужно осадить как раз разницу между этими процентами (8% - 5,9%),- пересчитайте разницу на массу соли и вычислите требуемую массу хлороводорода, по ней и посчитаете, через концентрацию количество раствора.
...Судя по уравнению, количество молей соли и хлороводорода 1:1, поэтому можно посчитать количество молей соли.
Не понятно выражение "осадить разницу между этими процентами". В условии исходная массовая доля 8% и полученная массовая доля 5 %. Объясните, пожалуйста, что вы имеете в виду.
Массу какой соли посчитать? AgCl? По массе AgNO3 считать? Как можно сделать такой вывод, не зная, что взяли в недостатке AgNO3 или HCl


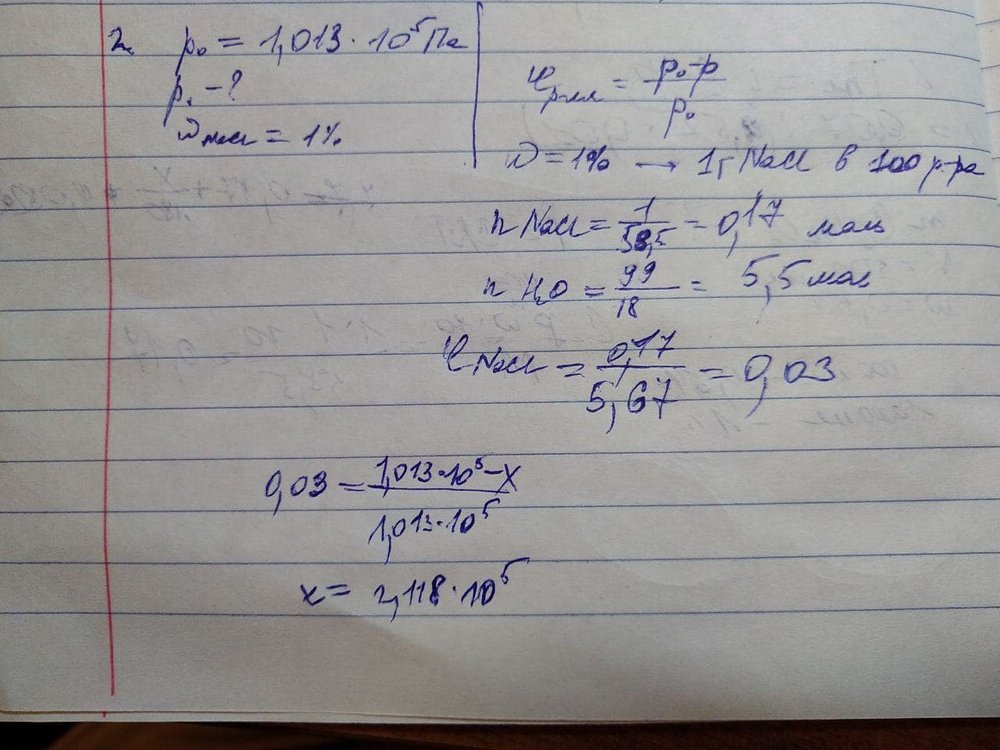
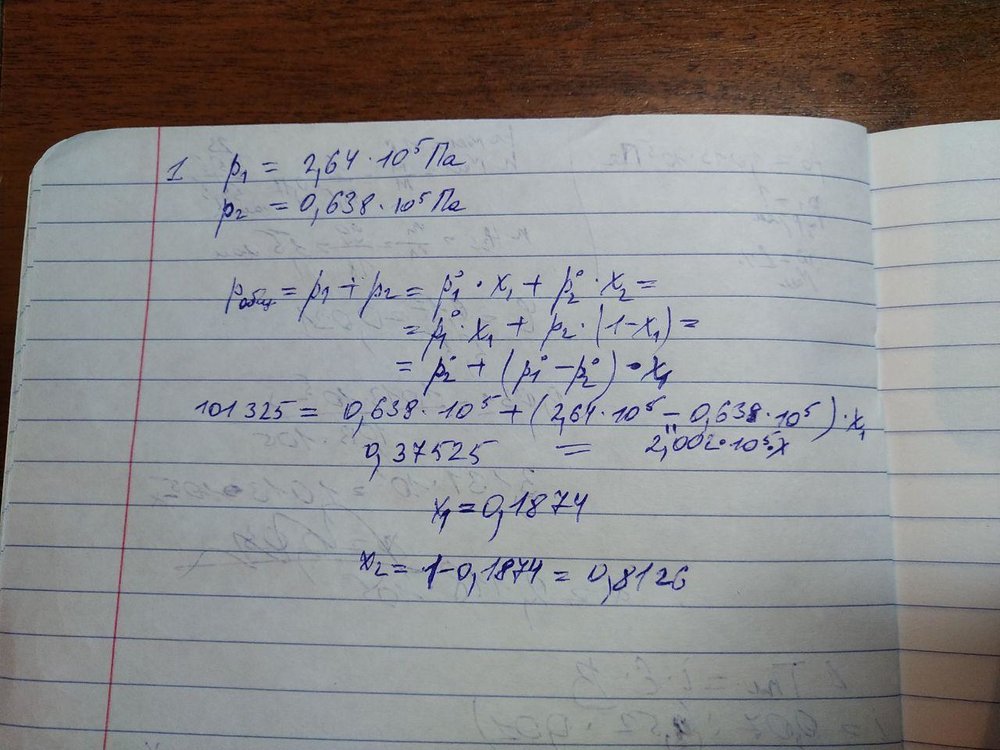

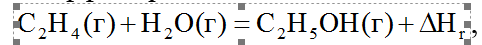
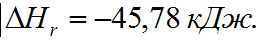


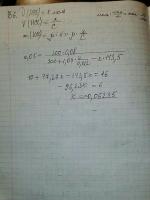
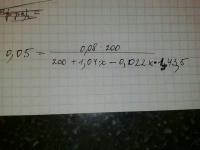
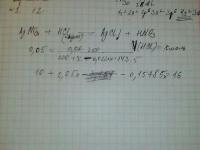
Возможна ли такая реакция по аналогии с фенолом?
в Решение заданий
Опубликовано
Доброго времени суток! Возможна ли такая реакция по аналогии с фенолом? Подскажите, пожалуйста.