
chęmicl881
-
Постов
23 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные chęmicl881
-
-
Текст задачи:
Внутри клеток млекопитающих рН=7,0, а в окружающей жидкости рН=8,0. Рассчитайте возникающую в этих условиях э.д.с. 1) 0,059 В; 2) 0,0295 В; 3) 0,118 В; 4) 0,236 В;
-
Помогите составить схему решения задачи. Есть известно два значения pH (pH внутри клетки и pH окружающей жидкости) и требуется найти ЭДС, нужно найти потенциалы по уравнению Нернста (ЭДС есть разность потенциалов). Если для стеклянного и хлорсеребряного, то для каждого электрода какое из двух значений pH нужно использовать?
-
В задаче требуется найти осмотическое давление для 0,1н раствора глюкозы. В уравнении Вант-Гоффа используется молярная концентрация. Как найти эквивалентное число у глюкозы,чтобы перевести нормальность в молярность?
-
Напишите качественные реакции, с помощью которых можно различить:
1) метиламин
2) метилэтиламин
3) альфа-аланин
Метиламин от метилэтиламина можно отличить по реакции с HNO2 (метиламин - первичный амин, в реакции с HNO2 образуется газ). Метилэтиламин (вторичный) с HNO2 образует нитрозамины (соединения жёлтого цвета). Альфа-аланин от метиламин можно отличить по биуретовой реакции с Cu(OH)2 (синий хелатный комплекс).
Помогите разобраться, правильно ли подобраны реакции.
-
Написать уравнения реакций взаимодействия малоновой кислоты и
1)хлорметана;
Решение (уравнение реакций)
COOH-CH2-COOH+CH3Cl=COOH-CH2-COO-CH3+HCl(метилгидромалонат)
COOH-CH2-COOH+CH3-C(O)Cl->(над стрелкой - триэтиламин) COOH-CH2-C(O)O-C(O)-CH3+[(C2H5)3NH]+Cl-(образование полуангидрида малоновой и уксусной кислот)
Проверьте, правильно написаны уравнения реакций?
-
Как правильно назвать соединение по ИЮПАК? 2-винил-4-метилпентен-1 или 2-изобутилбутадиен-1,3?
-
А) Zn(OH)2+2CsOH=(t,сплавление)Cs2ZnO2+2H2O - цинкат цезия.
Zn(OH)2(р-р)+2CsOH(р-р)=Cs2[Zn(OH)4] - тетрагидроксоцинкат(II) цезия
Б) Zn(OH)2(р-р)+Ca(OH)2(р-р)=Ca[Zn(OH)4] - тетрагидроксоцинкат (II) кальция
В) Ca(OH)2(изб)+HClO4=CaOHClO4+H2O - перхлорат гидроксокальция.
Г) H2SO3+(CaOH)2SO3=CaSO3(осадок)+H2O
Возможны реакции?
-
В 01.01.2019 в 23:47, aversun сказал:
С хлорной кислотой прокатит
Все что с борной кислотой в отношении основных и особенно кислых солей весьма сомнительно и основание и кислота весьма слабые.
Гидроборат калия можно получить?(1 реакция)
-
-
18 минут назад, Nachinayushchiy сказал:
Na2SO3 + H2O2 → Na2SO4 + H2O
а количество реактивов и стадий не ограничено?Стадия одна: взято из цепочки реакций
-
Добрый день

Условие задачи: Найти объём выделившегося газа (0°C, 101,3 кПа), если 6,3 г сульфида натрия Na2S вступает в реакцию с 7,3 г хлороводородной кислоты HCl
Решение:
Напишем уравнение реакции
0,08 0,2. x
Na2S+2HCl=2NaCl+H2S
1моль 2моль. 1моль
n(Na2S)=m(Na2S)/M(Na2S)=6,3 г/78 г/моль=0,08 моль
n(HCl)=m(HCl)/M(HCl)=7,3 г/36,5 г/моль=0,2 моль
nэк(Na2S)=n(Na2S)*zэк(Na2S)=0,08*2=0,16 моль-экв
nэк(HCl)=0,2 моль-экв
HCl в избытке –> считаем по сульфиду натрия
n(H2S)=n(Na2S)=0,08 моль
V(H2S)=Vm*n(H2S)=22,4*0,08=1,792 л — ответ
Правильно решено?
-
Добрый день. Возможно ли получить сульфат натрия Na2SO4 из сернистой кислоты H2SO3? Какой реакцией?
-
Составить электронную и электронно-графическую формулу атома Германия Ge и Рения Re в возбужденном состоянии.
1) Германий
32Ge* [Ar]4s13d104p3
n=4 s↑_p↑_↑_↑_
2) Рений
75Re* [Xe]6s14f145d56p1
n=6 s↑_p↑_ __ __
Подскажите, правильно составлены формулы?
-
7 часов назад, M_GM сказал:
один
Скажите, пожалуйста, как получить(какую формулу нужно использовать)
-
Найти количество моль эквивалентов (nэк) CO(оксид углерода II), если известно: молярная масса = 28 г/моль; масса=14 г; кол-во в-ва=0.5 моль; объём газа (н.у.)=11.2 л; число мол-л=3.01*10^23
-
И разберись, где у тебя первая задача, где вторая
В обеих задачах количество вещества нужно найти по другой формуле: не ν=Vρω, а ν=Vρω/M.
-
1. Определите, какой объём 15%-ого раствора гидроксида калия с плотностью 1,13 г/мл потребуется для полной нейтрализации 20 мл 10%-ой соляной кислоты с плотностью 1,05 г/мл.
2. Определите, какую массу магния можно полностью растворить в 20 мл 10%-ого раствора серной кислоты с плотностью 1,07 г/мл.
Проверьте, правильно ли решено.
Решение 1 задачи:
1) ν(H2SO4)=2.14 моль
2) ν(MgSO4)=ν(H2SO4)=2.14 моль
3) ν(Mg)=ν(MgSO4)=2.14 моль
4)m(Mg)=51.36 г
Ответ: 51.36 г.
Решение 2 задачи:
1) ν(HCl)=2.26 моль
2) ν(KCl)=ν(HCl)=2.26 моль
3) ν(KOH)=ν(KCl)=2.26 моль
4) V(KOH р-н)=13 мл.
Ответ:13 мл.
-
Проверьте решение задач.
1.40 г оксида цинка восстановили избытком углерода. Определите массу образовавшегося металла, если выход продукта реакции равен 85%.
2.490 г 20%раствора серной кислоты было нейтрализовано гашеной известью Ca(OH)2, причем получилось 60.6 г сульфата кальция. Определить выход продукта в % к теоретическому.
3.Ацетилен получают взаимодействием карбида кальция с водой. Сколько граммов ацетилена получится, если израсходовано 68 г карбида кальция, содержащего 7% примесей и выход ацетилена составил 75% к теоретическому.
Решение:
№1.1)ν(ZnO)=0.494 моль
2)ν(Zn)=ν(ZnO)0.494 моль
3)mтеор.(Zn)=32 г
4)mпр.(Zn)=27.2г
Ответ:27.2.
№2.1)m(H2SO4)=98г
2)ν(H2SO4)=1 моль
3)mтеор.(CaSO4)=136 г
4)η(CaSO4)=45%
Ответ:45%.
№3.1)m(прим.)=4.76 г
2)m(CaC2)=63.24 г
3)mтеор.(C2H2)=26 г
4)mпр.(C2H2)=19.5 г
Ответ: 19.5.
-
Есть такая реакция? Галогеналкан+спирт
CH3-CHBr-CH3+CH3OH=CH3-CHOH-CH3+CH3Br
-
1. Оксид алюминия прореагировал с раствором серной кислоты объёмом 25 см3 (ρ=1,303 г/мл) и массовой долей кислоты 40%. Определить массу образовавшейся соли.
2. Вычислить объём газа, который образуется при взаимодействии цинка с 180 мл раствора соляной кислоты(ρ=1,108 г/мл) с массовой долей соляной кислоты 30%.
Проверьте решение.
Решение задачи №1:
1)ν(H2SO4)=Vρω/M=0,133(моль)
2)по уравнению ν(Al2(SO4)3)=0,133/3=0,044(моль)
3)m(Al2(SO4)3)=ν(Al2(SO4)3)*M(Al2(SO4)3)=15,048(г)
Ответ:15,048 г.
Решение задачи №2:
1) ν(HCl)=Vρω/M=1,639 (моль)
2)по уравнению ν(H2)=1,639/2=0,8195(моль)
3) V(H2)=Vm*ν(H2)=22,4*0,8195=18,3568(л)
Ответ: 18,3568 л.
-
Проверьте задачи
1. Вычислить объём этанола (плотностью 0.8 г/мл и массовой долей 80%) и объём воды, необходимый для приготовления 1000 мл 0,2-молярного спирта).
2. Вычислить массу хлорида натрия и объём воды,необходимый для приготовления 200 г 1-молярного раствора NaCl (плотность р-ра 1.15 г/мл).
3. Вычислите массу соляной кислоты и объём воды, необходимый для приготовления 300 мл 0.1-молярного р-ра (плотность раствора 1.28 г/мл).
1. m(в-ва)=c(в-ва)*M(в-ва)*V(р-ра)=9,2 г
V(в-ва)=m(в-ва)/(p(в-ва)*ω(в-ва))=14 мл
V(H2O)=V(р-ра)-V(в-ва)=986 мл
Ответ: 14 мл; 986 мл.
2. V(р-ра)=m(р-ра)/p(р-ра)=0.174 л
m(в-ва)=c(в-ва)*M(в-ва)*V(р-ра)=10,179 г
m(H2O)=m(р-ра)-m(в-ва)=189,82 г
V(H2O)=190 мл
Ответ: 10,179 г; 190 мл.
3. m(в-ва)=c(в-ва)*M(в-ва)*V(р-ра)=1,095 г
m(р-ра)=V(р-ра)*p(р-ра)=0,3*1280=384 г
m(H2O)=m(р-ра)-m(в-ва)=382,905 г
V(H2O)=383 мл
Ответ: 1,095 г; 383 мл.
-
- К 158 г 21 % раствора сахара добавили 25 г сахара. Вычислить массовую долю сахара в полученном растворе.
- Раствор массой 4300 г, содержащий NaCl массовой долей 23%, охладили, в результате чего выпал осадок массой 10 г. Вычислите массовую долю соли в полученном р-ре.
- Из 520 г раствора с массовой долей H2SO4 10 % выпариванием удалили 250 г H2O. Определите массовую долю к-ты в полученном р-ре.
- К 250 г 16% раствора CH3COOH добавили 225 г H2O. Вычислите массовую долю CH3COOH в полученном р-ре.
- Смешали 200 г раствора с массовой долей NaNO3 30 % и 30 г р-ра с массовой долей NaNO3 20%. Определить м.д. соли в полученном р-ре.
- В 200 мл р-ра содержится 17.4 г K2SO4. Вычислите молярную концентрацию соли в растворе.
Задача 1.
m(раств.в-ва)=m(р-ра)*ω(раств.в-ва)=158*0.21=33.18 г
ω'(раств.в-ва)=(33.18+25)/(158+25)=31.8(%)
Задача 2.
m(раств.в-ва)=m(р-ра)*ω(раств.в-ва)=4300*0.23=989 г
ω'(раств.в-ва)=(989-10)/(4300-10)=22.8%
Задача 3.
m(раств.в-ва)=520*0.1=52 г
ω'(раств.в-ва)=52/(520-250)=19.3%
Задача №4.
m(раств.в-ва)=250*0.16=40 г
ω'(раств.в-ва)=40/(250+225)=8.4%
Задача №5.
m' раств.в-ва=200*0,3=60 г
m'' раств.в-ва=30*0,2=6 г
ω''' (раств.в-ва)=(60+6)/(200+30)=28,7%
Задача 6
c=m/(M*ν)=17,4/(174*0,2)=5 моль/л.

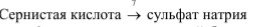
Задача на уравнение Фрейндлиха
в Решение заданий
Опубликовано
Текст задачи:
Рассчитайте адсорбированное количество уксусной кислоты в мг-экв/г, если при её адсорбции почвой равновесная концентрация равнялась 33,5 ммоль/л, константы уравнения Фрейндлиха K и 1/n соответственно равны 9,5 и 0,22.
Решение:
Уравнение Фрейндлиха:
x/m=K*C^(1/n)
Подставляя известные значения,получим
x/m=9,5*33,5^(0,22)≈20,57 (мг-экв/г)
Проверьте, правильно ли решена задача