
А007
-
Постов
34 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные А007
-
-
Все зависит от избытка/недостатка одного из реагентов, и в дело вмешивается растворимость веществ
Если каплю FeCl3 добавите к избытку раствора K2S,
то в растворе будет избыток сульфид-ионов,
которые будут связывать ионы железа в нерастворимый черный FeS
3K2S+2FeCl3=2FeS+S+6KCl
Но если каплю разбавленного K2S, добавите к избытку раствора FeCl3
то сульфид-ионы не успеют сделать своего черного дела,
т.к. все будут окислены до S:
K2S+2FeCl3=2FeCl2+2KCl+S?
Возможен и смешанный вариант, когда одновременно идет образование двух продуктов, т.к. все будет зависеть от того, с чем раньше встретится в растворе сульфид-ион - с ионом Fe(3+) и окислится, или с ионом Fe(2+) и уйдет в осадок FeS
В первой реакции осадков нет, так что правильным будет только первый вариант протекания реакции
В смысле в первой реакции осадков нет?
И возможны эти два варианта по отдельности?
-
Реакция:
KI+FeCl3=FeCl2+KCl+I2
Могут ли получаться продукты
KI+FeCl3=FeI2+KCl+I2?
И вот здесь
K2S+FeCl3=FeS+S+KCl
А почему не
K2S+FeCl3=FeCl2+KCl+S?
Как понять, когда в овр есть принцип ионного обмена, а когда нет?
Здесь вот например
KI+CuSO4=I2+CuI+K2SO4
-
Хомченко - Окислительно-восстановительные реакции (1989)
Бахметьева - Окислительно-восстановительные реакции (2005)
Кудрявцев - Составление химических уравнений (1991)
Спасибо огромное! )))
-
Добрый день! Подготовка к ЕГЭ по химии
Подскажите как научиться писать продукты реакции овр?
Я знаю,что есть схемы как изменяются,но там есть не всё
Можете дать полные схемы превращений,сайты с подробными написаниями продуктов овр или литературу?
Объясните логику решения,если можно)
Кроме манганатов,перманганатов,хроматов и дихроматов,здесь всё понятно)
А вот как с другими веществами,если нет ни соеденений марганца,ни хрома...
Спасибо заранее)))
-
 1
1
-
-
Лучше учебник почитать. Здесь в две строчки не напишут "полные схемы"
Подскажите какой)
-
Добрый день! Подготовка к ЕГЭ по химии
Подскажите как научиться писать продукты реакции овр?
Я знаю,что есть схемы как изменяются,но не всё там есть
Можете дать полные схемы превращений,сайты с подробными написаниями продуктов овр или литературу?
Спасибо заранее)))
-
Что бы "получился" никелат 3,никелат 4,так и надо же писать их оксиды, а не NiONi2O3
NiO2
А такие бывают?
Я их не видел
Что бы "получился" никелат 3,никелат 4,так и надо же писать их оксиды, а не NiONi2O3NiO2
Вы уверены про NiO2?
-
-
Но последние 2 реакции не уравниваются
-
Так же как и никелаты.
Напишите реакции
-
При сплавлении.
Сомнительно, что существуют IV
Напишите реакции
-
Когда образуются никелаты (II),никелаты (III),никелаты (IV)
Реакция с KOH и К2О
Заранее спасибо)))
И никто не знает...
-
Когда образуются кобальтаты (II),кобальтаты (III),кобальтаты (IV)
Реакция с NaOH и Na2O
Спасибо заранее)))
-
-
-
-
Ну. А там не азотная? Реакции 1) и 2) ко второму заданию
Понял. Спасибо)))
-
3Mg(NO3)2+2H3PO4=Mg3(PO4)2+6HNO3
1) 2Na3PO4+3MgSO4=3Na2SO4+Mg3(PO4)2
2) Mg3(PO4)2+6HF=2H3PO4+3MgF2
Из Mg(NO3)2 надо получить азотную кислоту!!!
-
-
Решите цепочку
Mg(NO3)2=>HNO3
Na3PO4=>H3PO4
-
Да сколько угодно! Сплавляйте оксид кальция с NaOH - и хрен там получится фаза химического соединения, будет просто сплав того и сего.
Спасибо,коллега)))
-
Это бывает. Просто в воде гидроксид никеля не даёт никелатов, поскольку относительно воды - это довольно сильное основание. А вот при сплавлении - там уже воды практически нет, и отношения совсем другие, там оксид никеля образует фазу, отвечающую химическому соединению, состав которого отвечает именно никелату.
Всё дело - в растворителе. Или он есть, или его нет. Ключевое слово тут - сплавление.
Спасибо огромное!
А то я думал,что если любые два вещкства сплавить реакция пойдет
Это бывает. Просто в воде гидроксид никеля не даёт никелатов, поскольку относительно воды - это довольно сильное основание. А вот при сплавлении - там уже воды практически нет, и отношения совсем другие, там оксид никеля образует фазу, отвечающую химическому соединению, состав которого отвечает именно никелату.Всё дело - в растворителе. Или он есть, или его нет. Ключевое слово тут - сплавление.
А есть такие реакции,которые при сплавлении не идут?
-
-
Оксиды с низкими степенями окисления не очень любят проявлять амфотерные свойства .Na4CoO3 - скорее ошибка или что-то типа Na2О*Na2CoO2 или Комплексное соединение Na4[CoO3] в котором один из кислородов с центральным атомом связан только донорно-акцеторно
Это не ошибка и некомплексный анион,Na4CoO3-кобальтат (II) натрия,где ион CoO34-
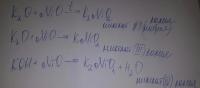
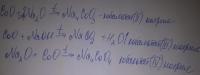
KI+FeCl3=FeCl2+KCl+I2
в Решение заданий
Опубликовано
А почему тогда реакция идет
K2S+FeCl3=KCl+FeS+S
А не так
K2S+FeCl3=KCl+FeCl2+S?
И что значит выпадают из раствора?
И как себя проверить,что продукты получились верными?
Спасибо за разъяснение