-
Постов
49 -
Зарегистрирован
-
Посещение
-
Победитель дней
1
Тип контента
Профили
Форумы
События
Сообщения, опубликованные XummY
-
-
9 минут назад, M_GM сказал:
Еще раз, что такое C0? - "C0 (начальная конц. исходных веществ)"
- почему она должна быть разной для одного эксперимента, где смешали исходные вещества,
и через заданные промежутки времени отбирают пробы и определяют текущую концентрацию?
Тогда почему здесь вычисляют C0 ? Из за увеличения объема кислорода?
-
13 минут назад, M_GM сказал:
И что тебе мешает для своей задачи просчитать и составить табличку
как по ссылке https://dropmefiles.com/pYD60,считая, что C0 - есть величина постоянная, равная 2.5 моль/л?
Тебе даже (C0 - х) считать не надо, тебе сразу дана концентрация исходного вещества (аналог CH3Br) через указанные промежутки времени от t0
на вашему C0 будет постоянной и равной 2,5 для любого t? -
9 минут назад, M_GM сказал:
Вот тоже (из методички)
https://dropmefiles.com/xdw00
https://dropmefiles.com/pYD60
Что за ерунда? -
23 минуты назад, M_GM сказал:
Так у тебя есть время t=0 - почему бы не считать,
что соотв. концентрация 2.5 моль/л и есть С0?
хорошо, но как рассчитать для каждого момента времени C0 ? -
-
2 минуты назад, M_GM сказал:
Так у тебя есть время t=0 - почему бы не считать,
что соотв. концентрация 2.5 моль/л и есть С0?
логично, но давление по другому рассчитывают -
Здравствуйте, уважаемые коллеги!
Помогите пожалуйста советом
Для данной реакции 2H2O2 → 2H2O + O2 необходимо определить порядок n и константу скорости 3 методами: графическим, подстановки и Вант Гоффа.Исходные данные:
время t (0; 10; 20; 30; 40 мин)
концентрация C(H2O2) (2.5; 0,90; 0,32; 0,12; 0,04 моль/л) - конц. исходных веществ к данному моменту времени t.
Для определения константы скорости реакции k2=1/t(1/C - 1/C0) (и не только k2) необходимо знать значение C0 (начальная конц. исходных веществ)
Помогите пожалуйста определить эту C0 для каждого момента времени t (каким методом она определяется)?
Спасибо! -
2 часа назад, M_GM сказал:
Если Кс = [В]2/([А]2[Б]3) то размерность Кс = (моль/л)-3 или (моль/м3)-3
Для Кр соответственно Па-3 или кПа-3
спасибо Вам, товарищ!
-
Здравствуйте!
Подскажите пожалуйста верно ли определена размерность Kp и Kc
Условие задачи:
Газообразные вещества А и Б реагируют с образованием газообразного вещества В (2А+3Б=2В).
1. Выразите константы равновесия Kp и Kc через равновесное количество вещества В, равное x, если исходные вещества А и Б взяты в стехиометрических количествах при общем давлении в системе P и температуре T, К.
2. Рассчитайте Kp и Kc при 300 К, если Р = 7,5·104 Па, x = 0,45.
3. Вычислите равновесное количество вещества В при давлении в системе, равном 3·104 Па и Т = 300 К.
4. Рассчитайте степень превращения веществ А и Б при T = 300 К.
-
-
-
Доброго времени суток, товарищи!
Имеется задача следующего типа:
Платье, в котором вы вымокли, впитало 1 кг воды и холодный ветер высушил его. Какое количество потерянной теплоты необходимо возместить организму? Сколько глюкозы нужно потребить, чтобы восполнить эту потерю? Предположим, что ваш организм не возместил потерю теплоты. Какова будет ваша температура после высыхания одежды (предположите, что теплоемкость вашего тела равна теплоемкости воды).
Буду ли я прав, если решу её подобным образом? Проверьте пожалуйста, напишите замечания, чтоб исправить ошибки.
Дано:
ΔH (H2O) = -285.8 (кДж/моль) - Ж
ΔH (H2O) = -241.8 (кДж/моль) - Г
ΔH (CO2) = -393.5 (кДж/моль) - Г
ΔH (C6H12O6) = -1264.8 (кДж/моль) - ТВ
Mr (H2O) = 18 (г/моль)
Mr (C6H12O6) = 180.1 (г/моль)
Масса тела = 75 кг
Начальная температура тела 36.6°C
Решение:
1. Определим Т.Э. фазового перехода H2O(ж) → H2O(г)
ΔHф.п.= ΔH (H2O)г - ΔH (H2O)ж = 44 (кДж/моль)
2. Рассчитаем на 1 кг воды:
ΔHф.п.= (44*1000)/18 = 2444.4 (кДж)3. Определим массу глюкозы, которую необходимо потребить:
Т.Э. окисления глюкозы = C6H12O6 + 6O2 → 6CO2(г) + 6H2O(г) ---- (ж)
ΔH = 6ΔH (CO2)г + 6ΔH (H2O)г - ΔH (C6H12O6)тв = -2547.8 (кДж)
Масса глюкозы = (2444.4*180.)/(-2547.8) = 172.7 (гр)
4. Определим изменение температуры:
ΔT = Q/(c*m) = 2444.4/(4.2*75) = 7,7 °C
Температура после высыхания одежды (если организм не возместил потерю теплоты) = 36.6 - 7.7 = 28.9 °C -
6 минут назад, M_GM сказал:
Ну вот, к чему бы им сходиться!
Кстати заметили, что в вашем источнике теплота сгорания вообще 2868,1 кДЖ/моль?
Возможно, правда это для газа...
Так что посчитайте по данным методички и не парьтесь.
Нестыковки в т.д. данных нередки.
Спасибо, приму к сведению. В других источниках значение примерно то же -
7 минут назад, M_GM сказал:
В методичках часто встречаются нестыковки ... А значение "стандартная энтальпия образования пиридина = 100,2 кДж/моль" - откуда?
Здесь нашел http://chemister.ru/Database/properties.php?dbid=1&id=645
Можно ли доверять этому источнику? -
43 минуты назад, M_GM сказал:
Особенно дико, что реакция эндотермическая ...
Т.е., что вещество т.д. неустойчиво ...
Посчитано то правильно, но:
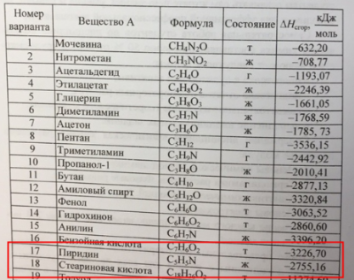
В тексте: ΔHсгор. = -2255,16 кДж/моль
Используется: ΔHсгор. = -2755,16 кДж/моль
В химической энциклопедии ΔHсгор. = -2783 кДж/моль
Если использовать последнюю величину, то получим -101,035 кДж/моль ...

Реакция экзотермическая, верно..... Исходные данные использовались из таблицы методички, в описании ошибку еще допустил
-
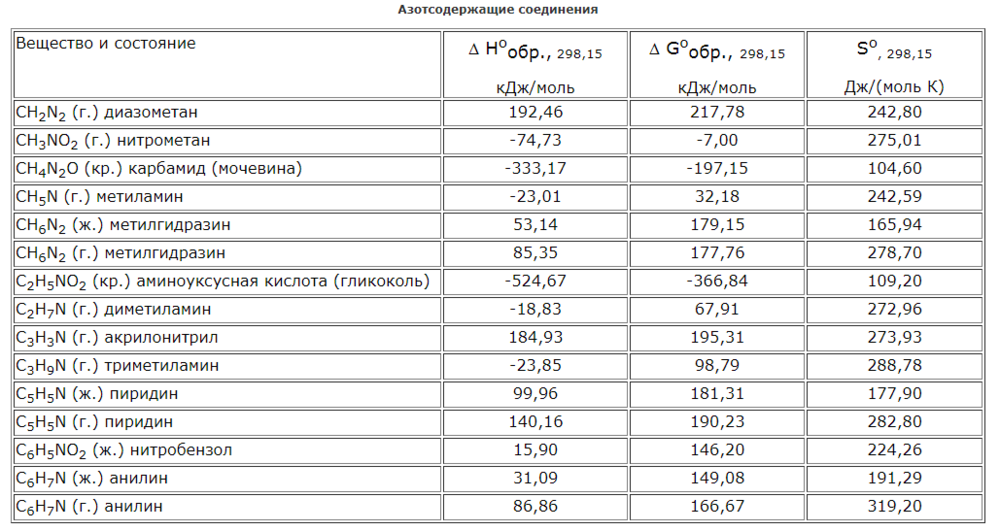
Здравствуйте, товарищи!

Помогите пожалуйста в проверке решения задания (приложение). Присутствует сомнение, т.к. стандартная энтальпия образования пиридина = 100,2 кДж/моль, а Т.Э. образования = -73 кДж/моль.
Условие: вычислите тепловой эффект образования пиридина из простых веществ при температуре 298 К и стандартном давлении, если известна его энтальпия сгорания (ΔHсгор. = -2255,16 кДж/моль) при этой температуре и стандартном давлении. При вычислении следует принять, что конечные продукты сгорания СО2(г), Н2О(ж), N2(г).
-
4 минуты назад, M_GM сказал:
Годится, можно поставить знак равенства:
5C + 5/2 H2 + 1/2N2 = C5H5N ; ΔНобр
Благодарю!
-
 1
1
-
-
3 минуты назад, M_GM сказал:
Чтобы рассчитывать энтальпию образования используют
уравнение реакции образования из простых веществ.Значит для получения пиридина С5H5N надо взять простые вещества углерод, водород и азот:
С + Н2 + N2 --> С5H5N
и расставляйте коэфициенты
5C + 5/2 H2 + 1/2N2 → C5H5N ?
-
 1
1
-
-
Здравствуйте, уважаемые форумчане!
Помогите пожалуйста составить термохимическое уравнение реакции образования пиридина (C2H5N) для решения задачи по физической химии на вычисление теплового эффекта образования пиридина (C2H5N).Уравнение реакции сгорания пиридина составил следующим образом: С5H5N + 25/4 O2 → 5CO2 (г) + 5/2H2O (ж) + 1/2N2 (г)
-
 1
1
-
-
-
Здравствуйте!
Пожалуйста, помогите составить уравнение реакции получения дибутилового эфира фталевой кислоты (С16Н22О4). Исходные вещества: бутиловый спирт, фталевый ангидрид и конц. серная кислота.
Спасибо!
-
Товарищи, разрешите ещё пару вопросов.
1) Быть может вспомните уравнение реакции гидрохинона и хлорида железа (3)? Что с окрашиванием раствора? Зелёный переходит в жёлтый?
2) Какую окраску даёт пирогаллол в связи с тем же хлоридом железа (3)?
Спасибо! -
Да, верно, спасибо Вам!
-




.thumb.jpg.4c25ad5bf4d61ce62a7a1fb9912da8bf.jpg)

Определение кинетических характеристик простых односторонних реакций
в Решение заданий
Опубликовано
Всё, я вас понял, невнимательность подводит!
Спасибо, разобрался!