
Влад махин супер
-
Постов
38 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Влад махин супер
-
-
Рассчитайте рН в 0,025М водном растворе HOOC-COOH ((pKa1 = 1,19, pKa2 = 4,3).
по какой тут ступени?
илм по две сразу и как определить?
-
Первое решение верное, хотя хотелось бы при проверке иметь больше пояснений.
Второе - неверное, начиная уже со второго расчета. Почему 32 г умножается на 0,4, хотя 32 г это масса меди+кислорода и массовая доля нитрата меди в растворе не имеет к 32 никакого отношения? почему считается, что при этом найдена масса нитрата меди? Как масса раствора уменьшилась на 32 г, если меди выделилось грубо 4 г и кислорода 1 г ? Почему при расчете массы итогового раствора не учитывается, что масса первого раствора уменьшилась на 32 г?
Все эти вопросы показывают, что человек, решая задачу, толком не понимает, что он делает, ни ее условия, ни смысла получаемых чисел.
И близко-похожий результат его сумбурных расчетов не делает решение верным.
ПОЧЕМУ 32 ЭТО МАССА МЕДИ И КИСЛОРОДА?!?!
-
. Ну просто там же масса раствора уменьшилась на 32 ,а было 282 г раствора. Ну и 282-32Первое решение верное, хотя хотелось бы при проверке иметь больше пояснений.
Второе - неверное, начиная уже со второго расчета. Почему 32 г умножается на 0,4, хотя 32 г это масса меди+кислорода и массовая доля нитрата меди в растворе не имеет к 32 никакого отношения? почему считается, что при этом найдена масса нитрата меди? Как масса раствора уменьшилась на 32 г, если меди выделилось грубо 4 г и кислорода 1 г ? Почему при расчете массы итогового раствора не учитывается, что масса первого раствора уменьшилась на 32 г?
Все эти вопросы показывают, что человек, решая задачу, толком не понимает, что он делает, ни ее условия, ни смысла получаемых чисел.
И близко-похожий результат его сумбурных расчетов не делает решение верным.
-
Для проведения электролиза взяли 282г 40% раствора нитрата меди. После того ,как масса раствора уменьшилась на 32 г , процесс остановили.К образовавшемуся раствору добавили 140 г 40% раствора NaOH
Определите массовую долю щелочи в полученном растворе. ПОЧЕМУ НЕЛЬЗЯ РЕШИТЬ , КАК НА 2 И 3 ФОТКЕ? Объясните пожалуйста
-
-
Все верно. Количество моль углерода в соединении равно количеству моль CO2, т.е. 0,1 моль, а количество моль хлора равно количеству моль HCl, т.е. 0,04 моль. В соответствии с формулой соединения количества моль углерода и хлора относятся как n к 2, отсюда находим n = 5, т.е. соединение имеет формулу C5H8Cl2. Далее надо нарисовать возможные изомеры и в соответствии с условием выбрать тот, который ему удовлетворяет
Почему количество моль С и Cl относятся как n к 2 , если из формулы получается , что С= 0,1 а Cl = 0.08
-
-
С2H4O это типа уксусный альдегид? если так то:С2H4O+ KMnO4 + KOH = CH3COOK + MnO2 + H2O
Почему у тебя марганец в щелочной среде окислился до Mno2 ????? ДОЛЖЕН ДО k2mno4
-
Акриловая кислота + kmno4 + h2o= ch2oh-choh-cooh
Она будет образовывать только это органическое вещество или ещё какие-нибудь,например, акрилат калия?
-
-
Для начала было бы неплохо составить уравнение реакции окисления алкенов (с использованием их общей формулы) водным раствором
перманганата калия по Вагнеру.
. С уважением
Вот
Для начала было бы неплохо составить уравнение реакции окисления алкенов (с использованием их общей формулы) водным раствором перманганата калия по Вагнеру.
. С уважением
Вот даже составил уравнение только получается отрицательное значение
-
-
Смесь циклобутана и водорода с плотностью по водороду 5,5 пропустили над нагретым катализатором. По окончании реакции плотность полученной газовой смеси по воздуху составила 7,8% от исходной плотности. Вычислите выход продукта реакции? ПОМОГИТЕ ПОЖАЛУЙСТА, Я правда не понимаю , как решать!! Объясните
-
K2FeO4 + h2SO4 + Cu2O =
NaFeO2 + NaNO3 + NaCO3=
Помогите пожалуйста!!
-
-
вроде C6H4OH-CH2-CH2-CH2-CH3
Что-то вообще не получается
-
Во первых формула неправильная, во вторых, а что помешает этим веществам опять вступить в реакцию?
Вы хоть читайте, что вам пишут.
Формула правильная , а просто другой комплекс
Во первых формула неправильная, во вторых, а что помешает этим веществам опять вступить в реакцию?Вы хоть читайте, что вам пишут.
Есть такая формула
Формула правильная , а просто другой комплекс
-
Можно и так, только тогда вы не получаете требуемый NaAlO2
А вот так можно? Первая K3[Al(OH)6]= AlOH3 + 3KOH ?
-
-
Вы же супер, да и что тут понимать?
Попробуйте написать сами, а мы уже проверим.
Пожалуйста , я не супервайзер
Вторая вот так ? Na3[Al(OH)6]=Na3AlO3 + 3H2O
-
. В таком случае можно и без осаждения гидроокиси алюминия обойтись, по-моему. Просто прокаливать гексагидроксоалюминат с эквимольным количеством оксида алюминия.
. С уважением
Напишите пожалуйста реакции, а то я не понял
-
Два случая:
В первом, чтобы получилось al(OH)3
Во втором - naalo2
Помогите пожалуйста
-
А дальше не совсем просто, т.к. сернистый газ со щелочью может давать разные соли.
В зависимости от избытка-недостатка
Получает что количество оставшегося NaOh = 0.9-1.2
А дальше не совсем просто, т.к. сернистый газ со щелочью может давать разные соли.В зависимости от избытка-недостатка
Так что пиши уравнения реакции и считай моли веществ.
Помогите
-







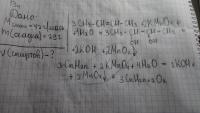
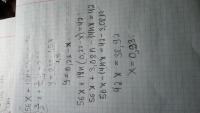


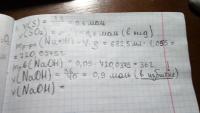

Задача
в Решение заданий
Опубликовано
Вычислите количество теплоты, которое выделится при взрыве смеси, содержащей 5,6л водорода и 22,4л кислорода (объемы измерены при нормальных условиях)