-
Постов
17 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные АИльяВ
-
-
-
-
-
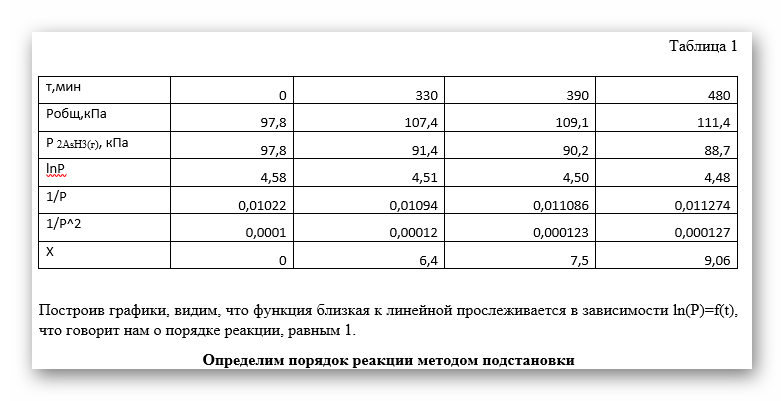
Здравствуйте, нужно определить порядок реакции
-методом подстановки
-графическим методом
-методом Вант-Гоффа
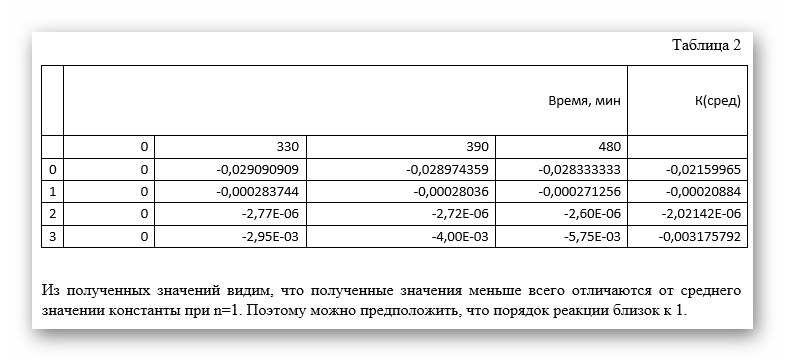
Первые 2 метода я сделал, но не уверен что сделал правильный вывод. А вот метод Вант-Гоффа рассчитать не могу. Тк не понимаю что откуда берется.
В методе Вант-Гоффа я понял что нужно рассчитать, вот эти данные. Но я не знаю по каким формулам.

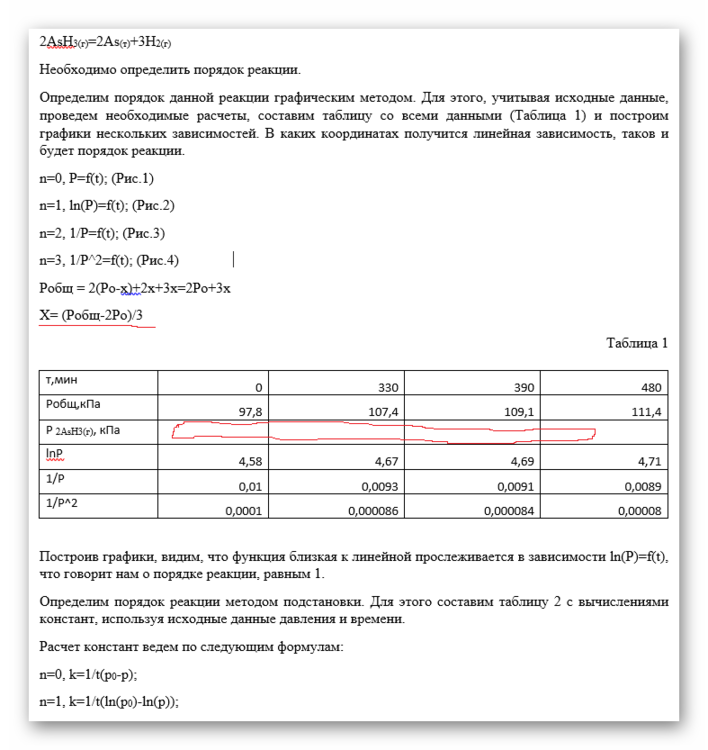
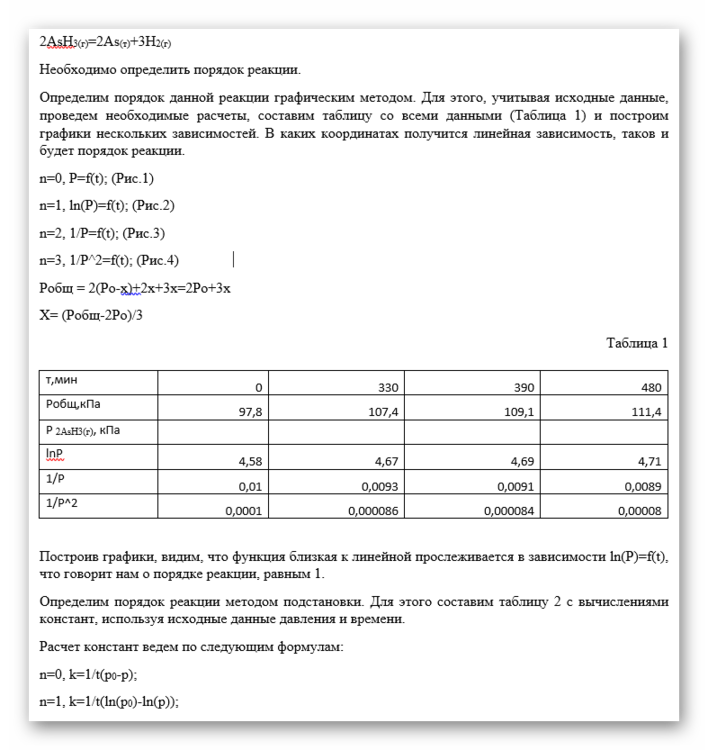
Вот само задание:

-
6 часов назад, M_GM сказал:
Какого вещества? У тебя три вещества в системе ...
Поскольку в показанном тобой листочке ничего про Х не говорится - остается только гадать
На мой взгляд, формула для расчета Х и предыдущая содержит некоторые ошибки
Если считать, что Х - парциальное давление мышьяка, я написал бы эти формулы так:
Pобщ = PAsН3 + PAs + PН2 =(Ро-х) + х + 1,5х = Ро + 1,5х
Х= (Pобщ - Ро)/1,5
Тогда в начальный момент времени t=to, Pобщ =Ро, X=0 , PAsН3 = (Ро-х) = 97,8 кПа
А вот в для t=330, , X=(107,4-97,8)/1,5=9,6/1,5 = 6,4
PAsН3 = (Ро-х) = 97,8 - 6,4 = 91,4 кПа и т.д.
Но вторая строчка в таблице не понятно к чему предназначена, далее не используется.
Обозначение "P2AsН3" на мой взгляд некая чушь. "PAsН3" - понятно, парциальное давление арсина
Что такое "P2AsН3" и чем оно отличается от "PAsН3" - хорошо бы спросить у автора методички
Понял, у преподавателя уточню, спасибо большое
-
2 часа назад, M_GM сказал:
p0 - это давление в момент времени t0 ( 97,8 в табл. 6)
Оно должно быть измерено в ходе эксперимента
Или расcчитано по pV=nRT, если известны V,T, n из данных по загрузке системы веществом
Понял спасибо, так и думал. Тоесть когда я рассчитаю вот этот Х, то он и будет давлением вещества ?
-
-
Кто нибудь может проверить ?
-
Всем привет
 , можете проверить решение ? Тему не очень понимаю.
, можете проверить решение ? Тему не очень понимаю.
Газообразные вещества А и Б реагируют с образованием газообразного вещества В (А+Б=1/2В).
Выполните следующие задания для данной реакции:
1. Выразите константы равновесия KP и KC через равновесное количество вещества В, равное x, если исходные вещества А и Б взяты в стехиометрических количествах при общем давлении в системе P и температуре T, К.
2. Рассчитайте KP и KC при 300 К, если Р = 7,5·104 Па, x = 0,45.
3. Вычислите равновесное количество вещества С при давлении в системе, равном 3·104 Па и температуре 300 К.
4. Рассчитайте степень превращения веществ А и Б при T = 300 К.
Еще часть решения
-
10 часов назад, M_GM сказал:
Мочевина сгорает в кислороде, поэтому в левую часть уравнения надо добавить кислород с нужным коэффициентом
Для расчета вы используете тепловые эффекты (Q), поэтому сначала получаете теплоту образования.
Теплоту сгорания азота здесь нет нужды учитывать, т.к. азот при сжигании мочевины выделяется в виде простого вещества. ("не сгорает")
Поэтому вместо ΔН = ΔН(С) + 2Δ Н(Н2) + Δ Н(N2) - Δ Н((NH2)2CO)
лучше записать формулу Qобр = Qсг(С) + 2Qсг(Н2) - Qсг((NH2)2CO)
ТогдаQ обр = (393,51 + 2·285,83 – 632,20) · 103 = 332,97 · 103 Дж/моль
А вот потом вы можете найти ΔН = -Q обр = -332,97 · 103 Дж/моль.
Но можно это и не делать, так как вопрос задачи "Вычислите тепловой эффект"
Проверка знаков: мочевина - устойчивое вещество.
У устойчивых веществ теплота образования положительна
(энтальпия образования отрицательна)Наверное есть смысл выражать результаты в кДж/моль,
тем более, что данные вы подставляете в кДж/моль
Все понял
 , спасибо большое. Осталось только запомнить
, спасибо большое. Осталось только запомнить
-
Здравствуйте уважаемые знатоки
 . Помогите, пожалуйста, решить (проверить) задание:
. Помогите, пожалуйста, решить (проверить) задание:
Вычислите тепловой эффект образования вещества А из простых веществ при температуре 298 К и стандартном давлении, если известна его энтальпия сгорания при этой температуре и стандартном давлении (табл. 1). При вычислении следует принять, что конечные продукты сгорания СО2(г), Н2О(ж), N2(г).
Теплоты сгорания простых веществ указаны в следующих уравнениях:
С(графит) + О2(г) = СО2(г) + 393,51
 ;
;
Н2(г) +
 О2(г) = Н2О(ж) + 285,83
О2(г) = Н2О(ж) + 285,83  .
.
Таблица 1:
Мочевина (СН4N2О); состояние твердое; ∆Нсгор,
 = –632,20
= –632,20
Решение:
(NH2)2CO (тв.) = N2
(г.) + CO2 (г.) + 2H2O (ж.)
ΔН = ΔН(С) + 2Δ Н(Н2) + Δ Н(N2) - Δ Н((NH2)2CO);
ΔН = (393,51 + 2·285,83 + 0 – 632,20) · 103 = 332,97 · 103 Дж/моль.
Q = - ΔН = -332,97 · 103 Дж/моль.
Мне кажется со знаками что то не то, и не уверен на счет энтальпии сгорания азота
Я жду...



-
 2
2
-
-
На аноде возможно окисление кислорода из воды, или бромид-ионов до свободного брома. Найдите их потенциалы, сравните и сделайте вывод, какой процесс протекает, и что там получается.
А уж потом считайте массу
А почему в схеме электролиза все для натрия написано? Хотя ранее сказано, что на катоде натрий не при чем?
А на аноде вообще, какой натрий? На анод идут анионы.
Понял, спасибо, все сделаю
-
Доброго времени суток, дали задание,
 ,
,  ,
,  ,
,уверен для вас оно будет не сложным, но у меня такого опыта не имеется и хотел бы попросить проверить, 1-й пункт правильный уже + стоит, а вот анодный процесс не правильный и еще надо было найти массу:
Наверно еще массу кислорода надо найти, я сейчас найду не не буду фото вставлять
-
Ну, мономолекулярный AlBr3 у Вас должен быть плоским треугольником, раз он sp2-гибридный и неполярный.
А что касается гибридизации брома в HBr, то здесь вопрос интересный. Я всегда думал, что в галогеноводородах галоген sp3-гибридный, также как атомы неметаллов в изоэлектронных воде, аммиаке, фосфине, сероводороде. Во всяком случае, в ониевых катионах типа H2Br+ галоген точно sp3-гибридный. С другой стороны, в учебниках при описании связей H-Hal рисуют просто p-орбиталь:
http://alnam.ru/book_chem.php?id=121 (по этой ссылке кликните на стр. 338)
В другом месте говорят, что
В молекуле HCl также имеется некоторая (!) sp3-гибридизация атома хлора, и поэтому три неподеленные электронные пары в атоме хлора оказываются равноценными.
http://window.edu.ru/catalog/pdf2txt/646/29646/12859?p_page=26
Для образования связи здесь гибридизация не нужна. Хватит ли сил отталкивания между неподеленными электронными парами для поддержания sp3 гибридного состояния - вот вопрос! Теоретически, конечно, может существовать любая суперпозиция между негибридизованными и sp3-гибридными орбиталями.
Я несколько озадачен.
Хочу еще раз сказать спасибо
 , я сдал задание, учитель проверил и сказал что все правильно, вы были правы на счет AlBr3, что касается HBr я глянул ссылки и решил ничего не исправлять, т. к. нет точного ответа
, я сдал задание, учитель проверил и сказал что все правильно, вы были правы на счет AlBr3, что касается HBr я глянул ссылки и решил ничего не исправлять, т. к. нет точного ответа-
 1
1
-
-
Ну, мономолекулярный AlBr3 у Вас должен быть плоским треугольником, раз он sp2-гибридный и неполярный.
А что касается гибридизации брома в HBr, то здесь вопрос интересный. Я всегда думал, что в галогеноводородах галоген sp3-гибридный, также как атомы неметаллов в изоэлектронных воде, аммиаке, фосфине, сероводороде. Во всяком случае, в ониевых катионах типа H2Br+ галоген точно sp3-гибридный. С другой стороны, в учебниках при описании связей H-Hal рисуют просто p-орбиталь:
http://alnam.ru/book_chem.php?id=121 (по этой ссылке кликните на стр. 338)
В другом месте говорят, что
В молекуле HCl также имеется некоторая (!) sp3-гибридизация атома хлора, и поэтому три неподеленные электронные пары в атоме хлора оказываются равноценными.
http://window.edu.ru/catalog/pdf2txt/646/29646/12859?p_page=26
Для образования связи здесь гибридизация не нужна. Хватит ли сил отталкивания между неподеленными электронными парами для поддержания sp3 гибридного состояния - вот вопрос! Теоретически, конечно, может существовать любая суперпозиция между негибридизованными и sp3-гибридными орбиталями.
Я несколько озадачен.
Спасибо большое
 , сейчас почитаю про HBr, во вторник химия будет, учитель проверит и если что, то я напишу
, сейчас почитаю про HBr, во вторник химия будет, учитель проверит и если что, то я напишу -
Товарищи, здравствуйте!
 Задача кажется не очень сложная, но есть сомнения . Посмотрите пожалуйста решение, может чего заметите, может чего исправить нужно.
Задача кажется не очень сложная, но есть сомнения . Посмотрите пожалуйста решение, может чего заметите, может чего исправить нужно.Условие задачи:
Определите характер химической связи между атомами в молекулах HBr и AlBr3. Укажите возможный тип гибридизации орбиталей центрального атома, наличие σ- и π-связей. Покажите пространственную структуру молекул. Полярны ли связь в молекулах и молекулы в целом? Определить разность электроотрицательности.Спасибо!-
 1
1
-












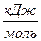 ;
;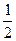 О2(г) = Н2О(ж) + 285,83
О2(г) = Н2О(ж) + 285,83 








Задача про материальные и тепловые расчеты
в Решение заданий
Опубликовано · Изменено пользователем АИльяВ
Доброго времени суток, есть задача, я вроде начал её решать, но она какая то не много не такая как мы делали. Звучит глупо, но факт есть факт.
Задача:
Для получения полифосфата натрия (NaPO3)n в качестве сырья используют 60%-ный раствор NaH2PO4. Этот раствор при постепенном нагревании в печи до 700оС испаряется, а затем происходит реакция дегидратации:
NaH2PO4 = NaPO3 + H2O
Провести материальные и тепловые расчеты на 1000 кг сырья.
Решение:
Молекулярная масса всех веществ:
NaH2PO4 = 119,977
NaPO3 = 101,961
H2O = 18,015
1. Исходное сырьё 1000 кг 60%-ный раствор NaH2PO4, следовательно
Сухого в-ва NaH2PO4 = 600 кг
Жидкого в-ва H2O = 400 кг.
А далее что делать вообще не пойму. Решали на паре одну большую задачу для примера и все. Может примеры есть, хотябы последовательность глянуть. А может у кого уже есть решение данной задачи ), но мне бы все равно понять что к чему.