-
Постов
27 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные привет всем
-
-
-
да ладно ты чего обиделся

-
я имел ввиду - графит и оксиды марганца
а ты и не понял

да ничего просто не в том порядке записал
но больше всего диоксида марганца
-
теоретически всё возможно
а на практике ...
-
-
прилил туда уксус прореагировало но цвет не изменился - черно-коричневый
выделился газ хотя
запах кислый отдаёт металлом
2MnO2 + 4CH3COOH = 2Mn(CH3COO)2 -светло-розовый + 2H2O + O2
добавил гидрокарбонат натрия (но он уже побывал в горяч воде-карбонат)
должен был выпасть осадок но нет - прозрачная жидкость с примесями углерода
а реакция была- газ выделился
вода же была горячей при растворении гидрокарбоната натрия а после (при реакции) остыла
-
 всё сходиться осталось придумать как осуществить
всё сходиться осталось придумать как осуществить -

2NaHCO3+MnO=MnCO3+Na2CO3+H2O
при каких условиях протекает
-
а можно ли получить из Mn2O3 получить соль в которой марганец в роли основания (но скорее всего марганец будет амфотерный
есть смесь оксидов марганца как бы их в одну степень окисления подогнать
-
а почему?
у марганца и не такие степени есть
-
можете ссылку дать на полную информ на это вещ-во
-
-
что будет если к смеси кислот добавить аммиак (или аммиачный раствор) например к HCl и HNO3 - взял по различаю присоединения водорода (к кислороду или галогену) или добавить к смеси HCl и HBr - по силе
как кажется образуется обе соли ( в первой смеси )
но нет ли здесь алгоритма - чего больше образуется
-
-
может кто знает хорошие( более полные) - таблицы растворимости ограники
-
почему аддукт похож на аддут
или это только написание
-
-
а как же происходит реакция в безвоздушной среде
-
всё ясно
но а всё таки какой же тогда состав зелёнки
-
значит всё таки более менее безопасна(реакция)
-
C27H34N2O4S(Зелёнка)= ...
она имеет свойство разлагаться на свету, а что же образуется
-
В учебном задании, где требуется нарисовать графическую формулу соли, будет вполне достаточно заменить в структурной формуле щавелевой кислоты атомы Н на Na. В действительности же, в оксалат-ионе С2О42- все связи между С и О являются равноценными, то есть, электронная плотность на них распределяется равномерно. Не вдаваясь в квантовомеханические рассуждения, просто примите на веру, что это энергетически наиболее выгодная структура. Такое положение дел вовсе не является чем-то из ряда вон выходящим, наоборот, практически все анионы кислородных кислот (CO32-, NO3-, SO42-, PO43- и т. д.) имеют такое же строение. Делокализация электронов графически может изображаться различными способами, посмотрите здесь на примере карбонат-иона СО32-.
При реакции с гидрокарбонатом натрия (или с нормальным карбонатом - без разницы) щавелевая кислота, как более сильная, вытесняет угольную кислоту из её соли, образуя оксалат натрия. Угольная кислота в свободном состоянии очень неустойчива и немедленно разлагается на углекислый газ и воду.
я почитал и понял специфику этих связей
всего вам хорошего
-
а как возможна такая связь углерода с кислородом
 заместить H на Na
заместить H на Naспасибо
а как проводится реакция h2c2o4 + 2nahco3 = Na2C2O4+H2O+CO2
-
2HCOONa→ (COO)2Na2 + H20 как эта реакция происходит
(COO)2Na2 и что это и какая у него структурная формула


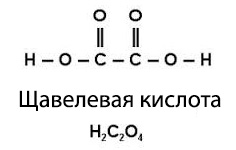 заместить H на Na
заместить H на Na
срочно! взял смесь оксидов марганца и графита
в Решение заданий
Опубликовано
ты сам болван
я не только кислород добывал (взял бы лучше марганцовку или перекись с тем же диоксидом марганца или электролизер )
просто хотел получить ещё соли марганца из его оксида без посредственных соединений
да это всё из батарейки
чего добру пропадать
планету не хочется загрязнять, а пункты сдачи батареек поблизости я не знаю
щёлочи там не было
я уже сам понял что опыт не удался из-за того что были примеси цинка и степень окисления у всех оксидов марганца была разной - просто чудилось что - что надо прореагирует а всё остальное останется в осадке или в процессе отойдёт да нет же) всё прореагировало
всё тема закрыта
спасибо конечно
а какая разница формула - она куда понятней
а если бы я написал что взял все реактивы в батарейке кто бы помог решить?