
andrey1999
-
Постов
88 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные andrey1999
-
-
Только что, Аль де Баран сказал:
А, ну так ты прикинулся валенком и проверяешь дяденек на вшивость. Мы-то уравняем, что угодно, только впредь пиши в топике что-нибудь за себя, тут я согласен с мнением M_GM.
1 курс, извиняйте, неопытен. Темы изучаю дома, так что и не думал, что все так сильно зависит от того, что должно быть в продуктах реакции.
-
18 часов назад, Аль де Баран сказал:
H2O2 - 2e = O2 + 2H+ (*3)
BrO3- + 6H+ + 6e = Br- + 3H2O (*1)
--------------------------------------------------------------------
3H2O2 + BrO3- = 3O2 + Br- + 3H2O
3H2O2 + KBrO3 = 3O2 + KBr + 3H2O
Дело в том, что должен выделяться Br2. Вот цитата из самой методички: В пробирку с подкисленным р-р KBrO3 прилить 3% р-р H2O2 и перемешать. Какие газы выделяются через небольшой промежуток времени? Определить выделение брома можно по запаху, по изменению окраски р-ра, по цвету газа над поверхностью жидкости в пробирке или с помощью органического р-ля, например, толуола".
-
Есть подкисленный раствор KBrO3, к нему мы приливаем 3% р-р H2O2 и перемешиваем. Какая будет среда (кислая или нейтральная), какие продукты реакции? Если нетрудно, прошу написать уравнение и ОВР методом полуреакций.
-
Как в данном случае выяснить термодинамическую возможность протекания реакций между растворами КМnO4 и Na2SO3 в: 1) кислой; 2) щелочной; 3) нейтральной среде? На фото полуреакции. И в какой среде окислительные свойства MnO4^- выражены сильнее?

-
4 минуты назад, Ximik500 сказал:
Правильно Na2CO3 - валентность у натрия I
Прописался, спасибо за поправку!
-
Почему для заполнения аппарата Киппа необходимо использовать мраморную крошку, а не порошок CaCO3 (NaCO3 или NaHCO3)?
-
Прошу помочь решить задачи.
1. 12,5 оксида некоторого элемента нагревали в токе водорода. Через определённое время нагревание прекратили. Масса остатка, в котором содержалась часто не прореагировавшего оксида, составила 11,7 г. Сколько воды образовалось в результате реакции?
2. К раствору, содержащему 16,1 г сульфата цинка, добавили раствор, содержащий 10 г едкого натра. Осадок отфильтровали. Какие соединения и в каком количестве находятся в фильтрате?
3. При сжигании 1 г смеси угля и серы образовалось 2,5 г смеси углекислого и сернистого газов. Сколько граммов угля и серы содержалось в смеси?
4. Какой объём займет кислород при нормальных условиях, если при 20 градусах Цельсия и 110 кПа его объём составляет 2,5 л?
5. При взаимодействии 5,2 г гидроксида металла с серной кислотой образуется 11,4 г сульфата. Рассчитайте эквивалент металла.
6. При растворении 1,18 г металла в серной кислоте получено 3,1 г сульфата. Удельная теплоёмкость металла равна 0,421 Дж/(г*К). Вычислите точное значение атомной массы металла.
7. При нагревании 1,61 г кристаллогидрата сульфита натрия образовалось 0,805 г безводной соли. Установите формулу кристаллогидрата.
-
Подскажите коэфф. омыления для рыбьего жира. Его состав нашел в Википедии, основные кислоты - олеиновая (более 70%) и пальмитиновая (около 25%). Мыло варить нужно, а соотношение масло/щелочь не известно.
-
-
Добрый день.Возник вопрос: "Можно ли произвести реакцию омыления, используя литиевую или бариевую щелочи вместо привычной калиевой и натриевой?"
Как это повлияет на конечный продукт (KOH - даёт пастообразное мыло, NaOH - твердое) с точки зрения консистенции, моющей способности и т.д?
Почему для изготовления мыла используют в основном два вида щелочи: KOH, NaOH (только ли из-за цены?)
Если можно провести реакцию, то как рассчитать кол-во масла (например, кокосового) на 1 грамм щелочи (LiOH, BaOH)? Я просто всегда считаю по калькулятору мыловара; с химическими формулами знаком.
-
Химию я немного знаю, иначе бы не поступал на химфак (а вот об уровне моих знаний...стоит промолчать, ибо всё зубрил и готовил сам, без чье-то помощи). Попробую тогда сделать, использую метод проб и ошибок ( авось, что выйдет, по крайней мере, будет интересно). О сложности промышленного процесса не знал, ибо не у кого было спросить. Поэтому, собственно, и обратился сюда. Спасибо.
-
Добрый день. Хочу сделать эмульгатор для косметики, для личного использования. Покупать аналог больно дорого (хотя компоненты в его составе не такие уж и дорогие), тем более он идет с Франции. Состав эмульгатора следующий: INCI: Cetearyl Olivate, Sorbitan Olivate. HLB: 12.
Я так понял тут две ступени реакции:
1. цетеариловый спирт + оливковое масло;
2. сорбит (глюцит) + оливковое масло.В обоих случаях идёт реакция этерификации (ссылаюсь на свои знания, может это и не так). В каком соотношении брать компоненты? Как именно проводить реакцию (шаги, условия, катализаторы, все мелочи)? В итоге должны получиться белые, твердые, воскообразные пластины-хлопья.
Вот цитата с одного сайта про этот эмульгатор: "Созданный из оливкового масла в процессе этерификации преэтоксилированным цетеариловым спиртом, этот эмульгатор содержит длинноцепочечные (C16-C22) жирные кислоты оливкового масла".
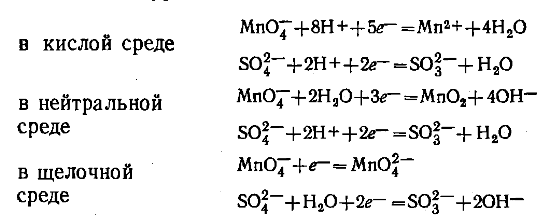
Реакции образования хлора. Проверить.
в Решение заданий
Опубликовано
1. Лабораторный метод получения хлора. 2KMnO4 + 16HCl = 2MnCl2 + 5Cl2 + 2KCl + 8H2O
В качестве индикатора используем полоску фильтровальной бумаги, смоченную р-ром.
А) Смачиваем полоску фильтровальной бумаги р-ром KI. Уравнение Cl2+2KI=2KCl + I2. Полоска будет темнеть (чернеть).
Б?) Подкислим р-р KI на фильтровальной бумаге конц HCl. Что будет происходить тут? Бумажка будет темнеть или светлеть?
По моим соображениям, она будет светлеть, так как HCl+Cl2+KI = KCl + HI (коэфф не расставлял, но выделение свободного йода не наблюдаем).
В) Смачиваем полоску фильтровальной бумаги р-ром KBr. 2KBr + Cl2 = 2KCl+Br2. Бумажка желтеет.
Г) После прекращения выделения хлора р-р в пробирке приобрел бурый цвет (Mn^2+). После того, как мы сливаем р-р в другую пробирку и добавляем воду, образуется бурый осадок Mn(OH)2.
Д)Оставшееся в пробирке в-во - MnCl2. После добавления к нему воды р-р становится малинового цвета.
2. В пробирку поместим небольшое количество MnO2 и добавим 1 мл конц HCl. 4HCl + MnO2 = Cl2 + MnCl2 + 2H2O. Р-р темно-фиолетового цвета. Сольем небольшое количество р-ра в другую пробирку и разбавим водой - р-р стал мутно-коричневого цвета, образовался осадок Mn(OH)2.
3. В пробирку поместим небольшое количество тщательно растертого K2Cr2O7 и добавим 1 мл конц HCl. 14HCl+K2Cr2O7 = 3Cl2+2CrCl3+2KCl+7H2O. Р-р из оранжевого стал темно-зелёным.
4. В пробирку поместим небольшое количество хлорной извести и добавим 1 мл конц HCl. Ca(Cl)OCl+2HCl = CaCl2+Cl2+H2O. Бумажка с KI чернеет, выделятся Cl2.
5. В пробирку поместим небольшое количество KClO3 и добавим 1 мл конц HCl. KClO3+^HCl=3Cl2+KCl+3H2O. Бумажка с KI чернеет, выделятся Cl2.
6. В пробирку поместим немного сухой смеси NaCl и MnO2 и добавим 1 мл конц H2SO4. Смесь слегка подогреем. MnO2+2NaCl+2H2SO4 = MnSO4+Cl2+Na2SO4+2H2O. Бумажка с KI чернеет, выделятся Cl2.
Прошу пожалуйста проверить на ошибки (особенно с цветом бумажек и р-ра). Будет ли свободный йод взаимодействовать с хлором и бумажка будет желтеть, или же не будет, и бумажка будет чернеть? В пункте Б для чего подкисляем р-р, что мы получим?