
valentinshved
-
Постов
63 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные valentinshved
-
-
01.05.2020 в 18:20, M_GM сказал:

По такой формуле сможем ли мы рассчитать время?
-
-
Сколько времени потребуется для выделения 11.2 л кислорода (н.у.) при электролизе раствора КОН, если сила тока равна 0.5 А? Запишите уравнения электродных реакций, если электроды платиновые.
Платиновые электроды = инертные, значит ф-ла реакции будет следующая:
(-) 2H2O + 2e = H2 + 2OH- | 2 | 1
(+) 4OH- - 4e = O2 + 2H2O | 4 | 2
2H2O = H2 + O2(0)
-
Добрый день всем, кто зайдёт сюда просто так или тому, кто действительно подскажет)
Интересует данная задача, её принцип решения и смысл.Условие и цель:


-
На основе данных об электродных потенциалах определите произведение растворимости Zn(OH)2 в воде
Чёт не допираю по какому методу это делать, хеелп
-
1. Как и во сколько раз изменится скорость ионной реакции Ag+ + Cl- = AgCl, если концентрацию этих ионов увеличить от 0.0002 до 0.004 моль/л?
2. В каком электролите - NaCl или AlCl3 - радиус ионной атмосферы катионов будет больше при одинаковой концентрации электролита.нужна пооомощь
-
Произведение растворимости Cu(OH)2 - 5.6*10-20
Какова концентрация ионов Cu2+ в растворе над осадком, если в раствор добавлен NaOH с концентрацией 0.1 моль/л?
Хеелп, подзабыл :-( -
пожалуйста, апдейт(
-
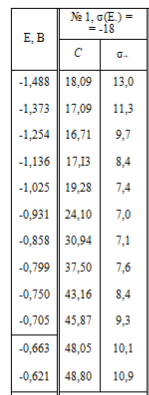
Помогите с задачей, в таблице брать данные g по столбцу "6"



-
Только 1 задание надо, со вторым вроде разобрался
-
Здравствуйте, нужна помощь по таким заданиям, с этой темой впервые сталкиваюсь, имеются сложности.
Задание 1: В какой форме находится аспарагин (pH = 4) и к какому электроду АК движется при проведении электрофореза?
Задание 2: изолейцин -> образование дикетопиперазина с последующим его гидролизом (HCl конц.) до линейного дипептида. -
-
5 минут назад, yatcheh сказал:
Спасибо большое! А ещё с одним не поможете?
Текст задания: Приведите условную схему сополимеризации мономеров
Соединения те же самые. -
Для каждого из мономеров привести реакцию полимеризации (условную схему)

-
Как будут выглядеть продукты реакции SnCl4*5H2O + Sb2O3?
-
Как изменится растворимость реагента I при добавлении в его насыщенный раствор реагента II до концентрации с(реагента II) = 0,25 М?
Реагент I = PbCl2
Реагент II = NaNO3
Остановился на этом
-
Как реагируют третичные амины с серной кислотой, с последующим гидролизом? Взять например тот же метилдиэтиламин
-
Господа химики, мне и вправду интересно наблюдать за Вашими спорами, но по реакции что можете сказать?
Я и облазил интернет, и сам пытался. По заданию поможете?
-
Вот полный текст задания. Видимо для моего проточного редокс элемента это задание не выполнимо

ЦитатаРазбить реакцию на электродные полуреакции, найти в справочниках значения стандартных электродных потенциалов, рассчитать стандартное значение и общее выражение для ЭДС гальванического элемента. Указать, какие факторы влияют на ЭДС. Оценить температурную зависимость ЭДС. Рассчитать величину накопленной электрической энергии, полученной при преобразовании энергии химической реакции в электричество. Для топливных элементов
-
15 минут назад, Иван1978 сказал:
как такое может быть? они ставят эти проточные редокс элементы на электромобили и утверждают что проехали 1000 км на одной зарядке. Это же солевые растворы, у них удельная энергия должна быть никакая в сравнении с металлическими батареями. Кажется обмануть нас хотят. Непонятно как мембрана удержит растворы от перемешивания. Им чтобы мощность потребную для авто сделать надо иметь огромную поверхность электродов. Как они ее обеспечат? В литиевых аккумуляторах сворачивают в ленты электроды.
Реакция не осуществима?
-
5 минут назад, Иван1978 сказал:
а разве хлорид титана и хлорид марганца реагируют? или у вас продукты слева написаны?
Такая реакция написана
Изучаю физ химию и тема «Химические источники тока: топливные и проточные элемент»
Под реакцией прописано "проточный редокс элемент" -
TiCl3 + MnCl3 + H2O ⇄ TiOCl2 + MnCl2 + 2HCl
Разбить реакцию на электродные полуреакции, помогите =)
-
1. Укажите pH раствора электролита до электролиза (кислая, щелочная, нейтральная)
2. Запишите уравнение электродных реакций электролиза с графитовыми электродами.
3. Как изменяется pH раствора у электродов в процессе электролиза (увеличится, уменьшится, не изменится).
4. Рассчитайте, сколько и каких веществ выделится на электродах при электролизе при заданных условиях. Анодный выход по току во всех случаях равен 100%Раствор электролита - BeSO4
Катодный выход по току - 0%
Сила тока - 3 A
Время - 7 часов
Замена материала анода - Fe.
Помогите пожалуйста! -
1. Укажите pH раствора электролита до электролиза (кислая, щелочная, нейтральная)
2. Запишите уравнение электродных реакций электролиза с графитовыми электродами.
3. Как изменяется pH раствора у электродов в процессе электролиза (увеличится, уменьшится, не изменится).
4. Рассчитайте, сколько и каких веществ выделится на электродах при электролизе при заданных условиях. Анодный выход по току во всех случаях равен 100%Раствор электролита - BeSO4
Катодный выход по току - 0%
Сила тока - 3 A
Время - 7 часов
Замена материала анода - Fe.
Помогите пожалуйста!




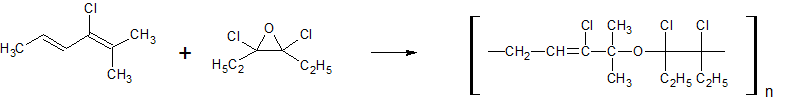



Электролиз на платиновых электродах
в Решение заданий
Опубликовано
Извиняюсь за вопрос! Что в данной ситуации считается за "n"? Количество электронов на аноде?