
sova
-
Постов
38 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные sova
-
-
спасибо, так и сделаю
-
Здравствуйте, то что хлорид аммония разлагается, я знаю, но вот моему бывшему ученику задали термодинамический расчет, в котором дана реакция разложении хлорида аммония и нада в числе прочего найти коэффициент активности газа по приведенным температуре и давлению.
Из общих соображений критические параметры будут похожи на среднее арифметические для аммиака и хлороводорода.
Т.е мне взять критическую температуру аммиака сложить с приведенной температурой хлороводорода, поделить на 2 и использовать это значение при расчетах?
-
Здравствуйте.
Уважаемые химики, помогите пожалуйств найти значения критической температуры и давления для хлорида аммония (NH4Cl).
Надо произвести термодинамический рассчет в котором кроме всего прочего нужны эти значения. Перерыла все справочники и в интернете искала- не нашла.
Заранее спасибо
-
Здравствуйте.
Помогите найти основные положения теории фон Веймарна.
Надо решить задачу:
При гравиметрическом определении Са2+ в кальция хлориде осаждение проводят:
а) раствором аммония оксалата или кислоты щавелевой;
б) из разбавленных или концентрированных растворов кальция хлорида;
в) в кислой, нейтральной или щелочной среде;
г) при нагревании или охлаждении раствора;
д) с последующим созреванием или без него.
Выберите из перечисленных необходимые условия для осаждения и аргументируйте свой выбор, используя положения теории фон Веймарна
Без теории вроде могу написать какие надо условия, а как их аргументировать с помощью теории не знаю, т.к не нашла саму теорию
Заранее спасибо
-
В данном растворе потенциал просто не способен устанвиться хоть на каком-то реальном значении, так как в нем нет никаких реальных редокс-систем. Ваш ответ ничуть не лучше всех остальных возможных. Просто задача исходно не корректна.
В принципе, Вы правы, но может посоветуете, что же все таки написать. Я читала про потенциалы редокси систем, может ....
Блин даже не знаю, что с этой задачей делать, взять потенциал (Cu + /Cu2+ ) то же не вариант. Так какой потенциал нужен преподавателю?!? ну не потенциал же платины вставить.
-
Здравствуйте, нужна помочь в решении задачи, точнее не помощь, а указать где ошибка.
Задача. Рассчитать потенциал платинового электрода, помещенного в раствор, содержащий 25 г сульфата меди (II) в 250 см раствор
Моё решение:Вычисление электродного потенциала электрода производится по уравнению Нернста
Е=Е0(Cu2+/Cu)+0.059/2lg(Cu2+)
Далее определила концентрацию сульфата меди в растворе (0.625 моль/л), она равна концентрации ионов меди в растворе
Потом подставила:
Е=0,345+0,059/2lg0.625=+0.339 B
В рецензии написали: В задаче расчитывается потенциал платинового электрода, в растворе , содержащем сульфат меди. Вы почему-то берете стандартный окислительно-восстановительный потенциал для медного электрода.
Вот и не знаю, что именно подставлять и как быть вообще.
Заранее спасибо
-
Я то же об этом думала, но как именно это правильно оформить я так и не поняла. Я понимаю , что по уравнеию Нернста концентрация ионов водорода и сульфат ионов будет значительно больше 1М. Но в задании надо именно объяснить с помощью потенциалов возможность протекания этой реакции. И как правильно это описать я и не знаю.
-
Здравствуйте
Подскажите, пожалуйста, где я делаю ошибку. Требуется с помощью ОВР потенциалов доказать возможность протекания реакции меди с концентрированной серной кислотой. Я выписываю стендартные потенциалы процессов восстановления и окисления:
Е(Сu2+/Cu)=+0,34 B
E(SO42-,H+/SO 2 ,H2O)=+0,20 B
Но по этим данным получается , что потенциал окислителя (серной кислоты) меньше потенциала восстановителя, т.е реакция НЕ возможна?
Но ведь со школьного курса химии известна , что эта реакция протекает, и именно с выделением сернистого газа.
Заранее спасибо
-
При вычислении Кр из формулы ΔG = -2,3RTlgKp применяется R=8,31 Дж/(моль*К). Подставьте эту размерность в формулу и убедитесь.
Кр измеряется в единицах атм, в вашем случае Кр= ... атм-2
Кс измеряется в единицах моль/л, в вашем случае Кс= ... (моль/л)-2 или (л/моль)2.
Поэтому при пересчете Кр в Кс (или наоборот) надо брать R=0,082 л*атм/(моль*К)
спасибо, т.е на сколько я поняла надо использовать данную формулу: Кр=Кс(RT)-Δν
-
Здравствуйте. Мне надо рассчитать Kр(R = 8,31 Дж/моль*К) и KC (R = 0,082 л*атм/моль*К), при заданной температуре T для заданной реакции CO(г) + 3H2(г) = CH4(г) + H2O(г)
Я рассчитала так : нашла изменение энергии Гиббса и по уравнению нашла Кр
D rG 01000=-2,3RTlgКр
А такнайти Кс? использовать для этого Кр=Кс(RT)-Δν
или то же уравнение
D rG 01000=-2,3RTlgКс
только вместо К=8,31 вставить 0,082
Честно говоря не нашла ни в одном задачнике ответа на этот вопрос, т.к в задачниках Кр=Кс(RT)-Δν в данное уравнение подсавляют 8,31 Дж/моль*К, а не 0,082 л*атм/моль*к
Заранее спасибо
-
Не совсем понятно.
Вот именно что не понятно, то ли речь идет о титровании или просто о переводе вещества в раствор. Но все равно всем спасибо,
-
Здравствуйте.
Очень нужна ваша помощь товарищи химики. Есть такой вопрос:
Как выбирают условия фотометрирования, если определяемое соединение и используемый реактив имеют окраску, отличную друг от друга , и реактив присутствует в избытке.
Что то меня совсем заело на этом вопросе.
Когда вещество окращенно то выбирают такую длину волны, при которой имеется максимум светопоглощения, но в данном случае и вещество и реактив окращенны, как быть?
-
Спасибо, идея хорошая, но :unsure: у меня ссылка почему- то не открывается. А видеоопыты нужны, конечно есть некоторое количество, но хотелось бы еще .
-
Здравствуйте , подскажите пожалуйст ответ на такой вопрос : В какой среде необходимо проводит перманганатометрическое определение калия гексацианоферрата(II) с индикатором метиловым фиолетовым, и какая должна быть окраска в начале титрования и в конце. Я уже второй день ищу эту информацию, и в книгах и в интернете.
Единственное , что нашла это интервал перехода этого индикатора, с указанием того что он является кислотно основным. Я предполагая, что среда должна быть сернокислой ( как для обычного перманганатометрического титрования), в начале титрования окраска , наверное желтая ( по цвету титруемого вещества, да и индикатор в сильнокислой среде желтый, хотя сильно смущает, что индикатор все же кислотно основной и как с его помощью определить конечную точку титрования???
 и зачем он вообще нужен???).
и зачем он вообще нужен???).А в конце титрования цвет вообще без понятия какой.
Заранее спасибо
-
Дизай нормальный, привыкнем.
Меня смущает только одно : вот этот значок( не знаю как он правильно называется) рядом с адресом форума . Я этот значок уже встречала ( причем один в один ) у другого сайта, который занимается написанием студенческих работ. Старый был право лучше.
-
Здравствуйте.
Помогите советом , если можете Есть такая задача:
Рассчитайте и постройте кривые зависимостей численной концентрации первичных (одинарных), двойных и тройных частиц от времени быстрой коагуляции τ гидрозолей, используя данные об изменении общей концентрации частиц vΣ в процессе коагуляции
τ,с 10 20 50 120 240 360
νΣ•10-14частиц\м3 37,2 30,9 20,6 11,6 6,6 4,6
Вообщем проблема в том, что не дана начальная концентрация частиц. А именно она входит во все формулы коагуляции. Я впринципе подобные задачи решала не раз, но в этих заданиях нет начальной концентрации и меня берет сильное сомнение в правильности решения :
При быстрой коагуляции изменение частиц во времени выражается уравнением
ν_ϵ=ν0* 1/(1+τ⁄θ)
где θ не зависит от времени коагуляции и является постоянной величиной. Зависимость ν0/ν—t представляет прямую, не проходящую через начало координат. Тангенс угла наклона этой прямой к оси абсцисс равен 1/θ. Построим график ( я условно приняла начальную концентрацию равной 37,2 ( первое число)). ну и далее определила все остальные величины.
Однако меня берет сииильное сомнение. Подскажите , пожалуйста , что делать
-
Спасибо Всем большое за подсказку.
-
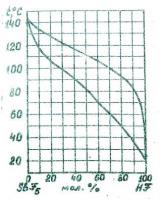
Здравствуйте, господа химики. У меня такой вопрос по диаграмме:подчиняется ли система состава 20 мол% НF при температуре кипения закону Рауля и объясните причины отклонения от идеального раствора.
Если я правильно поняла, то данная система не подчиняется закону Рауля, т.к. растворенный компонент( HF) является летучим, а закон Рауля справедлив для растворов с нелетучим растворенным веществом. СОоответственно это и являюется причиной отклонения от закона Рауля.
Я правильно ответила на этот вопрос ?
-
Здравствуйте. Помогите найти учебник Липатников,Казаков .Физическая и коллоидная химия. Не знаю, хороший ли это учебник. Я с ним не знакома. Дело в том, что я по образованию химик- биолог, но закончила университет в 1999 году. С тех пор судьба меня бросала в отрасли, весьма далекие от химии. Сейчас мне предстоит вести в СУЗе 2 дисциплины: физическиая и коллоидная химия и аналитическая химия ( у технологов общественного питания - поваров по-русски). Нужно самой вспомнить + научить их на доступном языке. Уровень их - махровые троечники
 Еще бы найти методички по проведению лаб.работ. буду благодарна всем, кто откликнется
Еще бы найти методички по проведению лаб.работ. буду благодарна всем, кто откликнетсяЗдравствуйте. У меня есть текстовая версия данного учебника, только без некоторых таблиц( я их не копировала,т.к. эти данные есть и в других справочниках), но все картинки на месте. Если надо могу отправить на мыло.
Хотя если честно мне больше нравиться учебник Евстратовой К.И. и Купиной Н.А. , но для поваров сойдет и Липатников.
-
1.Напишите формулы коллоидных частиц мицеллы золя, полученных при взаимодействии 10 мл 0,0001 н. раствора MnSO4 и 30 мл 0,0001 н. раствора NaOH.
Для начала определим какое из веществ взято в избытке. Согласно закона эквивалентов вещества взаимодействуют в эквивалентных колличествах, следовательно:
C(MnSO4)V(pMnSO4)=C(NaOH)V(pNaOH)?
однако :
0,01 л*0,0001н меньше 0,03л*0,0001н,
следовательно NaOH в избытке, тогда формула частиц мицеллы:
{m(Mn(OH)2) nOH-(n-x)Na+}x- xNa+
-
Калиевые мыла жидкие, могут быть получены при обработке жиров (или жирных кислот) едким кали или поташем.
Это я знаю, мне из твердого надо было получить жидкое, а вообще спасибо всем
-
Думать еще никому не вредило. Только смысл твоих размышлений не понятен. Что такое по твоему твердое мыло
помоему это натриевая соль жирных кислот
-
Здравствуйте , товарищи ( или господа) Химики.
нужен совет: как из твердого мыла получить жидкое( в теории) . Я так думаю надо вначале провести рекцию с кислотой ( например соляной). Тогда по
лучится хлорид натрия и жирные кислоты, и затем провести реакцию с гидроксидом ка
лия или карбонатом.
Я правильно думаю?
-
Здравствуйте господа химики!
У меня есть несколько небольших вопросов :
Задан гальванический элемент состоящий из цинкового электрода и кислородного электрода
Надо написать электродные процессы и токообразующую реакцию( я написала так).
А: Zn -2e = Zn2+
K: O2+2H2O=4OH-
Zn+O2+2H2O= Zn2+ +4OH-
Надо вычислить ЭДС , исходя из а) термодинамических и б) электрохимических данных.( Это я сделала).А вот как объяснить небольшое различие в величинах ЭДС у меня както не поллучется.
Но самый главный для меня вопрос"Покажите графически ход поляризационных кривых." Я не поняла их надо высчитывать ( если да то как) или нарисовать схематически( тоже не знаю как).
И еще необходимо определите температурную зависимость ЭДС . Это используя Уравнение Нернста или по другому?
Заранее спасибо.
Поверхностное натяжение пленки бутиламина
в Решение заданий
Опубликовано
Здравствуйте. Мы с дочкой решали контрольную по коллоидной химии. Все задания решили , а одно не можем. Подскажите , пожалуйста как её решить ( ну хотябы с чего начать или формулу, а то я понять не могу как решить)
Краевой угол воды на парафине равен 111° при 298 К. Для 0,1М раствора бутиламина в воде поверхностное натяжение составляет 56,3 мДж/м2, краевой угол на парафине равен 92°, Рассчитайте поверхностное натяжение пленки бутиламина, адсорбированного на поверхности раздела парафин-вода. Поверхностное натяжение воды 71,96 мДж/ м2.
Заранее спасибо.