
Александр-chem
-
Постов
79 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Александр-chem
-
-
Подождите,а дальше как мне нужно идти?
-
Kд= а^2/1-а*С
Кд=0,061^2/1-0,061*0,1=0,000396272630458(HNO2)
Kд=0,0132^2/1-0,0132*0,1=0,000017657073368 (CH3COOH)
А дальше через а= корень К/С найти С?
-
Растворы азотистой и уксусной кислот имеют одинаковую концентрацию С=0,1 моль/л и характеризуются степенями диссоциации 0,061 и 0,0132, соответственно. До какой концентрации необходимо довести раствор уксусной кислоты,чтобы степень ее диссоциации достигла величины,характеризующей исходный раствор азотистой кислоты.
Ребят,помогите,пожалуйста!
Получается, HNO2 и CH3COOH имеют одинаковую концентрацию = 0,1моль/л.
а1=0,061 (HNO2)
a2=0,0132 (CH3COOH)
Формула степени диссоциации:
a= n/N
Исходя из формулы: C=n/V
Найдем моли: Примем V=1л
n(HNO2,CH3COOH)=0,1 моль/л*1 л=0,1 моль
А вот дальше я не знаю
-
Fe3C+H2O —CH4+Fe(OH)3
Ребят,помогите пожалуйста,запутался. Реакция идёт?
-
34 минуты назад, BauVictoria сказал:
Дигидрат диакватетраамминмеди, правильно?
Нет.
Гидроксида диакватетраамминкупрат (1)
-
-
В 0,2 М растворе фосфористой кислоты H3PO3 концентрация тонов H^+ равна 0,05 М. Вычислите константу диссоциации H3PO3 предполагая,что второй протон не отщепляется.
Решение
Kд=a^2*C/1-a
Из этой формулы я как раз найду Kд, С-концентрация кислоты, а вот a=[H^+]/C
a-степень диссоциации,из это формулы, я не могу a=[H^+]/C, подставить. Объясните,пожалуйста!
-
При повышении температуры от 60 до 70 градусов константа скорости реакции возросла в два раза. Рассчитайте энергию активации реакции.
Решение
2=70-60/10=2^1=2
Ea=R*T1*T2/T2-T1*Ln*K2/K1
Дальше я не могу понять,как найти энергию активации,даже не могу найти константу 2
-
Какой металл имеет четыре соединения с кислородом,двух из которых содержание металла 83 %и 71%?
-
При сгорании газообразного вещества «А» образуется белое твердое вещество «В», хорошо растворимое в воде с образованием кислоты. Вещество «В» реагирует в присутствии воды с «С», образуя смесь двух солей, которая используется в качестве комплексного удобрения. Элементы, входящие в состав «А» и «С», находятся в одной группе периодической системы. Что из себя представляют вещества «А», «В», «С»?
Я пока,что определил «А» это PH3,а «В» это P4O10
А вот «С» не могу никак определить
-
Газовая смесь, имевшая объемный состав: кислорода 20%, азота 75%, оксида углерода (IV) 0,5 % и хлора 4,5%, была растворена в воде при 00С под давлением в 5 атм. Растворимость в воде при 00С кислорода 4,89 мл, азота 2,35 мл, оксида углерода (IV) 171 мл и хлора 461 мл на 100 мл воды. Вычислитемассу указанных газов, содержавшихся в 1 л раствора.
Через уравнение Менделеево-Клапейрона можно решить?
-
-
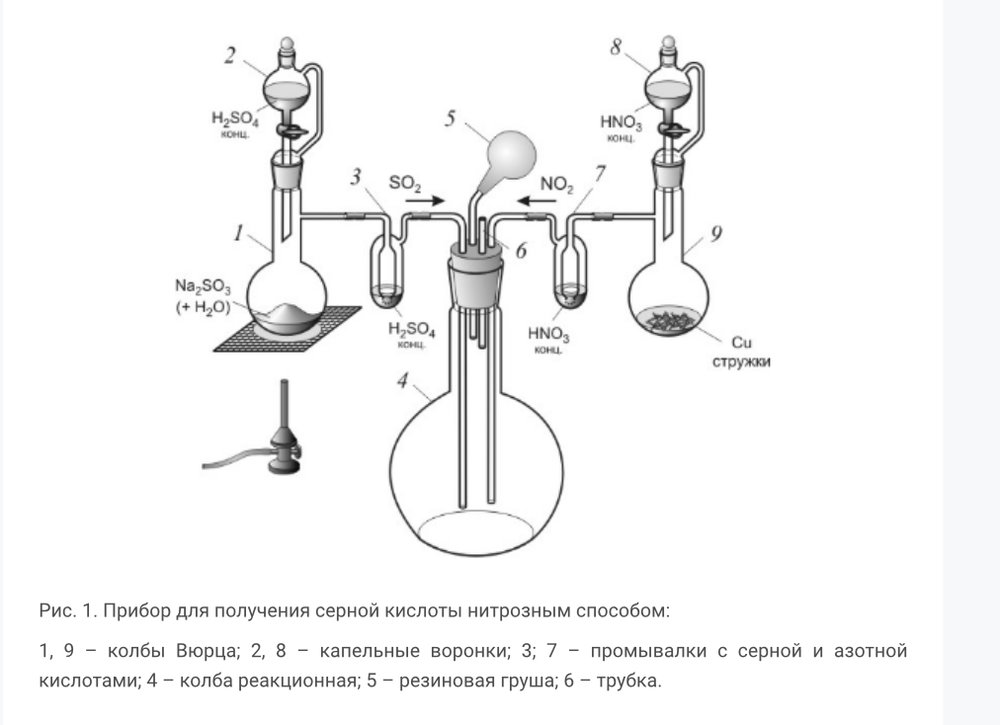
Промывалку 3 он заполнил концентрированной серной кислотой, а промывалку 7 – концентрированной азотной кислотой (в защитных очках и перчатках!). В колбу Вюрца под номером 1 он через стеклянную воронку поместил 28 г сульфита натрия и смочил дистиллированной водой, а в колбу Вюрца 9 положил 7,5 г медных стружек.
Он знал, что выделяющиеся газы ядовиты, поэтому проверил прибор на герметичность. Далее он отсоединил колбу 4 и подержал ее горловину над стаканом с кипящей водой, чтобы на стенках внутри колбы сконденсировались мельчайшие капли воды. В дальнейшем в этих местах закристаллизуется нитрозилсерная кислота. Он установил колбу на свое место. В капельную воронку 2 он налил концентрированную серную кислоту, а в капельную воронку 8 – концентрированную азотную кислоту.
Открыв кран в правой части прибора, он заполнил колбу 4 диоксидом азота (окраска стала достаточно интенсивной), затем закрыл кран капельной воронки 8 и запустил в колбу 4 ток диоксида серы. После обесцвечивания содержимого колбы и кристаллизации выпавшей нитрозилсерной кислоты на стенках колбы 4, он прилил 2 мл воды в трубку 6 и ополоснул стенки колбы. С помощью резиновой груши 5 он прокачал немного воздуха через колбу 4, наблюдая изменение окраски газа.
Затем он вновь пропустил ток сернистого газа в колбу 4 до обесцвечивания содержимого колбы 4 с последующим прокачиванием воздуха для окисления оксида азота. Цикл окисления сернистого газа он повторил несколько раз, приливая при необходимости воду через трубку 6 и восполняя потери диоксида азота. После прекращения выделения сернистого газа в колбе Вюрца 1 он ополоснул колбу 4 еще некоторым количеством воды и вылил полученную жидкость в стакан.
Определите, какова массовая доля серной кислоты в полученном растворе, если суммарно он прилил 10,5 мл воды в колбу 4, а реакция взаимодействия сульфита натрия с серной кислотой протекает с выходом 99%.
SO2 + HNO3 = (NO)HSO4
(NO)HSO4 + H2O = H2SO4 + HNO2
Реакции оксида азота(IV):
3NO2 + H2O = 2HNO3 + NO
SO2 + NO2 = SO3 + NO
4SO2 + 2NO2 = 4SO3 + N2 -
Напишите название простого вещества молекулярного строения, если известно, что 3 моль данного вещества весит 2,16 кг и оно содержит больше 50 атомов в своем составе.
2,16 кг=2160 г
Mr(X)=m/n=2160/3=720 г/моль
50/720*100= 6,94 -это Лития
-
Благодарю
-
В 08.01.2019 в 21:40, yatcheh сказал:
Может пирамидон
Да,возможно)
-
Структурные формулы: Пирамидин,
круглая кислота
-
Благодарю
-
Рассчитайте тепловой эффект фотохимической реакции хлорирования метана, если хлорированию подверглось 160 г алкана с образованием тетрахлорметана.
CH4+Cl2=CH3Cl+HCl
CH3Cl+Cl2=CH2Cl2+HCl
CH2Cl2+Cl2=CHCl3+HCl
CHCl3+Cl2=CCl4+HCl
Q= число превращённых молекул светопологающего вещества/ число поглощённых световых квант
сначала я нашёл моль (СCl4)=m/M=160г/154г/моль=1,03896 моль
Лучше решить через закон Гесса или по-другому как-нибудь можно?
-
CH3-C(CH3)2-(C=O)-CH3+KMnO4+H2SO4=
Что получится?
-
Как из гексадиена-3,4 получить ch3-c(ch3)2-(c=o)-ch3 (кетон получить)?
-
Но тут даже не написали,просто дали смеси и все
-
Какой моносахарид будет реагировать с избытком баритовой воды,при этом образуется белый осадок?
-
Смесь трёх газов, взятых в объемном соотношении 1:2:2, при 32 градуса и давлении 1,2 атм имеет плотность 2,110 г/л. После увеличения мольной доли первого газа в два раза и уменьшения мольной доли второго газа в полтора раза плотность смеси не изменилась. Предложите возможные формулы газов


Концентрация
в Решение заданий
Опубликовано
a=Корень K/C
С= корень К/а= Корень 000017657073368/0,061=
0,017013530472984