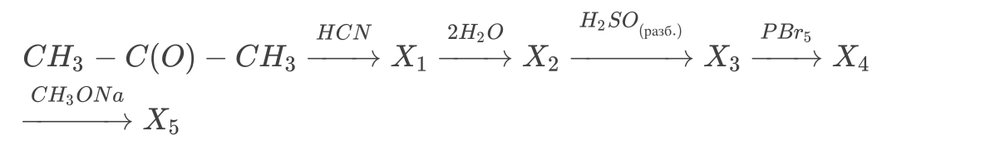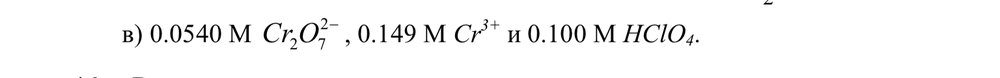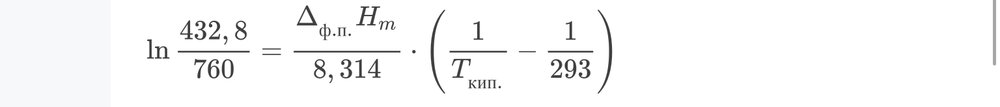Alex-chem
Участник-
Постов
342 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Alex-chem
-
Найдите значения потенциалов ионизации следующих металлов: а) Лития и натрия б) Кальция и магния в) Алюминия и галлия Сравните найденные значения потенциалов ионизации для каждой пары металлов. Подтверждается ли вывод о зависимости металлических свойств простых веществ от потенциалов ионизации атомов? Ребят,помогите,пожалуйста!
-
Да,в этом проблем. Спасибо X=0,02 Y=0,01 z=0,01 Чтобы мне найти мольные доли,то мне надо 0,02*46/1,82?
-
CH3COOH+NaOH — CH3COONa+H2O HCOOH+NaOH — HCOONa+H2O Ag2O+4NH3+H2O — 2[Ag(NH3)2]OH n(NaOH)= p*V*w/100%*M=1,06г/мл*18,9 мл*6,0%/100%*40г/моль=0,03моль n(NaOH)=n(CH3COOH)=0,03моль n(NaOH)=n(HCOOH)=0,03моль HCOOH+2[Ag(NH3)2] —CO2+2Ag+4NH3+H2O HCOH+2[Ag(NH3)2]— HCOONH4+2Ag+3NH3+H2O n(Ag)=m/M=8,64г/108г/моль=0,08 моль Составим уравнение: x-HCOOH,y-CH3COOH,z-HCOH X+y=0,03 2x+2y=0,04 46x+60y+30z=1,82 Ребят,пожалуйста,проверьте,не могу решить уравнение.
-
145,669 (бензойная кислота) 83,731 ( фталевая кислота) m1=300-145,669=154,331г m2=300-83,731=216,269г m(общая)= 370,6г выход1= 145,669г/370,6г*100%=39,31% выход2= 216,269г/370,6г*100%=58,356% Вот так? Поправьте,пожалуйста,если я неправильно сделал
-
Фталевая кислота:166 г/моль Бензойная кислота: 122 г/моль 288г/моль- общая масса всех кислот если мы станем находить кислород,то у нас получиться 22,2%,что-то опять не сходится А вот это как нужно находить?
-
Тут реакция через КОН водный или нет?
-
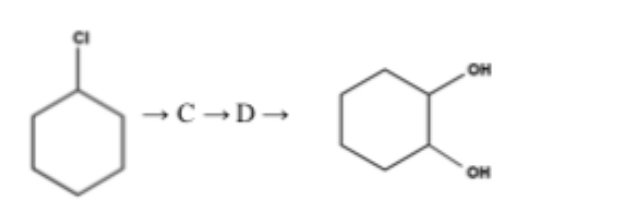
из D реакции получить циклогександиол-1,2,можно из циклогексанол-1 под действии OsO4, а вот как получить из хлорциклогексан С и D. Подскажите,пожалуйста!
-
Нужно было по-другому решить? Объясните,пожалуйста! Не пойму я просто.
-
Теплота образования F2O из простых веществ при стандартных условиях составляет 22 КДж/моль. Рассчитайте энергию связи O-F в молекуле фторида кислорода,если энергия связей в молекулах O2 и F2 составляет соответственно 498 и 159 КДж/моль. Решение: F2+1/2O2 — F2O dH(F2O)=1/2*498+159-2*22=364 КДж/моль Ребят,проверьте,пожалуйста! Правильно ли я решил?
-
4) 5) 2Na3[Cr(OH)6]+3CO2 —2 Cr(OH)3+ 3Na2CO3+3 H2O А вот дальше решать через уравнение?
-
Смесь гидроксидов хрома (||) и (|||) общей массой 2,92г растворили в избытке соляной кислоты. К полученному раствору добавили избыток щелочи и получили осадок массой 0,86г. Через фильтрат пропустили углекислый газ до прекращения выделения осадка. Найдите массу второго осадка. Напишите уравнения реакции ( все опыты проводили в инертной атмосфере). 1) Cr(OH)2+2HCl — CrCl2+2H2O 2) Cr(OH)3+3HCl —CrCl3+3H2O 3) CrCl2+2NaOH — Cr(OH)2+2NaCl 4) CrCl3+3NaOH — Cr(OH)3+3NaCl 5) 2Cr(OH)3+3CO2= Cr2(CO3)3+3H2O Правильно я написал уравнения? Проверьте,пожалуйста!
-
Решение: 1. 2Na+2H2O–2NaOH+H2 2. Na2O+H2O—2NaOH n(Na2O)=m/M=20г/62г/моль=0,3226 моль Пропорция: 0,3226 —— (-76,76) 1 —— X X=-238 КДж/моль H=2*(-238) КДж/моль -( (-76,76)КДж/моль+ (-285,8) КДж/моль=-476КДж/моль+362,56КДж/моль= - 113,44 КДж/моль P.S Ребят,правильно я решил? Проверьте,пожалуйста!) Если я неправильно решил,то поправьте,пожалуйста!)
-
Получается: CH3-CH(-OH)-COOH?
-
-
Извиняюсь,получается С6Н4(Cl)CH2CH3 А куда уйдёт хлор?
-
1)C6H6+CH2=CH2——C6H5CH2CH3 2) C6H5CH2CH3+Cl2——AlCl3——C6H4(Cl)CH2CH3+HCl 3) C6H5(Cl)CH2CH3+KMnO4+H2SO4—-t—- Подскажите,пожалуйста,что тут получится?
-
А да,тогда уже будет 6. Спасибо Е=E0+8,314*298/6*96500*ln0,149*0,100*10^-12/0,0540=-0,1237 у меня вот такой ответ получился. В чем ошибка?
-
Рассчитайте потенциал Pt-электрода, погруженного в раствор, содержащий: Cr2O7+14H+3e————Cr^3+. +7H2O Решим через уравнение Нерста E=Eo+RT/nFLn [Cr3+]/[Cr2O7]= Ответ:1,199В . У меня не сходится. Помогите,пожалуйста. В чем моя ошибка?
-
Во-первых,такие задачи встречаются в ЕГЭ,они легко решаются. n(CO2)=61,6/44=1,4моль n(CO2)=n(C)=1,4моль n(H2O)=25,2/18=1,4 моль n(H2O)=n(H2)=2,8моль m(C)=16,8г m(H2)=2,8г mобщ=42-16,8-2,8=22,4г n(O2)=22,4/16=1,4моль 1,4:2,8:1,4. /1,4 1:2:1=CH2O Во-вторых,тут про плотность ничего не пишут. Это задача полная?!
- 4 ответа
-
- 1
-

-
У меня вот ответ получается,1/Ткип=3,24785*10^-3
-
Получается будет вот такое уравнение, 1/Tкип=Ln(432,8/760)/28344,83/8,314+1/293=?
-
Ой,извиняюсь,забыл написать, delta Hm=28344,83 Дж/моль
-
Ребят,у меня возникла проблема,не могу посчитать Ткип. Но ответ получается. 307,9К. Объясните,пожалуйста,как тут надо правильно посчитать.
-
Определите структуру углеводорода состава C5H8, дающего с избытком хлороводорода соединение состава C5H10Cl2. Также известно, что гидролиз образующегося соединения приводит к образованию кетона нормального строения. При мономолекулярном присоединении к исходному соединению хлороводорода образуется вещество состава C5H9Cl, не имеющее геометрических изомеров и не подвергающееся гидролизу. Исходно название это пентин-1?