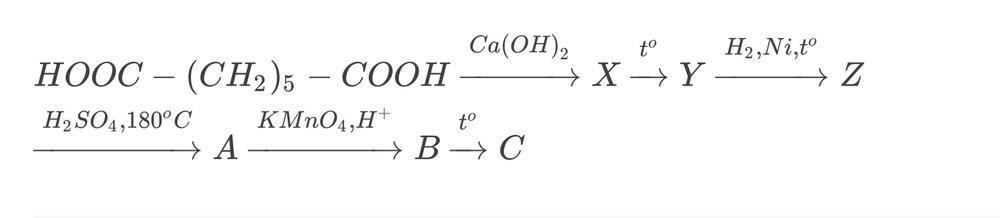Alex-chem
Участник-
Постов
342 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Alex-chem
-
Ср=34,7 Дж/моль*К (лёд) Ср=75,3 Дж/моль*К (вода) S=CpLnT2/T1 S1=200г/18г/моль*34,7Дж/моль*К*Ln273K/363K=-109,8Дж/К S3=200г/18г/моль*75,3Дж/моль*К*Ln363K/273K=238,4Дж/К S2=Q/T=200г/18г/моль*6000Дж/моль/363К=183,6 Дж/К S=S1+S2+S3=-109,8Дж/К+183,6Дж/К+238,4Дж/К=312,2 Дж/К В ответе 37,1 Дж/К. Какая у меня ошибка?
-
Рассчитайте изменение энтропии при добавлении 200 г льда, находящегося при температуре 0 оС, к 200 г воды (90 оС) в изолированном сосуде. Теплота плавления льда равна 6.0 кДж/моль. Решение: Т = 273 К дальше по формуле нахожу S S1= Cp* mл * Ln(T/Tл) S2= Cp* mв * Ln(T/Tв) S=S1+S2 Ответ: 37.1 Дж/K Чему будет равен Cp? Cp=4,184? Почему дана теплота?
-
Я думаю,что это AlBr3 и Zn(NO3)2 были. Алюминии с ацетатом дают белый осадок,а бурые пары это NO2
-
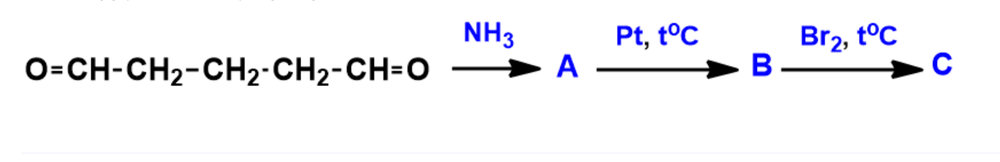
Ребят,проверьте,пожалуйста у меня. Какую ошибку я допустил? А: NH=CH-CH2-CH2-CH2-CH=NH B: NH2-CH2-CH2-CH2-CH2-CH2-NH2 C: Br-CH2-CH2-CH2-CH2-CH2-Br
-
Решил! T1/2=-Ln2/Ln*m/m*t=-Ln2/Ln*0,016мг/0,050мг*24,9ч=83,476ч. Правильно я решил?
-
Хлорид натрия-24 используют для изучения натриевого баланса живых организмов. Образец содержит 0,050мг натрия-24. Через 24,9ч содержание уменьшилось до 0,016мг. Рассчитайте период полураспада натрия-24 Решение: из формулы: m(t)=m0*(1/2)t/T1/2 T1/2=Ln*m1/m2*t/ln2*t Правильно я вывел формулу? Помогите,пожалуйста
-
При электролизе водного раствора калиевой соли одноосновной кислоты на аноде образовались газ и твёрдое вещество, содержащее 93,5% углерода. Назовите неизвестную соль и напишите уравнение электролиза. Решение Реакция Кольбе 2RCOOK+2H2O=R-R+2CO2+H2+2KOH n(C)=х моль n(H)=y моль W(C)/M(C):W(H)/M(H)=93,5%/12:6,5/1=7,79:6,5=1,1987:1. Умножаем на 2=2,3974:2.Формула: C2H2 Подскажите,пожалуйста,что дальше нужно делать!
-
Ребят,пожалуйста,проверьте! C6H5NO2=(CH2=CH-CH3)=C6H5-C3H6NO2 C6H5-C3H6NO2+Fe+HCl=[C6H5-C3H6NH3]Cl
-
Ребят,пожалуйста,подскажите,как это вещество называется? (CH3)2CH-C(O)-CH3
-
Но если поместить кусочек меди и прилить 5 мл концентрированной серной кислоты, после чего нагреть пробирку. Медь медленно начинает растворяться, раствор окрасился в сине-зеленый цвет, а над поверхностью смеси появились бурые пары. Значит,это трёхвалентный хром. Если поместить гидроксида натрия в пробирку,раствор помутнел, затем выпал белый аморфный осадок, который при дальнейшем добавлении щелочи полностью растворился. Это уже Al(OH)3 (белый,аморфный осадок).При добавлении раствора карбоната натрия в пробирку выпал белый осадок и выделился газ без запаха. Значит,это CO2 газ и анион CO3,то неизвестный металл
-
Ой,извините,не разглядел. Спасибо большое!
-
При добавлении лакмуса по каплям,раствор окрасился в бледно-красный цвет? Что за неорганическая соль может быть такая? А если прилить 1-2мл раствора ацетата свинца,становится белый осадок?
-
Ответ тогда будет 5,96,если перевести в практическую массу?
-
Определите, какое число различных изомеров получится, если трижды провести реакцию алкилирования по Фриделю-Крафтсу хлорбензола необходимым количеством хлорметана в присутствии AlCl3. Считайте, что все реакции протекают последовательно. C6H5Cl+CH3Cl=(AlCl3)=C6H4(CH3)Cl+CH3Cl=(AlCl3)=C6H3(CH3)Cl(CH3)+CH3Cl=(AlCl3)=C6H2(CH3)3Cl 9 изомеров будет?
-
В следующий раз,я буду повнимательнее тогда,зато есть напоминание о правилах работы в лаборатории Спасибо большое! Окрашивание кожи при попадании на нее HNO3 обусловлено ксантопротеиновой реакцией
-
Для этого он напильником от большого куска алюминия отпилил 4 г порошка алюминия, отобрал 13 г железной окалины и тщательно перемешал. Прибор для эксперимента собирал в вытяжном шкафу. В металлическое кольцо на штативе он поместил сложенное конусом асбестовое одеяло, положил внутрь сложенный бумажный фильтр и насыпал в него полученную смесь для алюминотермии. В этой смеси он сделал небольшую ямку и поместил в него запал, в который установил магниевую ленту массой 0,3 г. Внизу штатива под реакционной смесью он поставил металлическую емкость с песком. Он надел очки, поджег алюминиевую ленту и быстро закрыл створки вытяжного шкафа. Определите, какую массу металлического железа сможет получить по приведенной методике, если потери составляют 20%. Правильно ли я решил? Алюминотермия: 3Fe3O4 + 8Al = 4Al2O3 + 9Fe n(Al) = m/M = 4 г/27 г/моль = 0,148 моль n(Fe3O4) = 13 г/216 г/моль = 0,06 моль По уравнению видно, что алюминий в недостатке, поэтому n(Fe) =9/3n(Fe3O4) = 0,18 моль m(Fe) теор = n*M = 0,18 моль*56 г/моль = 10,08=10,1 г W=100%-20%=80% m(Fe) практ = m(теор) *w/100%= 10,1 г*80%/100%= 8,08=8,1г
-
Подскажите,пожалуйста! Металлический кальции можно хранить в банке из темного стекла под слоем керосина,вдали от воды,окислителей и открытого огня или хранят в сухом шкафу,в банке с плотно закрытой крышкой? KMnO4(х.ч)- можно хранить в вытяжном шкафу,в банке из темного стекла? NaOH хранят в сухом шкафу, в банке с плотно закрытой крышкой? А вот бензол могу хранить в вытяжном шкафу,вдали от открытого огня? Азотну кислоту можно хранить в сухом в шкафу,в банке с плотно закрытой крышкой,чтобы концентрация не уменьшилась? Только вот хлористое железо ч.д.а хранят ли в сухой банке с плотной закрытой крышкой или в сухом в шкафу,вдали от восстановителей и открытого огня?
-
Выберите среди предложенных утверждений верные: 1.Все эксперименты необходимо проводить в вытяжном шкафу 2.В химической лаборатории необходимо находиться в специальной одежде (защитном халате) 3.В химической лаборатории нельзя принимать пищу или пить воду, но в случае сильной жажды можно выпить немного дистиллированной воды 4.Помещение химической лаборатории должно быть хорошо вентилируемым 5.Для грамотного планирования работы и анализа результатов необходимо вести записи в лабораторном журнале 6.Отработанные соли, кислоты и щелочи сливают в одну специальную емкость, которую называют "слив" 7.В лаборатории разрешается работать одному, только если эксперимент не занимает много времени 8.Все реактивы необходимо хранить в герметично закрытых емкостях 9.Если пролитый органический растворитель загорелся от пламени горелки, его можно потушить водой 10.В каждой химической лаборатории должна находиться аптечка. Ответ:2345610 Ребят,пожалуйста,проверьте. Правильно ли я выбрал или я что-то ещё упустил?
-
Подумал,прочитал,что вы мне посоветовали,что желтые пятна- это проявление реакции белков кожи с азотной кислоты. Опасно нет никакой
-
А реакция считается экзотермическая?
-
Из-за чего окраска появилась? Желтая рука проявление реакции белков кожи азотной кислоты,или желтая окраска кожи возникает из-за реакции жиров на поверхности кожи с гидрокарбонатом,или азотная кислота может вызвать ожоги,даже если ее смыть водой? Нужно срочно обратиться к врачу,или можно просто подержать под струей холодной воды, потом обработать пантенолом или все это неопасно?
-
Я готовил раствор 10%-ной азотной кислоты без перчаток и случайно разлил ее себе на руки. Я знал, как правильно действовать в таких случаях: я промыл руки в проточной воде, затем обработал 3%-ным раствором гидрокарбоната натрия и вновь промыл водой. Поскольку действовал быстро, то боли от пролитой азотной кислоты не почувствовал. Но тем не менее, кожа на руках пожелтела и стала жесткой. С чем связана такая окраска и что мне делать?
-
А стоп,нет,перепутал! Получается А-циклогексен,В- Адипиновая кислота,С-циклопентанон
-
X-(OOC(CH2)5COO)2Ca Y-циклогексанон Z- циклогексанол А-гексен-3 B- CH3CH2COOH C- не получается у меня Подскажите,пожалуйста!