Alex-chem
Участник-
Постов
342 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Alex-chem
-
-
Спасибо большое!
-
Оксид кальция, полученный при прокаливании 60 г карбоната кальция, растворен в строго необходимом количестве 36,5%-ной соляной кислоты. Полученный раствор охлажден до 00С. При этом выпал шестиводный гидрат соли. Насыщенный раствор при указанной температуре содержит 27,2% кристаллогидрата. Вычислите массу выпавших кристаллов. Решение: CaCO3=CaO+CO2 n(CaCO3)=m/M=60г/100г/моль=0,6моль CaO+2HCl=CaCl2+H2O n(CaCO3)=n(CaO)=0,6 моль n(CaO)=2n(HCl)=0,12моль m(HCl)=n*M=0,12моль*36,5г/моль=4,38г m(HCl)=m*w/100%=4,38г*36,5%/100%=1,5987г n(HCl)=m/M=1,5987г/36,5г=0,0438моль CaCl2+6H2O=CaCl2*6H2O n(HCl)=6n(CaCl2*6H2O)=0,2628моль m(CaCl2*6H2O)=0,2628моль*220г/моль=57,816г m(CaCl2*6H2O)=57,816г*27,2%/100%=15,7259г В ответе написано m(CaCl2*6H2O)=123,1г В чем ошибка?
-
[Co(NH3)6]Cl3 - хлорид гексаамминкобальт (|||) Na3[Al(OH)6]- гексагидроксоалюминат натрия (|) K2[Zn(OH)6]- гексагидроксоцинкат калия (|) Проверьте,пожалуйста,правильно ли я назвал вещества?
-
От 0 до 4 это алкан,от 4 до 7 алкен, от 6 до 9 ароматика,а вот от 9 идет уже альдегид,карбонильные группы
-
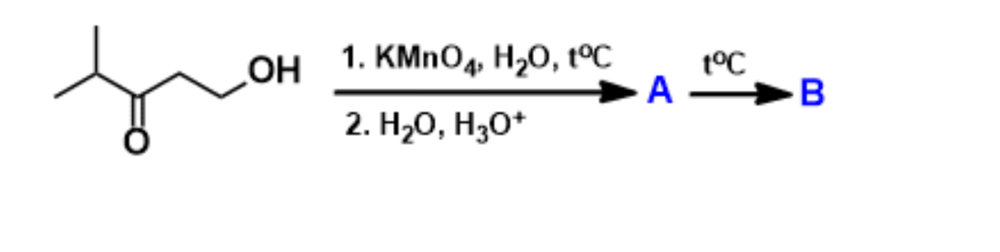
CH3-CH=CH-CH3 —> 2CH3-CHO (ацетальдегид) Катализатор: 1) O3, 2) Zn,H2O
-
MoCp2H2=6+5*2+2=18 [HCr2(CO)10]=1+6*2+2*10=33 [Co3(CO)10]=9*3+2*10=47 [H2Re4(CO)12]=2+21*4+2*12=110 [VCp(CO)4]=5+5+2*4=18 Mn2(CO)7(NO)3=7*2+2*7+3*3=37 HRe3(CO)14=1+21*3+2*14=92 [Fe(CN)5(NO)]=8+1*5+3=16 Поправьте меня,пожалуйста,если я не правильно посчитал электроны во внешней оболочке.
-
Если вы про первую реакцию,то там 100% спирта Если про вторую реакцию,то 10% Вы имеете ввиду это?
-
Посчитал, n(CH3COOH)=2,5 моль n(C2H5OH)=3,21 моль Значит, Kp= [эфир]*[H2O]/[CH3COOH]*[C2H5OH]= (X+0,1)*(X+0,1)/(X-2,5)*(X-3,21) Правильно или я что-то перепутал?
-
При нагревании до некоторой температуры 36 г уксусной кислоты и 7,36 г 100%-ного этанола в присутствии серной кислоты получена равновесная смесь. Эта смесь при действии избытка раствора хлорида бария образует 4,66 г осадка, а при действии избытка раствора гидрокарбоната калия выделяет 12,1 л оксида углерода (IV) (при н. у.). Найдите количество вещества сложного эфира (в молях) в равновесной смеси, которая образуется при нагревании до той же температуры 150 г уксусной кислоты и 200 мл 90%-ного этанола (плотность 0,82 г/мл) в присутствии серной кислоты в качестве катализатора. Решение CH3COOH+C2H5OH=CH3COOC2H5+H2O n(CH3COOH)=m/M=36г/60г/моль=0,6моль (избыток) mв-ва(C2H5OH)=mр-ра*W/100%=7,36г*100%/100%=7,36г n(C2H5OH)=m/M=7,36г/46г/моль=0,16 моль (недостаток) n(C2H5OH)=n(CH3COOC2H5)=0,16 моль H2SO4+BaCl2=BaSO4+2HCl n(BaSO4)=m/M=4,66г/233г/моль=0,02моль n(H2SO4)=n(BaSO4)=0,02моль H2SO4+2KHCO3+K2SO4+2CO2+2H2O n(CO2)=V/Vm=12,1л/22,4л/моль=0,540моль n(CH3COOH)=m/M=150г/60г/моль=2,5моль mр-ра(С2Н5OH)=V*p=200мл*0,82г/мл=164г mв-ва(C2H5OH)=mр-ра*W/100%=164г*90%/100%=147,6г n(C2H5OH)=m/M=147,6г/46г/моль=3,21 моль Объясните,пожалуйста,как делать дальше,а то я все перевёл моли,а теперь не знаю,как найти CH3COOC2H5
-
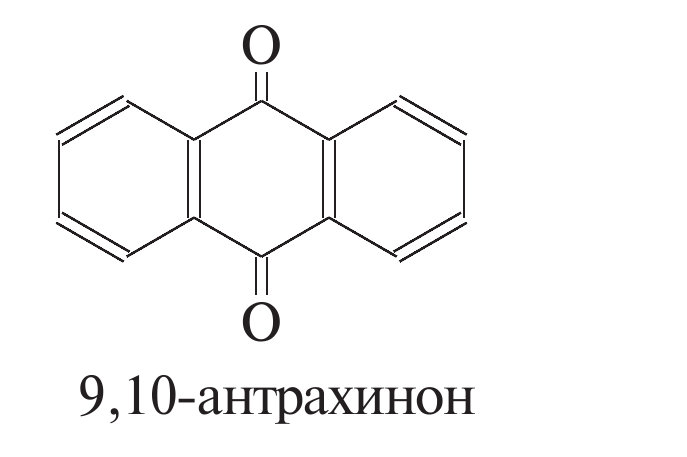
Почему 9,10-антрахинон? Может 1,4-антрахинон? Просто я не понимаю нумерации название веществ. Объясните,пожалуйста,откуда я должен называть сложные вещества,когда 2,3,4,5,6 бензольных колец
-
Здравствуйте! Порекомендуйте мне,пожалуйста,книги «про обработку ракетных топлив». Можно химическую,теория и т.д
-
- 1 ответ
-
- 1
-

-
Или нужно было по-другому решать?
-
Газовая смесь, имевшая объемный состав: кислорода 20%, азота 75%, оксида углерода (IV) 0,5 % и хлора 4,5%, была растворена в воде при 00С под давлением в 5 атм. Растворимость в воде при 00С кислорода 4,89 мл, азота 2,35 мл, оксида углерода (IV) 171 мл и хлора 461 мл на 100 мл воды. Вычислите массу указанных газов, содержавшихся в 1 л раствора. Решение n(O2)=0,2моль n(N2)=0,75моль n(CO2)=0,005 моль n(Cl2)=0,005 моль n(O2)=V/Vm=0,00489/22,4=0,00022моль n(N2)=0,00235/22,4=0,0001моль n(CO2)=0,171/22,4=0,0076моль n(Cl2)=0,461/22,4=0,02моль n(O2)=0,2+0,00022=0,2моль n(N2)=0,75+0,0001=0,75моль n(CO2)=0,005+0,0076=0,55моль n(Cl2)=0,005+0,002=0,025моль m(O2)=n*M=0,2*32=6,4г m(N2)=0,75*28=21г m(CO2)=0,0126*44=0,55г m(Cl2)=0,025*71=1,775г Задачка правильная решена?
-
А точно,не заметил. Спасибо большое!
-
В смысле? Я все написал. Просто если найти массу,то я объём умножаю на плотность,дальше уравнение клапейрона у меня другие числа получаются m=p*V=1,429*0,00489=0,006987 PV=nRT n=PV/RT=101,325*0,00489/8,314*273=0,00022моль M(X)=m/n=0,006987/0,00022=31,759=32 значит это кислород?
-
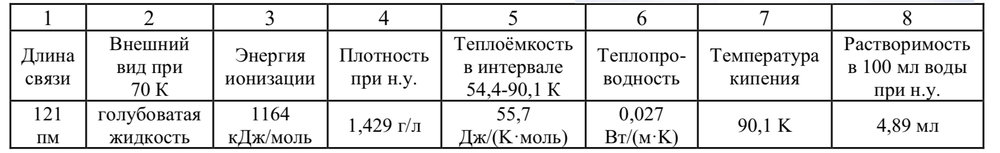
9. Сродство к электрону -42,38 кДж/моль 10. Теплота испарения 3,410 кДж/моль 11. Содержа ние в атмосфере 20,94 об. % 12. Сродство к протону -401,7 кДж/моль 13. Энергия связи 498 кДж/моль 14. Постоянный дипольный момент 0Д 15. Теплоёмкость в интервале 90,1- 298 К. 29,3 Дж/(K·моль) 16. Температура плавления 54,4 K Как из этих данных получить простое вещество?
-
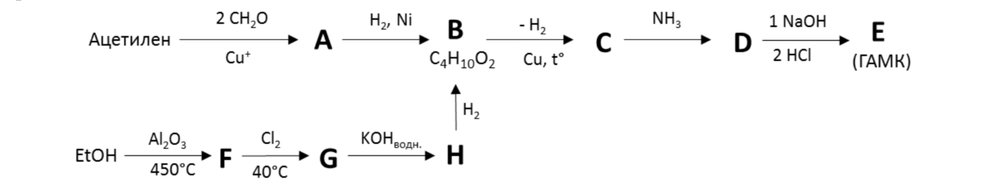
1) C2H2+2CH2O=OHCH2CCCH2OH 2) C4H6O2+2H2=C4H10O2 3) C4H10O2+H2+C4H8O2 4)C4H8O2+NH3=NH4+C4H7O2 5)C2H5OH=Al2O3=C2H4+H2O 6)C2H4+Cl2=C2H4Cl2 7)C2H4Cl2+2KOH(водный)=С2Н6O2+2KCl 8)C2H6O2+2H2=C2H10O2 9)C4H10O2+H2+C4H8O2 10)C4H8O2+NH3=NH4+C4H7O2 Вот дальше у меня не получается...
-
FeS2+H2SO4(разб)= Реакция идет?
-
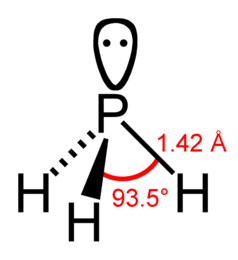
Простое вещество голубтоватого цвета,у которого длина связи 121пм Что за вещество? Думал,что это озон,но длина связи неподходит...
-
а массу надо найти природного газа это метан?
-
Принимая, что в природном газе метан составляет 90% (по объему), вычислите, какой объем займет (при н.у.) метан, содержащийся в 1м3 природного газа, находящегося в магистральном газопроводе под давлением 40 атм и при 00 С. Какова масса этого газа? 1m^3=1000л V=90%*1000л/100%=900л n=V/Vm=900л/22,4л/моль=40,18 моль Я запутался,потому что слишком много получается моль. Объясните,пожалуйста!
-