
Валерия123
-
Постов
14 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Валерия123
-
-
Установите строение мономера, если известно, что его димер при озонолизе превращается в смесь уксусного и изомасляного альдегидов. Написать уравнения реакций димеризации и озонолиза димера.
-
При получении водорода взаимодействием окиси углерода с водяным паром СО + Н2О(г) = СО2 + Н2 при 1000 К и Кр = 1,37. Вычислить равновесное количество водорода , если исходная смесь содержит 0,4 моль окиси углерода и 0,6 моль водяного пара
-
12 минут назад, yatcheh сказал:
P/P0 = exp(-dG/RT)
dG = -228572 - (-237129) = 8557
RT = 8.31*298 = 2476.38
P0 = 1 атм = 98100 Па
P = P0*exp(-3.455) = 3099 Па
По справочнику 3167 Па
спасибо большое!
-
-
-
-
4 минуты назад, yatcheh сказал:
Строите кривую титрования, находите точку эквивалентности, вычисляете содержание основного вещества в процентах. Всё остальное - индифферентные примеси.
Точка эквивалентности появляется на 5 мл
Вы бы не могли помочь с математическими расчетами?
Ответ должен быть 6,12%
у меня никак не получается, не понимаю, что не верно -
1. Навеску технического гидросалицилата натрия массой 0,8606 г растворили в мерной колбе вместимостью 50,00 мл и раствор довели до метки ледяной уксусной кислотой. При потенциометрическом титровании 5,00 мл полученного раствора 0,1 М HClO4 в ледяной уксусной кислоте (К = 1,030) получили следующие результаты:
V(HClO4), мл
4,00
4,20
4,40
4,60
4,80
5,00
5,20
5,40
Е, мВ
440
447
458
474
512
595
615
625
Построить кривые титрования и вычислить массовую долю (%) индифферентных примесей в препарате.
Нужна помощь в расчетах массовой доли примесей в препарате
-
2 минуты назад, yatcheh сказал:
Ошибка в методичке. Вместо деления на 0.5 умножили на 0.5.
Спасибо большое!)
-
3 минуты назад, yatcheh сказал:
Вам дана концентрация раствора щёлочи, и его объём. Отсюда вы можете вычислить количество КОН, израсходованное на нейтрализацию кислот.
Количество КОН равно суммарному количеству кислот в навеске 0.5 г. Средняя молярная масса кислот дана (274 г/моль) - отсюда вычисляется масса кислот. Делите эту массу на массу навески и получаете массовую долю кислот.
пробовала так считать, но выходит в ответе 26%, а в методичке указано, что ответ должен быть 6,71%, вот не понимаю, что упущено
-
12. Для определения массовой доли свободных кислот в льняном масле навеску 0,5000 г растворили в 20 см3 спирт - эфирной смеси и оттитровали 2,45 см3 0,2005 М раствора KOH в присутствии фенолфталеина. Определить массовую долю кислот, если средняя молярная масса кислот равна 274 г/моль.
Помогут хоть какие то мысли
-
Я имею в виду, что мне нужно объяснение почему именно он образует из всех галогенов)
6 минут назад, Paul_K сказал:Возможно, у меня был глюк, но по-моему, сначала вопрос был "почему не может".
А может он потому, что сравнительно большой атомный радиус позволяет ему разместить вокруг себя много атомов кислорода.
спасибо)
-
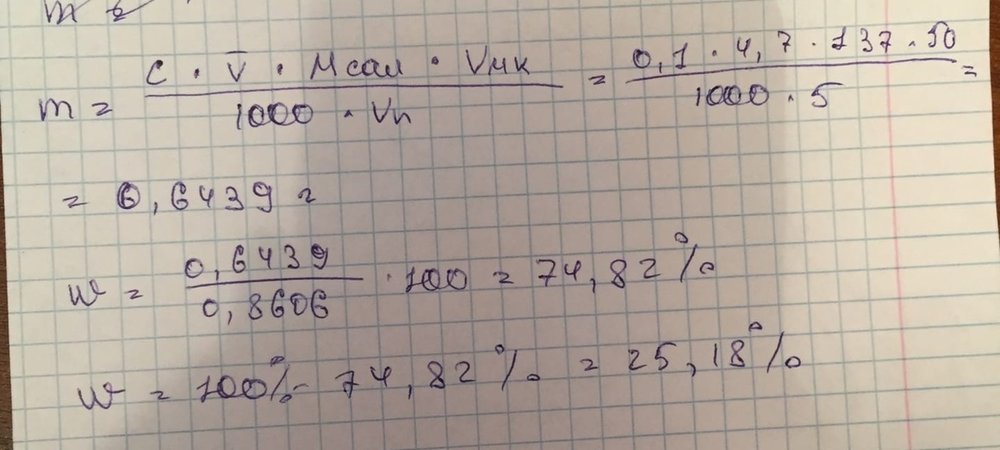
Задача на буфер
в Решение заданий
Опубликовано