-
Постов
20 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Exio
-
Стоит она, мягко говоря, дофига, я тут цены посмотрел... В Москве меньше 4000 за литр не нашёл, в основном, больше
-
Так вопрос не в том, как её хранить, а в том, почему некоторые люди (и весьма почтенные!) считают, что нет никакой 100% азотной кислоты, а максимум 60-70%.
-
Неоднократно слышал мнение о том, что азотной кислоты с концентрацией близкой к 100% не существует. Сначала такое говорили в школе, затем в универе седой профессор толкал такую мысль... В то же время, работая в лабе, сам пользовался дымящей азоткой с концентрацией около 100% и плотностью 1,5. Отсюда вопрос: откуда пошла такая легенда? Может, раньше технология не позволяла производить кислоту с концентрацией выше 60%, люди и привыкли?
-
Решили не делать ЯМР для примеси, но, возможно, сделаю, только уже осенью. Если очень интересно, могу потом эту тему поднять)
-
Выделил, но она белая
-
Если предположить, что образуется именно это, то становится ясно почему подобных примесей та же реакция, но с бензоксазолом, не давала.
-
И правда... Спасибо!
-
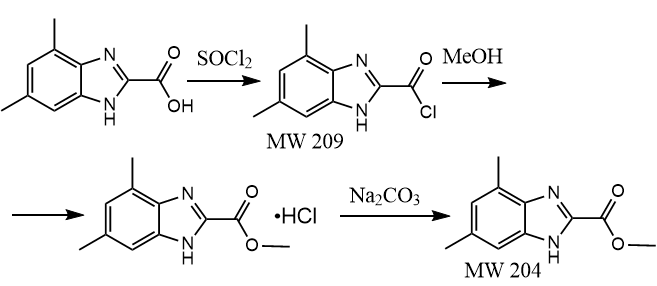
Добрый день! Вашему вниманию представляю головоломку. Провели следующую реакцию: ТСХ показала, что вместе с гидрохлоридом метилового эфира образовалось ещё что-то, идущее на фронте растворителя (хлороформ:метанол 9:1). После разрушения гидрохлорида появилось пятно метилового эфира, но старое осталось на фронте без изменений. В УФ (254 нм) пятно светится синим. Задача идентифицировать это неизвестное соединение. ЯМР-спектра нет. Пики масс-спектра: 226 [M]+ (100%), 227 (20%), 228 (64,8%), 229 (8,2%), 230 (10,2%), 231 (1%). Судя по соотношению M : M+2 : M+4 там может быть 2 атома хлора каким-то образом. В общем, буду рад любым идеям.
-
Если Вам не сложно, просто интересно Спасибо за предложения!
-
Полагаю, всё же в данном случае про таутомерию речь не идёт) Хотя с Вами вынужден согласиться.
-
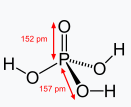
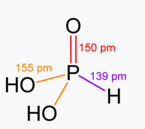
Фосфористая кислота H3PO3 на самом деле имеет строение (OH)2PHO, в ней один протон связан с атомом фосфора, поэтому он не является кислым. Кислые протоны только в OH-группах. Следовательно, K2HPO3 - полностью замещённое соединение, грубо говоря. Соль поэтому средняя. Ортофосфорная же кислота H3PO4 имеет строение (OH)3PO, следовательно, у неё все три протона кислые, а K2HPO4 - дважды замещённое соединение, в котором один протон остаётся кислым. Поэтому и соль называется кислой. Если так будет проще, вот картинки из википедии. Все протоны, что у атомов кислорода, могут быть замещены, остальные - нет.
-
Добрый день! Есть следующее соединение: Оно существует преимущественно в имино-кето-форме, это подтверждено. В связи с этим вопрос: как сдвинуть равновесие в сторону ароматической системы? Например, для того чтобы диазотировать аминогруппу. Дополнительный вопрос: какие, по-вашему, можно провести с ним реакции? Спасибо!
-
Мне знакомо это понятие
-
Добрый день! Объясните, пожалуйста, нюансы использования различных восстановителей. Интересуют следующие: Олово и хлорид олова в кислой среде, цинк в кислой и щелочной средах, дитионит натрия, диоксид тиомочевины, железо (II), формиаты, а также ЛАГ и боргидрид. Ясное дело, что у них различная восстанавливающая способность, но как их расположить по возрастанию силы? Какой когда применяется? Какой каким можно заменить? Какие ещё применяются? Где о них можно почитать?
-
Раствор оранжевый, продукт светло-жёлтый, да. Осадок в растворе также жёлтый.
-
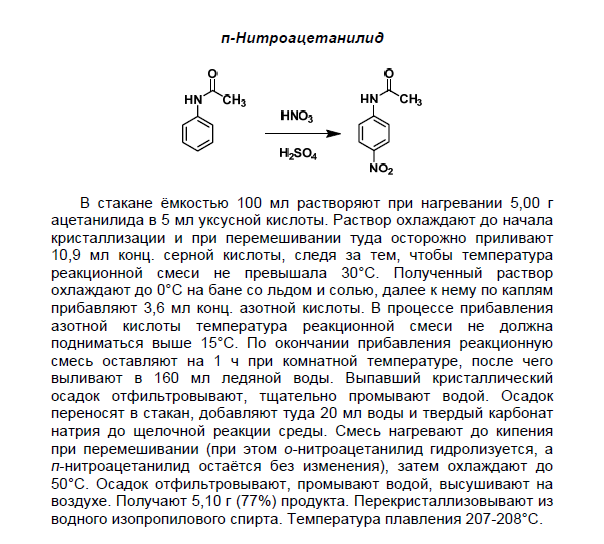
Здравствуйте! Синтезировал 4-нитроацетанилид по данной методике. На стадии отделения пара-изомера от орто- после фильтрования на фильтре осталось целевое соединение, а из маточника после остывания выпало какое-то ещё. Есть предположение, что это как раз орто-изомер. В методике как-то расплывчато сказано про гидролиз... Вопрос, в общем, вот в чём: может ли этот осадок быть орто-нитроацетанилидом, и есть ли смысл его пытаться выделить?
-
Здравствуйте, можно и мне список? victor130215@mail.ru