-
Постов
128 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Папа_школьника
-
-
21 час назад, Wittig сказал:
Самый работающий способ - получить в начале хлороформ по галоформной реакции из белизны и ацетона, а затем дохлорировать до четыреххлористого углерода.
В одной немецкой статье рекомендуется использовать хлорид иода в качестве катализатора, который образуется in situ просто от добавления в реакционную смесь кристаллика иода.
И, конечно же, нужно облучать ультрафиолетовой лампой, которую можно сделать из ДРЛ 125 (нагуглите как).
Лампу желательно поместить внутрь одного из горлышка колбы, чтобы лучи не поглощались стеклом. Поэтому колбу желательно иметь трехгорлую. И все делать под вытяжкой.
В этой книге на 145 странице подробно описано получение CCl4:
https://1lib.eu/book/1100590/1ed275
Правда требуется знание английского.
Добрый день,
подскажите пожалуйста, где можно скачать такую шикарную немецкую книгу?
Спасибо
-
Задача такая: При обработке карбида алюминия раствором 20%-ной соляной кислоты массой 346,75 г выделилось 6,72л (ну) газа. Определите массовую долю соли в полученном растворе.
Вроде как из вопроса ("долю соли") подразумевается, что реакция - именно с кислотой, а не с водой. Но ведь карбид алюминия среагирует и с 20% кислоты, и с 80% воды? Или он сначала будет реагировать только с кислотой, пока она не будет израсходована, и только потом - с водой (если карбид останется)?
Понятно, что можно найти общую прореагировавшую массу карбида, поскольку дан объем выделившегося аммиака, а пропорция моль карбида к аммиаку одинакова в обеих реакциях (1:3). Но что заставляет карбид реагировать именно с кислотой, а не с водой?
Или гидроксид алюминия из реакции с водой всё равно потом прореагирует с кислотой, так что в результате все равно в растворе будет только хлорид алюминия?
Какая последовательность реакций?
Спасибо.
-
02.04.2020 в 21:29, Knecht сказал:
В своей работе со школьниками постоянно сталкиваюсь с очень низким уровнем знания и понимания химии. [Моё личное мнение - это связано с неудачным подходом к химии в школьной программе, в результате чего только единицы способны осилить школьную программу по химии.] Я считаю, что эту ситуацию можно и нужно исправлять - в частности, за счёт создания игр.
Учебников толковых нет. В тех, что есть - бардак. Много отрывочных сведений предлагается именно запомнить, а не понять. Плохой (или неполный) учебник + Среднего уровня учитель = уже дают Плохие знания по химии
-
57 минут назад, бродяга_ сказал:
закономерность есть но она многократно сложней такой схемы вертикаль - горизонталь. разве что в одной группе
к примеру галогенов.
здесь посмотри...
О, нет, я нечто гораздо более примитивное имел в виду. Например, таблица, где название строки, например, "белое", а по столбцам пошли "творожистое", "порошок", "блестящее", "матовое" и т.п. То есть не внешние свойства по закономерностям предсказать, а наоборот - по внешнему виду вещество определить.
-
9 часов назад, M_GM сказал:
Спасибо, понятно. А есть на просторах интернета какая-нибудь мега-таблица, типа определителя веществ по цвету и еще по каким-нибудь качествам? Например, по вертикали цвет, по горизонтали что-нибудь ещё? Так сказать, для азов/начал качественного анализа? Понимаю, что вопрос "а есть ли в интернете" дурацкий, и сам поищу, но возможно вы знаете наилучший источник?
-
-
4Fe(OH)2 + 2H2O + O2 = 4Fe(OH)3
Условия: реакция уравнена без электронного баланса
На вашем уважаемом сайте есть такая реакция. А как это? Нерастворимый гидроксид железа II обдаем кипятком и горячим кислородом?
-
Как получить из Fe2(SO4)3 -> FeI2?
Читаю, что Fe3+ и I- при встрече дают Fe2+ и I2...
Очень много йодоводорода добавить?
Fe2(SO4)3 + 6HI = 2FeI2 + I2 + 3H2SO4?
2F3+ + 6I- = 2Fe2+ + I2 + 4I-
-
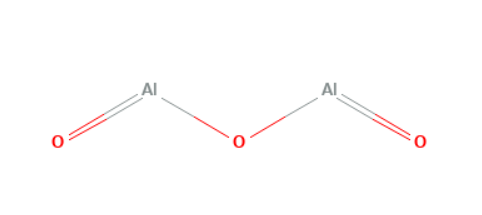
Почему на PubChem структура изображена углами на атомах Al? Я понимаю, почему угол на центральном О - там sp3 гибридизация, на всех 4-х орбиталях есть электроны, и это две из вершин тетраэдра. Но разве у атомов Al не sp-гибридизация? Там же всего 3 электрона на 3-х орбиталях, из которых одна - это пи-связь, то есть остается две сигма-связи и значит - должна быть линейная структура?

-
Не могли бы вы пояснить, или кинуть ссылку, где почитать,
что такое ЛЕТУЧИЕ и НЕЛЕТУЧИЕ оксиды и кислоты, что это означает,
и если оксид летучий, то значит ли это, что и кислота летучая (и наоборот), или могут быть несоответствия.
Вот читаю, что и твердые оксиды бывают летучими (например, P2O5, N2O5, SeO2), и это кажется совсем странным...
-
Может ли такая реакция идти не в растворе? То есть без того, чтобы кислотный оксид принимал воду и превращался в кислоту?
Например,
Ca(HCO3)2 + SO3 = ?
Потому как если в растворе, то это опять гидрокарбонат с кислотой, где сама кислота в ионном уравнении не участвует (вроде бы)
-
Пытаюсь смоделировать реакцию гидрокарбоната кальция с кислотой (какой-нибудь). Взял HCl, получается вот что:
Ca(HCO3)2 + HCl
Ca2+ H+ H+ CO32- CO32- H+ Cl- = H2O вода CO2 газ H+ Cl-
то есть кислота вообще ни при чём? То есть просто перегруппировываются катион и 2H+ ? Так это наверное в любом растворе произойдет, и в воде тоже? Мне важно понять, "реакция с кислотой" - это свойство гидрокарбоната кальция, или нет такого свойства как такового?
В отличие, например, от "реакции с щелочами", где очевидно OH- от щелочи будут потрачены на воду, типа
2KOH + Ca(HCO3)2 = 2H2O + K2CO3 + CaCO3
и соответственно такая реакция несомненно существует как отдельное свойство.
-
Только что, M_GM сказал:
Но причина этой реакции в образовании осадка, а не в силе кислот
Вот на этом как раз сейчас моё познание химии пробуксовывает. Тут же два фактора складываются вместе - и хлорид серебра в осадок (это бесспорно!), но и HNO3 более слабый электролит, чем HCl, разве нет? Если бы какой нибудь другой хлорид был и не выпадал в осадок, всё равно бы равновесие было бы смещено вправо, хоть и в меньшей степени, так ведь?
-
Только что, M_GM сказал:
основнуюкислую соль в реакции 2:Пардон, спешил, перепутал )
Только что, M_GM сказал:Но это все несколько притянуто
Самое простое - считать, что после растворения осадка Zn(OH)2 раствор содержит некоторый избыток HCl и потому протекает его реакция с нитратом серебра:
HCl + AgNO3 = AgCl осадок + HNO3
Действительно, это самое простое! Мне в голову не пришло. Сильные кислоты вытесняют слабые. Спасибо!!
-
Только что, Инфинити сказал:
Мне интересно, а где сам школьник?
Или вы он и есть?
Далеко пойдете, если будете за свое чадо все жевать.
На выпускных суфлировать через радиомикрофон будете? 300%.
Вроде взрослый мужик, а не понимает, что надо от сиськи уже отлучать.
Вроде взрослая баба, а не в курсе, что с советами по воспитанию детей к чужим людям не лезут. Вали отсюда, если по предмету нечего сказать.
-
Только что, Инфинити сказал:
Папа у Васи силен в математике, учится папа за Васю весь год, где это видано, где это слышано, папа решает, а Вася сдает!)))))))))))))))))))))))
Тут же есть для шуток "Курилка"? А здесь ждут "Помощи". От вас, уважаемая, я никогда никаких советов не слышал, и как-нибудь без ваших подколок проживу.
-
В пробирку, содержащую раствор сульфата цинка, по каплям до полного растворения осадка добавляли раствор гидроксида калия. Далее в полученный раствор по каплям добавили соляную кислоту, при этом сначала наблюдали образование осадка, а затем его растворение. В конечный прозрачный раствор добавили раствор нитрата серебра. Напишите не менее 7 УХР, которые протекают при указанных операциях.
Мой вариант:
1. ZnSO4 + 2KOH = K2SO4 + Zn(OH)2 в осадок
2. 2KOH + Zn(OH)2 = K2[Zn(OH)4] растворение осадка
3. K2[Zn(OH)4] + 2 HCl = 2 KCl + 2 HCl + Zn(OH)2 снова осадок
в ионном виде: 2K+ Zn(OH)42- 2H+ 2Cl- = 2K+ + Zn(OH)2 + 2H2O+ 2Cl-
сокращенно: [Zn(OH)4]2- + 2H+ = Zn(OH)2 + 2H2O
4. Zn(OH)2 + 2 HCl = ZnCl2 + 2H2O
5. ZnCl2 + 2 AgNO3 = 2 AgCl осадок + Zn(NO3)2
Стал думать, куда еще 2 УХР приткнуть. Нашел промежуточную реакцию для 4 (кислая соль):
4а. 2 Zn(OH)2 + 2HCl = 2 Zn(OH)Cl + H2O
По аналогии попробовал сформулировать основную соль в реакции 2:
2а. KOH + Zn(OH)2 = KHZnO2 + H2O
Но вот тут уже не уверен, правильно ли это, и как из этого получается комплексная соль K2[Zn(OH)4]. У сына в распечатке было правило - если в расплаве, то средняя соль (цинкат), если в растворе - то комплексная. Про промежуточные стадии ничего не сказано. Может ли такой кислый цинкат в растворе вообще образоваться? Ну предположим, из HO-Zn-OH обе H+ отрываются и уходят - одна в H-OH, другая продолжает быть в растворе. Или нет? KHZnO2 вообще растворим или нет? Или он плавает в виде K+ и HZnO2-? Пишут, что кислые соли более растворимы, чем средние. Как из этого комплексная соль получается?
-
21 час назад, Леша гальваник сказал:
А у алюминия окисная пленка мешает - снять бы ее в растворе гидроксида натрия (крота) примерно 100 г/л содержание (там сами увидите как снимается - поначалу редкие пузырьки, потом чаще, еще чаще, и вот уже пузырит вся поверхность - это буквально минуты времени), потом промыть и в раствор медного купороса.
С алюминием (через 1 час):
1. В ЦЕНТРЕ - как советовал уважаемый Леша Гальваник, гранулу алюминия бросил в раствор NaOH (чисто наобум), пошли пузырьки, подержал полминуты, сполоснул и положил в купорос. Явно виднеется желтый налет.
2. СЛЕВА - просто гранула алюминия без добавок, для контроля. Визуально никаких изменений.
3. Наконец, СПРАВА - с поваренной солью. Пузырилось так, что пробка слетала.
Всем спасибо, и спокойной ночи!
-
12 часов назад, Krolikoff сказал:
Скрепки обычно делают никелированными, чтобы не ржавели. Доступный образец железного изделия - обычные неоцинкованные гвозди
СЕГОДНЯ!!!
1. Слева - пол-гвоздя через 1 час после опыта. Раствор: 6г 5-водного купороса на 125мл воды.
 8 часов назад, aversun сказал:
8 часов назад, aversun сказал:Лучше добавьте какой-либо растворимой соли хлора, хлорида. Ионы хлора сильные катализаторы коррозии
2. В ЦЕНТРЕ - пол-гвоздя с добавленной поваренной солью (йодированной, кстати - другой нету)
3. СПРАВА - чисто для контроля, развел порошок железа (раствор без соли). Изначально порошок был темно-серый, а здесь это видимо уже медь
-
20 часов назад, Леша гальваник сказал:
Имхо, скрепка как минимум никелированная (в руках бы подержать/посмотреть)
2. Хоть наверное и никелированная, а всё же немало меди выделилось
3. А вот что осталось от гранул цинка (раствор сульфата, без соли). Раствор кстати стал полностью прозрачным, и нейтральным
СЕГОДНЯ вместо скрепки взял гвоздь, а также пытался убрать оксидную пленку с алюминия
-
ПОДВОЖУ РЕЗУЛЬТАТЫ!!! Сначала вчерашний опыт, без всякой соли и прочих ухищрений....
1 час назад, yatcheh сказал:1. В точности как предсказывал уважаемый Yatcheh, после суток гранула алюминия выглядит вот так:
-
 1
1
-
-
2 часа назад, Nemo_78 сказал:
И последний вопрос, если позволите. Теперь, когда в растворе плавает много катионов Al3+ (из оксида и после ОВР Al0 с Cu2+) и одновременно CuOH+ от неполного гидролиза сульфата, будет ли (1) Al3+ на себя оттягивать OH- от меди (=> Cu2+ AlOH2+), или (2) он будет свой оснОвный катион формировать AlOH2+ , так что сразу будет и CuOH+ и AlOH2+ в растворе, или (3) пока гидролиз не закончится в сторону полного Cu(OH)2, катиону Al3+ ничего не перепадет?
2 часа назад, Nemo_78 сказал:2Al + 3Cu2+ ==> 2Al3+ + 3Cu
а может идти сразу 2 реакции?
2Al + 3Cu2+ ==> 2Al3+ + 3Cu
и 2Al + 6H2O = 2Al(OH)3 + 3H2
Это я к тому, что если увижу пузыри, чтоб знать, что это.
-
Только что, Nemo_78 сказал:
Но и поваренная соль способна хорошо разогнать процесс восстановления, о чём Вам уже писали и aversun, и Paul_S, если не ошибаюсь
Ааа! так я не понял, о какой соли Paul_S писал... думал, просто надо добавить того же сульфата
-
Только что, Nemo_78 сказал:
Спасибо! Может, тогда раствор подогреть? Больше H+ -> сильнее реакция с Al2O3 -> быстрее Cu2+ соприкоснётся с Al0 ?

.thumb.jpg.8a6f751a33dd10b2b5836f441b0d541b.jpg)






Почему HClO4 не окислитель как HNO3?
в Решение заданий
Опубликовано
Чем хлор в с.о. +7 хуже азота в с.о. +5? Почему в реакции HNO3 с металлом некоторым атомам азота удается понизить с.о. , например до N2, а никаким атомам хлора в HClO4 не удается? По крайней мере в школьной методичке окислители - это только HNO3 и конц. H2SO4.
Я было подумал, в геометрии аниона дело - но вот в SO42- сера плотно окружена кислородом, но тем не менее отрывается, чтобы дать S или там H2S...
Почему не хлор? Есть этому интуитивное или логическое объяснение?
Спасибо