
MoreFeeling
-
Постов
48 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные MoreFeeling
-
-
В 08.12.2023 в 04:11, ash111 сказал:
В этой статье комплекс супрамолекулярный. Содержит нужный мне фрагмент, но, конечно, молекула намного больше там. Видимо, таких соединений отдельно там нет, но спасибо за помощь
-
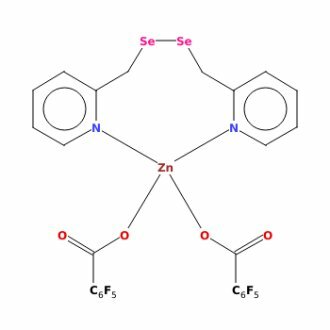
Здравствуйте. Возникла проблема. В базе CCDC имеется несколько кристаллографических формул соединений. Пыталась найти статьи в поисковике, где фигурирует сам синтез от авторов и характеристики, но, к сожалению, не смогла. Быть может, есть у кого-нибудь доступ к scifinder, например, пробить? CCDC 1912976 и CCDC 766453. Фотографии прилагаю. Заранее благодарю!
-
Подскажите, пожалуйста, возможна ли реакция между 2-оксопропил тиоцианатом (CH3COCH2SCN) и фенолом/тиофенолом? Если да, то какой продукт будет?
-
В 14.02.2023 в 22:24, Lеоnid сказал:
Посмотрел - хорошо растворима в хлороформе. Это хорошо подойдет вам, хлороформ не смешивается с водой и легколетуч.
Спасибо. Тоже о нём подумала
-
В 14.02.2023 в 21:25, Nemo_78 сказал:
Для этого, поди, абсолютированный этанол понадобится.
Ну, фармтехнологические прописи рекомендуют для удаления остаточного спирта ток осушенного прохладного воздуха, а лучше азота (с температурой не выше +12 по Цельсию) в целях минимизации потерь целевого продукта.
Хотя, наверное, и аккуратное вакуумирование без нагрева тоже поможет.
Спиртовой раствор можно помучить,конечно, а метод возгонки мокрой камфоры непригоден по типу как иод сублимируют?
-
В 14.02.2023 в 20:43, Lеоnid сказал:
Следы она будет содержать всегда. Уточните требования к следам - ppm, ppb?
Для меня главное, чтобы при дальнейшем её использовании не происходила реакция взаимодействия следов воды с амидом натрия, который с камфорой встретится в реакционной колбе
В 14.02.2023 в 20:43, Lеоnid сказал:Опять-таки - очень испаряется эта камфора. От спирта на чем гнать, чтоб без больших потерь? Если на роторе, то боюсь, что забьёт установку.
-
Здравствуйте. Из камфорного спирта путём разбавления водой была получена сама камфора. Теперь необходимо, чтобы она не содержала следов воды. Как лучше высушить сей продукт? Была идея с сублимацией. Возможна ли она и какие есть особенности?
-
-
Подскажите, пожалуйста, может быть есть какие-либо справочники по растворимости неорганических веществ? Интересует борная кислота. Необходимо подобрать такой растворитель, чтобы борная не растворялась (отделить от орг.вещества нужно). Воду нельзя использовать
-
В 27.01.2023 в 04:57, yatcheh сказал:
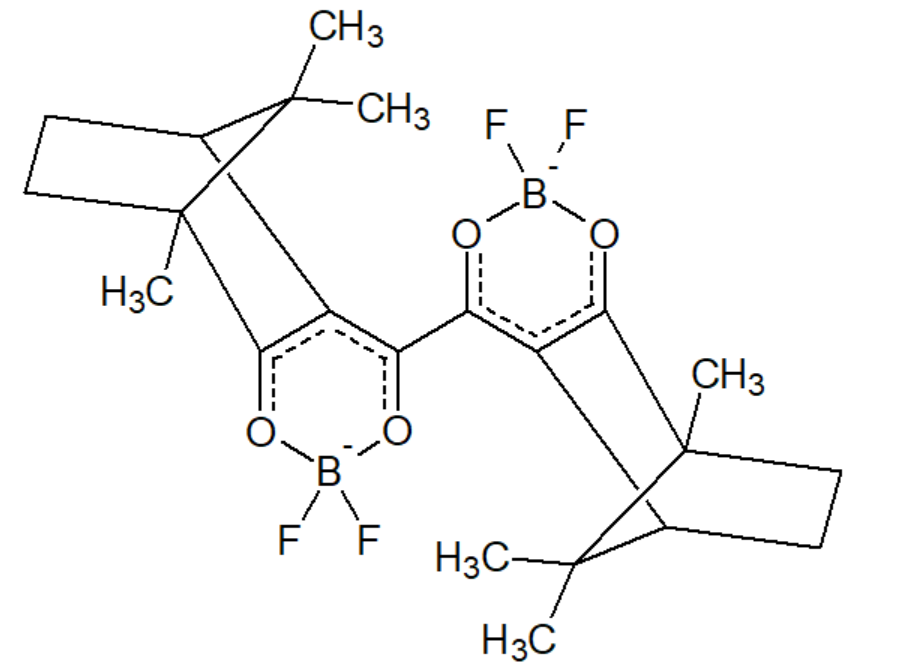
Исходная структура - кетоенол (как на левой картинке). Могут ли в теории в молекуле находиться оба цикла с BF2-фрагментами?
-
Подскажите, пожалуйста, с точки зрения различных стерических и электронных факторов, может ли получаться и существовать подобное соединение?

-
В 30.11.2022 в 19:51, yatcheh сказал:
В хлороформе енолизация будет 100%-й, а в воде?
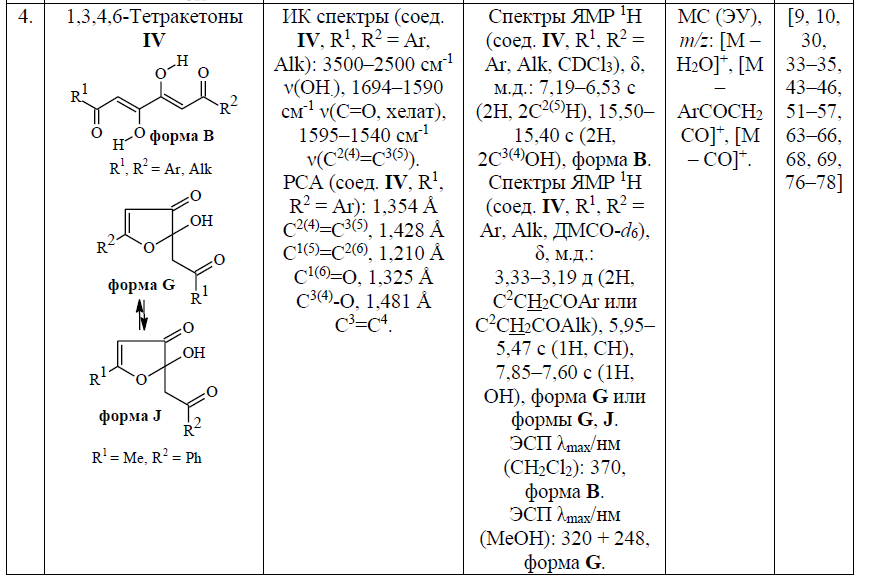
Я поискала и нашла информацию, что в полярных растворителях большинства 1,6-диалкил- и 1,6-диарилзамещенных тетракетонов наблюдается равновесие между линейной формой B и циклическими оксофурановыми формами G или J. Если R1 = Me, R2 = Ph, то формы G будет 84% (это сведения для раствора ДМСО). Но с другой стороны, есть факт cуществования тетракетонов в водном растворе в диоксодиенольной форме. Это вероятно, связано с небольшим индуктивным эффектом алкильного заместителя, который не затрудняет поляризацию карбонильных групп тетраоксоскелета молекулы, что приводит к возникновению эффективного заряда на углероде метиленовых групп, протоны которых становятся подвижны, и после енолизации молекулы наблюдается образование сопряженного бис-хелатного фрагмета, стабилизированого ВВС. Данному процессу, вероятно, способствуют полярные молекулы воды, облегчающие миграцию протонов метиленовых групп к кислороду

-
В 30.11.2022 в 19:51, yatcheh сказал:
Развал теоретически возможен, как ретро-сложноэфирная конденсация. Но тогда у вас как минимум - ацетофенон останется, а он должен экстрагироваться, и вес при этом уменьшится максимум вдвое. Да условия для такой ретро-реакции нужны жёсткие.
А вы уверены, что в избытке кислоты ваш тетракетон сохранится в енольной форме? Енол-то должен экстрагироваться хлороформом в силу малой полярности и связанных ВМВС гидроксилов. А вот кетон может и не полезет. В хлороформе енолизация будет 100%-й, а в воде?
Это теоретическое предположение. То есть в избытке кислоты в водном растворе может быть кето-форма, которая не экстрагируется, поэтому выхода продукта в экстракте толком нет? Как же тогда быть и чем достать продукт? Мне продукт нужен для дальнейшей реакции комплексообразования с образованием двух циклов. Думаю, кето-форма тоже будет применима.
-
Здравствуйте. Известно, что натриевое производное растворимо хорошо в воде. В органике значительно хуже. Тетракетон, соответственно, наоборот. При растворении в воде соли, затем при добавлении 10% соляной кислоты к этому раствору должен происходить переход к енольной форме. Может ли, чисто теоретически, молекула тетракетона под действием кислоты гидролизоваться и распасться на две части? Смущает ещё факт того, что соли для перевода берется много, но после экстрагирования хлороформом раствора с добавленной кислотой и упаривания экстракта, выходят какие-то десятки мг продукта. Куда остальное могло бы деться? Среда водного раствора была кислая, поэтому вряд ли соль могла остаться в воде.

Вот сама соль
-
В 11.11.2022 в 07:47, Paul_S сказал:
Метанол добыть не удалось, а в этаноле не особо хорошо. Более менее ещё в этилацетате, но тоже с трудом. Частично то растворяется, но очень плохо. Обычно в тетракетон переводят обработкой раствором кислоты по статьям. Думаете, водой одной тоже может гидролизоваться до кетона?
-
Здравствуйте. Занятный вопрос на ум пришел. Если вещество практически не растворяется в органике, но хорошо растворимо в воде, то можно ли провести экстракцию вещества из водного раствора тем же серным эфиром? Будет ли оно переходить в органику в таком случае? Вообще необходимо синтез провести в орг.растворителе, но для этого необходима гомогенная система. Соединение такого рода:

-
В 26.10.2022 в 20:18, yatcheh сказал:
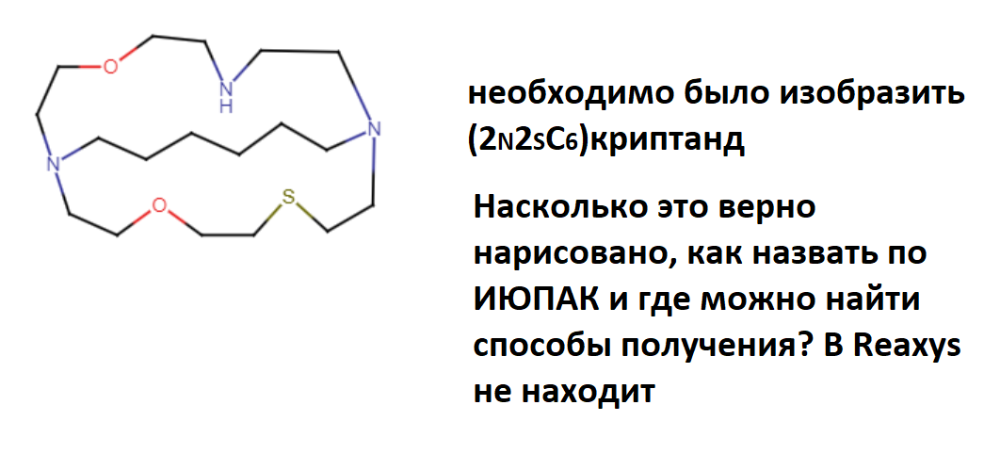
4,16-диокса-13-тиа-1,7,10-триазабицикло[8.8.6]тетракозан
Спасибо!
-
В 25.10.2022 в 23:09, yatcheh сказал:
верно
А по ИЮПАК то как назвать?
-
-
Здравствуйте. Мне необходимо для дальнейших реакций получить тетракарбонильные соединения по типу соединений(6 и 7). Нашла способ представленный на фото, но он трудоемкий по исполнению. Насколько поняла, данные соединения при получении из натриевых производных (1-5) при комнатной температуре осмоляются. Соли достаточно устойчивы. В идеале мне необходимо провести хелатирование для получения комплексных соединений. Пробовала из солей напрямую получить, но полагаю, что в процессе отрыва катиона натрия происходит то же самое осмоление, а проведение реакции при охлаждении колбы смесью соли со льдом не дало результатов. Осложняется еще все тем, что натриевые соли практически не растворяются в органике. Разве что в этилацетате и то при нагревании. Воду для синтезов нельзя использовать. Может быть, у кого-то есть опыт проведения подобных экспериментов. Что можно предпринять?

-
В 17.09.2022 в 01:52, yatcheh сказал:
Походу это просто сдвиг в герцах. Шобы получить м.д. надо поделить герцы на частоту в мегагерцах. Т.е. 146 Гц = 146/60 = 2.43 м.д. А уж от чего эти м.д. - зависит от стандарта.
В герцах обычно дают константы расщепления (на то они и константы, что от частоты не зависят), но в 60-х годах, видимо, ещё не было устоявшейся практики.
Кстати, Вариан-60 для того времени - крутейший прибор. Я такой застал в конце 80-х, и он считался весьма приличным.
Спасибо большое!
-
В статье 60-х прошлого века описан ПМР: "Chemical shift (c. /sec.) - 146, Varian HE60 spectrometer (6 x l0 в 7 c./sec).Chemical shifts are in C.P.S - 138, 143, Varian A-60 spectrometer."
Как это перевести в м.д.? (перевод в шкалу м.д.)
-
Здравствуйте, подскажите, пожалуйста

-
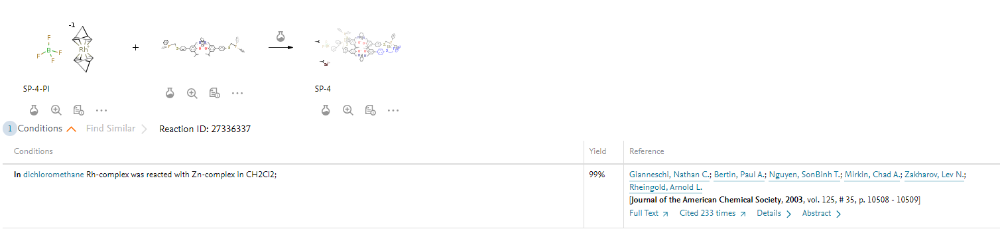

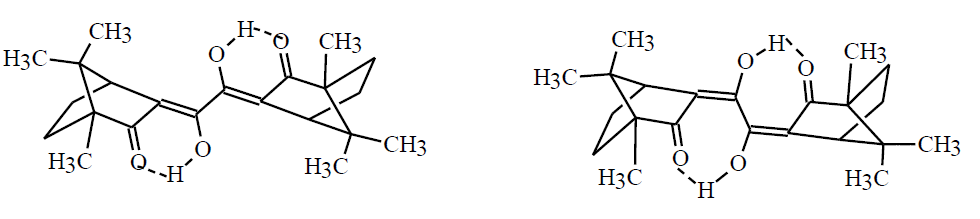
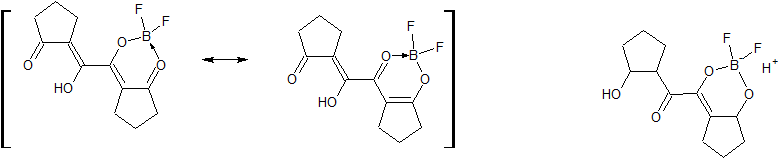




Выходные данные статей
в Решение заданий
Опубликовано
Благодарю!