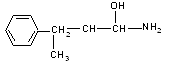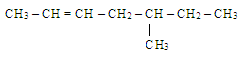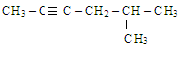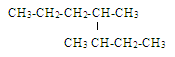Danivel
Пользователи-
Постов
59 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Danivel
-
Спасибо большое
-
Реакция 1-го порядка имеет энергию активации 25 ккал/моль и предэкспоненциальный множитель 5·1013с-1. При какой температуре время полураспада для данной реакции составит 1 мин? Объясните, пожалуйста, как решать. 🙏🙏🙏 Я так предполагал, что надо как-то через уравнение Аррениуса, но это не точно, ибо я так и не понял как именно.
-
Определите молярный объем (м3/кмоль) жидкого дейтерия при 18,65К, если при этой температуре dP/dT равно 4,1·106Па/град, теплота плавления дейтерия равна 196 Дж/моль и молярный объем кристаллического дейтерия составляет 2,05·10–2м3/кмоль.
-
Температура перехода ромбической серы в моноклинную под нормальным атмосферным давлением равна 95,6°С. Теплота полиморфного превращения Sромб ↔ Sмонокл составляет 13,07 Дж/г. Изменение температуры плавления при повышении давления на 1 Н/м2равно 3,94·10–7град/Па. Вычислить разность удельных объемов ромбической и моноклинной сера. Объясните, пожалуйста, как решать данную задачу 🙏🙏
-
Определите максимальное число фаз и число степеней свободы равновесной системы. 4Fe+3O2=2Fe2O3 Пожалуйста, объясните как решать, и дайте формулы для решения. 🙏🙏🙏 Я нашел формулу для числа степеней свободы: f=К-Ф+2, где К компоненты и Ф фазы. Число компонентов К, К = s - n - m , где s - число веществ,n - число независимых химических реакций,m - число соотношений между концентрациями веществ или составами фаз. к= 3-1-0=2 (вроде) Но как найти число ФАЗ не понимаю.
-
(0,25+х)*(0,5+х)/(0,5-х) = 33,4 (Кр по условию 33.4, вы наверное перепутали) х=0.9727 р(C2H6)=(0,5-9727)= -0.4728 МПа; р(C2H4)=(0,25+9727)= 1.2228 МПа; р(H2)=(0,5+9727)= 1.4728 МПа "Но, в заключение признаюсь, что я тут несколько затупил и напрасно усложнил решение задачи. На самом деле, все эти переходы к концентрациям, Па - МПа, и обратно были ... совершенно не нужны! Зато вспомнили связь давлений и концентраций, Кр и Кс " Для меня это наоборот хорошо, с этим дистанционным обучением ничего толком не объяснили. Так что, чем больше я сейчас вспомню/выучу/пойму тем лучше. Спасибо.
-
Здравствуйте, пожалуйста, проверьте правильность решения данной задачи. Если, что-то не так скажите. Заранее спасибо. Найти соотношение констант равновесия при 500К и 600 К для реакции HgCl2 + 2KBr=HgBr2 + 2KCl, если тепловой эффект этой реакции составляет 16,8 кДж. Решение: HgCl2(кр)+2KBr(кр)=HgBr2(кр)+2KCl(кр) ΔH=(H(HgBr2)+2*H(KCl))-(H(HgCl2)+2*H(KCl))=(-169,9+2*(-436,56))-(-228,24+2*(-393,5))=-27,48 K=(ΔH*dT)/(8,413*T2) где, dT=16,8 K=0,00015 K=0,00022 K2/K1=1,46
-
Константа химического равновесия Кр реакции С2H6=C2H4 + H2 при 1500 К равна 33,4. Определите направление процесса и парциальные давления компонентов системы в конце процесса, если в начале реакции их значения следующие (МПа) : P(C2H6)=0,50,P(C2H2)=0,25,P(H2)=0,50 Пожалуйста, объясните как решать, и дайте формулы для решения.🙏🙏🙏
-
Формула дипальмитоолеата. Напишите ее пожалуйста.
-
Помогите пожалуйста с органической химией. Прорешал все тестовые задания, кроме этих. Тут или вообще не знаю или предполагаю, но очень не уверен. Заранее спасибо. 5. В схеме превращений H2CH3COOH CH3CHO→ X1 →--------------- → X2 веществом Х2 является а) диэтиловый эфир; б) глицерин; в) этилацетат; г) диметиловый эфир? 6. С помощью какого реагента можна отличить целобиозу от сахарозы? а) бромная вода гидрогенизация; б) раствор щелочи; в) оксид меди (1); г) реактив Фелинга? Тут вроде, А. 9. Наименьшей основностью обладает соединение а) аммиак; б) анилин; в) метиламин; г) диметиламин. Тут вроде, А. 9. Реакция, протекающая с участием гидроксильных групп в молекуле галактозы Nit0 а) С6Н12О6 + H2→?; б) С6Н12О6+ [Ag(NH3)2]OH→?; в) С6Н12О6 + Cu(OH)2+ NaOH→?; в) С6Н12О6+ Br2+ H2O →? 9. С помощью какого реагента можна отличить лактозу от трегалозы? а) оксид меди (I); б) реактив Селиванова; в) реактив Фелинга; г) бромная вода. 10. Возможным продуктом реакции взаимодействия азотистой кислоты и первичного ароматичного амина будет: а) С6Н5-N≡NCl; б) С6Н5-N=N-CH3; в) С6Н5-N-(C6H5)2; г) Н2N – C6Н12-NH2? 10. Укажите число асимметрических атомов углерода в молекуле 2-аминокапроновой кислоты а) 0; б) 1; в) 2; г) 3; д) 4. Тут вроде, Б. 10. Реакция, при помощи которой можно отличить трипептиды фен-гли-ала и сер-гли-ала а) с нитратом свинца (II); б) с нингидрином; в) биуретовая; г) ксантопротеиновая. 9. Назовите соединение: смотрите прикрепленный рисунок а) 2-метил-2-фенил-3-ол-пропанамин; б) 4-амино-2-фенилбутанол-3; в) 4-амино-2-бензилбутанол-3; г)1-амино-1-ол-3-метил- 3-фенилпропан. Тут вроде, Г.
-
Назовите углеводород: 2-метил-4-гексин; б) 5-метил-2-гексин; в) 5-метил-2-гептин; г) 5-метил-2-гептен.
-
-
1. Назовите соединение: а) 2-изопропилпентан; б) 3,4-диметилгептан; в) 4,5-диметилгептан; г) 3-метил-2-этилгексан
-
Название соединения по международной номенклатуре соответствует Н3С - С = СН - СН - СН2- ОН а) 2-метил-4-метилпентенол-3; б) 2,4-диметилпентен-3-ол-1; в) 1-гидрокси-2,4-диметилпентен-3; г) 2,4-диметилпентен-3-аль | | СН3СН3
-
неа, все один в один со сборником.
-
На кондуктометрическое титрование пробы, полученной из 3 г технического препарата лимонной кислоты, затрачивают 5,15 см3 0,0100 н раствора хлороводородной кислоты. Найти содержание (%) лимонной кислоты (молярная масса 192,13 г/моль) в анализируемом препарате.
-
Рассчитать навеску хлорида натрия, необходимую для приготовления 250 см3 0,0500 н раствора, используемого для установления титра раствора нитрата серебра. Дайте формулу или скажите как, и я сам решу. Спасибо.
-
На кулонометрическое титрование уксусной кислоты генерированными ионами ОН- затрачивают 23 с при силе тока 8 мА. Общий объем анализируемого раствора 100 см3, для титрования отбирают 10 см3 раствора. Вычислить массу (мг) уксусной кислоты в анализируемом растворе. Скажите как или дайте формулу, и я сам решу. Спасибо.
-
Вычислить объем 0,1000 н раствора AgNO3, который расходуется на титрование 25 см3 0,1034 н раствора бромида калия. Скажите как или дайте формулу, и я сам решу. Спасибо.