
Danivel
-
Постов
59 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные Danivel
-
-
Реакция 1-го порядка имеет энергию активации 25 ккал/моль и предэкспоненциальный множитель 5·1013с-1. При какой температуре время полураспада для данной реакции составит 1 мин?
Объясните, пожалуйста, как решать. ???
Я так предполагал, что надо как-то через уравнение Аррениуса, но это не точно, ибо я так и не понял как именно.
-
-
Температура перехода ромбической серы в моноклинную под нормальным атмосферным давлением равна 95,6°С. Теплота полиморфного превращения Sромб ↔ Sмонокл составляет 13,07 Дж/г. Изменение температуры плавления при повышении давления на 1 Н/м2равно 3,94·10–7град/Па. Вычислить разность удельных объемов ромбической и моноклинной сера.
Объясните, пожалуйста, как решать данную задачу ?
 ?
?
-
Определите максимальное число фаз и число степеней свободы равновесной системы.
4Fe+3O2=2Fe2O3
Пожалуйста, объясните как решать, и дайте формулы для решения. ???
Я нашел формулу для числа степеней свободы: f=К-Ф+2, где К компоненты и Ф фазы.
Число компонентов К,
К = s - n - m ,
где s - число веществ,n - число независимых химических реакций,m - число соотношений между концентрациями веществ или составами фаз.
к= 3-1-0=2 (вроде)
Но как найти число ФАЗ не понимаю. -
6 часов назад, M_GM сказал:
Замечательно

Но, в заключение признаюсь, что я тут несколько затупил и напрасно усложнил решение задачи.
На самом деле, все эти переходы к концентрациям, Па - МПа, и обратно были ... совершенно не нужны!
Достаточно было поработать с уравнением реакции на языке давлений, как то так:
Предположим, что к моменту равновесия израсходуется определенное число моль C2H6,
в результате его парциальное давление уменьшится на х МПа.Тогда по уравнению реакции образуется столько же моль C2H4 и H2,
а значит, их давление возрастет на такую же величину, на х Мпа!
В результате равновесные давления веществ в системе будут равны:
р(C2H6)=(0,5-х) МПа; р(C2H4)=(0,25+х) МПа; р(H2)=(0,5+х) МПаПодставляем эти концентрации в выражение для Кр:
Кр = (0,25+х)*(0,5+х)/(0,5-х) = 34,4
и получаем уравнение с одним неизвестным, находим х и равновесные давления веществ.
Вот так
 !
!
Зато вспомнили связь давлений и концентраций, Кр и Кс


(0,25+х)*(0,5+х)/(0,5-х) = 33,4 (Кр по условию 33.4, вы наверное перепутали)
х=0.9727
р(C2H6)=(0,5-9727)= -0.4728 МПа;
р(C2H4)=(0,25+9727)= 1.2228 МПа;
р(H2)=(0,5+9727)= 1.4728 МПа
"Но, в заключение признаюсь, что я тут несколько затупил и напрасно усложнил решение задачи.
На самом деле, все эти переходы к концентрациям, Па - МПа, и обратно были ... совершенно не нужны!
Зато вспомнили связь давлений и концентраций, Кр и Кс

 "
"
Для меня это наоборот хорошо, с этим дистанционным обучением ничего толком не объяснили. Так что, чем больше я сейчас вспомню/выучу/пойму тем лучше. Спасибо.
-
10 минут назад, M_GM сказал:
Хорошо, может стоило посчитать чуть поточнее: х =0,03825.
Остался последний штрих:
Вопрос задачи: "Определите ... парциальные давления компонентов системы в конце процесса"
Эти давления нужно рассчитать, снова используя связь p=CRT ( и перевести обратно в МПа)
С(C2H6)=0.002*8.314*1500= 24.9 кПа=0.025 МПа
С(C2H4)=0.058*8.314*1500= 723.3 кПа=0.72 МПа
С(H2)=0.078*8.314*1500=972.7 кПа=0.97 МПа-
 1
1
-
-
1 час назад, M_GM сказал:
Неправильный перевод давления 1 МПа (106 Па) = 1000 кПа (103 Па). Да они еще и перепутаны.
Поэтому все концентрации будут в 1000 раз меньше, соответственно 0,04 моль/л и 0,02 моль/л
С константой думаю тоже промашка. Видимо она была посчитана в МПа,
переходя к кПа ее нужно наоборот умножить на 1000: Кс = 2,6
Теперь можно рассчитывать по уравнению реакции - это одна строчка:
Предположим, что к моменту равновесия прореагирует х моль C2H6 в каждом литре системы.
Тогда по уравнению реакции в каждом литре системы образуется х моль C2H4 и х моль H2;
В результате равновесные концентрации веществ в системе будут равны:
С(C2H6)=(0,04-х) моль/л; С(C2H4)=(0,02+х) моль/л; С(H2)=(0,04+х) моль/лПодставляем эти концентрации в выражение для Кс:
Кс = (0,02+х)*(0,04+х)/(0,04-х) = 2,6
Получаем уравнение с одним неизвестным,
из которого любой знаток школьной математики немного попыхтев найдет х(0,02+х)*(0,04+х)/(0,04-х) = 2,6
х=0.038
С(C2H6)=(0,04-0.038)=0.002 моль/л;
С(C2H4)=(0,02+0.038)= 0.058 моль/л;
С(H2)=(0,04+0.038)= 0.078 моль/л
-
28 минут назад, M_GM сказал:
Если ты не знаешь, где опечатка, будем считать, что в уравнении всё правильно, а в условии надо считать, что "P(C2H4)=0,25"
Это сделает решение чуть проще.
Чтобы вести расчёты далее, надо от давлений переходить к концентрациям, от Кр переходить к Кс.
Соответствующие формулы известны: С = p/RT и Kc = Kp/(RT)Δn, где R - универсальная газовая постоянная, Т - температура по шкале Кельвина, Δn - изменение числа молей в ходе реакции, для нашего случая Δn=1.
Вот тебе задача: Первое: для исходного состояния рассчитать по суммарному давлению суммарную концентрацию всех веществ в системе Ссум. Давление лучше брать в кПа, тогда концентрация будет в моль/л.
И второе - рассчитать значение Кс для этой реакции.P(C2H4)=250 000 кПа P(H2)(C2H6)=500 000 кПа
С(C2H4)=250 000/(8.314*1500)=40.1 моль/л
С(H2)(C2H6)=500 000/(8.314*1500)=20.05 моль/л
Ссум=40.1+40.1+20.05=100.25 моль/л
Кс=33.4/(8.314*1500)=0.0026 моль/л -
42 минуты назад, M_GM сказал:
"Продуктов реакции" - это верно, а значит вы ответили на первый вопрос задачи "Определите направление процесса" - реакция идет в сторону образования продуктов реакции.
"Если их увеличить до 16.7, то 16.7/0.5=33.4" - а это так просто не делается. Ведь если концентрация продуктов возрастает, то из чего они получаются? Значит концентрация и давление исходного вещества тоже изменится и никаких 0,5 там не будет.
Придется вести расчеты по уравнению реакции.
О-о-о!
 Только сейчас я заметил, что уравнение реакции у тебя не соответствует данным!
Только сейчас я заметил, что уравнение реакции у тебя не соответствует данным!
Что дано: "P(C2H2)=0,25" А в уравнении какой продукт: "=C2H4 + ..."
Может есть смысл заглянуть в условие и проверить, где написано правильно???
"Что дано: "P(C2H2)=0,25" А в уравнении какой продукт: "=C2H4 + ...""
Забыл написать (исправить) это опечатка в сборнике, при переносе не исправил.
Спасибо, что объясняете.
Так как вести расчеты по уравнению реакции? -
39 минут назад, M_GM сказал:
Неверно!
Кусл=(P(C2H4)*P(H2))/P(C2H6)=...
"Реакция идет в направлении увеличения концентрации." Концентраций каких веществ?
(P(C2H4)*P(H2))/P(C2H6) - Числитель или знаменатель этой дроби должен увеличиться, чтобы ее значение приблизилось к значению К=33,4??
Концентрации (а значит и давления) каких веществ должна увеличиться? Исходных или продуктов реакции?
"Концентрации (а значит и давления) каких веществ должна увеличиться? Исходных или продуктов реакции?"
Продуктов реакции. Если их увеличить до 16.7, то 16.7/0.5=33.4 -
17 часов назад, M_GM сказал:
Выражение для константы равновесия через парц. давления ты сам должен знать
и формулу для нее писать в лёгкую. Вот с этого и начни.А потом подставляй в эту формулу исходные давления и считай, что получится,
сравнивай результат с константой. Он больше или меньше?
Процесс будет идти в том направлении,
чтобы этот результат приближался к константе за счет протекания реакции,а значит изменения текущих концентраций
Их расчёт - это уже следующий этап решения.
Спасибо огромное.
К=(P(C2H4)+P(H2))/P(C2H6)=(0,25+0,5)/0,5=1,5
Кр>К
Реакция идет в направлении увеличения концентрации.
Что дольше? Заранее спасибо. -
Здравствуйте, пожалуйста, проверьте правильность решения данной задачи. Если, что-то не так скажите. Заранее спасибо.
Найти соотношение констант равновесия при 500К и 600 К для реакции
HgCl2 + 2KBr=HgBr2 + 2KCl,
если тепловой эффект этой реакции составляет 16,8 кДж.
Решение:
HgCl2(кр)+2KBr(кр)=HgBr2(кр)+2KCl(кр)ΔH=(H(HgBr2)+2*H(KCl))-(H(HgCl2)+2*H(KCl))=(-169,9+2*(-436,56))-(-228,24+2*(-393,5))=-27,48
K=(ΔH*dT)/(8,413*T2)
где, dT=16,8
K=0,00015
K=0,00022
K2/K1=1,46 -
Константа химического равновесия Кр реакции
С2H6=C2H4 + H2
при 1500 К равна 33,4. Определите направление процесса и парциальные давления компонентов системы в конце процесса, если в начале реакции их значения следующие (МПа) : P(C2H6)=0,50,P(C2H2)=0,25,P(H2)=0,50
Пожалуйста, объясните как решать, и дайте формулы для решения.??? -
Формула дипальмитоолеата. Напишите ее пожалуйста.
-
Помогите пожалуйста с органической химией. Прорешал все тестовые задания, кроме этих. Тут или вообще не знаю или предполагаю, но очень не уверен. Заранее спасибо.
5. В схеме превращенийH2CH3COOH
CH3CHO→ X1 →--------------- → X2 веществом Х2 является
а) диэтиловый эфир; б) глицерин; в) этилацетат; г) диметиловый эфир?
6. С помощью какого реагента можна отличить целобиозу от сахарозы?
а) бромная вода гидрогенизация; б) раствор щелочи; в) оксид меди (1); г) реактив Фелинга? Тут вроде, А.
9. Наименьшей основностью обладает соединение
а) аммиак; б) анилин; в) метиламин; г) диметиламин. Тут вроде, А.
9. Реакция, протекающая с участием гидроксильных групп в молекуле галактозы
Nit0
а) С6Н12О6 + H2→?; б) С6Н12О6+ [Ag(NH3)2]OH→?; в) С6Н12О6 + Cu(OH)2+ NaOH→?;
в) С6Н12О6+ Br2+ H2O →?
9. С помощью какого реагента можна отличить лактозу от трегалозы?
а) оксид меди (I); б) реактив Селиванова; в) реактив Фелинга; г) бромная вода.
10. Возможным продуктом реакции взаимодействия азотистой кислоты и первичного ароматичного амина будет:
а) С6Н5-N≡NCl; б) С6Н5-N=N-CH3; в) С6Н5-N-(C6H5)2; г) Н2N – C6Н12-NH2?
10. Укажите число асимметрических атомов углерода в молекуле 2-аминокапроновой кислоты
а) 0; б) 1; в) 2; г) 3; д) 4. Тут вроде, Б.
10. Реакция, при помощи которой можно отличить трипептиды фен-гли-ала и сер-гли-ала
а) с нитратом свинца (II); б) с нингидрином; в) биуретовая; г) ксантопротеиновая.
9. Назовите соединение:
смотрите прикрепленный рисунок
а) 2-метил-2-фенил-3-ол-пропанамин; б) 4-амино-2-фенилбутанол-3; в) 4-амино-2-бензилбутанол-3; г)1-амино-1-ол-3-метил- 3-фенилпропан. Тут вроде, Г.
-
Назовите углеводород:
2-метил-4-гексин; б) 5-метил-2-гексин; в) 5-метил-2-гептин; г) 5-метил-2-гептен.
-
-
-
Название соединения по международной номенклатуре соответствует
Н3С - С = СН - СН - СН2- ОН а) 2-метил-4-метилпентенол-3; б) 2,4-диметилпентен-3-ол-1; в) 1-гидрокси-2,4-диметилпентен-3; г) 2,4-диметилпентен-3-аль
| |
СН3СН3
-
22 часа назад, ash111 сказал:
а почему лимонную кислоту титруют солянкой? тут нет ошибки? щелочью же надо титровать.
неа, все один в один со сборником.
-
На кондуктометрическое титрование пробы, полученной из 3 г технического препарата лимонной кислоты, затрачивают 5,15 см3 0,0100 н раствора хлороводородной кислоты. Найти содержание (%) лимонной кислоты (молярная масса 192,13 г/моль) в анализируемом препарате.
-
Рассчитать навеску хлорида натрия, необходимую для приготовления 250 см3 0,0500 н раствора, используемого для установления титра раствора нитрата серебра.
Дайте формулу или скажите как, и я сам решу. Спасибо.
-
На кулонометрическое титрование уксусной кислоты генерированными ионами ОН- затрачивают 23 с при силе тока 8 мА. Общий объем анализируемого раствора 100 см3, для титрования отбирают 10 см3 раствора. Вычислить массу (мг) уксусной кислоты в анализируемом растворе.
Скажите как или дайте формулу, и я сам решу. Спасибо.
-
Вычислить объем 0,1000 н раствора AgNO3, который расходуется на титрование 25 см3 0,1034 н раствора бромида калия.
Скажите как или дайте формулу, и я сам решу. Спасибо.
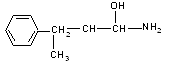
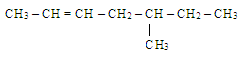
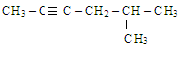
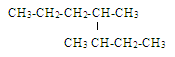
Время реакции в зависимости от температуры
в Решение заданий
Опубликовано
Спасибо большое