
ferrrrera
-
Постов
2 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Сообщения, опубликованные ferrrrera
-
-
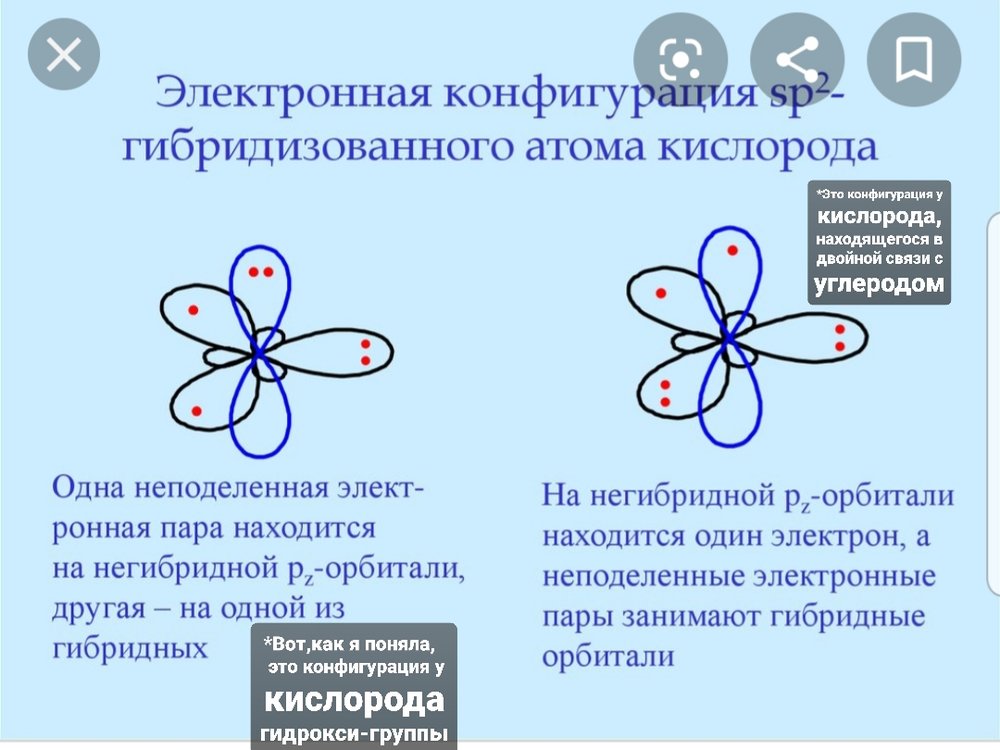
Здравствуйте! Пытаюсь познать органику, у меня возник такой вопрос при изучении строения карбоновых кислот, а в частности их карбоксильной группы.
Я поняла, что электронная плотность п-связи C-O смещается в сторону кислорода, так как он более электроотрицателен, и в итоге он принимает как бы отрицательный заряд, а у углерода, чей электрон смещён в сторону кислорода, остаётся положительный заряд.
И углерод этот положительный заряд пытается компенсировать.
Но я не понимаю за счёт чего именно.
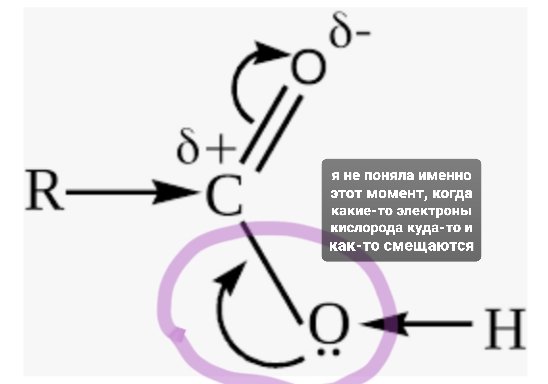
Он электронную плотность в о-связи с другим кислородом смещает в свою сторону(смещает электрон кислорода в свою сторону)? Или углерод пытается как-то забрать неподелённые электроны пары с негибридизированной p-орбитали у этого кислорода?
Или происходит что-то другое?
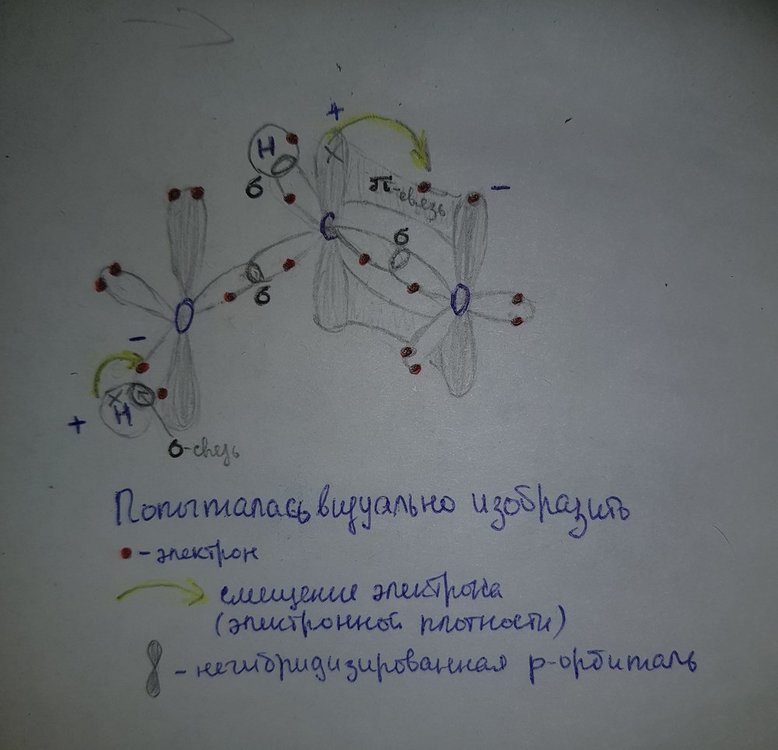
Но в итоге, насколько я поняла, потом уже кислород пытается компенсировать это смещением электрона водорода в свою сторону, и тем самым связь O-H приобретает большую полярность, водород остаётся с положительным зарядом, без электрона, становится более подвижным и способным к отщеплению => и при диссоциации образуется уже карбоксилат-ион, у которого электронная плотность распределяется более равномерно.
Как я поняла, за счёт этого они и считаются кислотами, так водород при диссоциации спокойно отщепляется.
Но главный вопрос, за счёт каких электронов/электрона компенсируется углерод? Откуда углерод забирает электрон(ы) у кислорода?
Простите, возможно я много чего перепутала, буду благодарна за разъяснение.. Не смогла найти чёткого и полного ответа на просторах интернета.
Заранее спасибо!


Гибридизация атомов в SO, SO2, SO3, S2O2
в Общий
Опубликовано · Изменено пользователем ferrrrera
Хотелось бы разобраться в гибридизации атомов в молекулах SO, SO2, SO3 и S2O2.
И если с SO2 у меня примерно получилось разобраться, и, как я поняла, у атомов серы и кислорода sp² гибридизация, у серы при этом происходит переход одного электрона с p-орбитали на d-орбиталь, и этот электрон на d-орбитали в связях не участвует, одна неподеленная пара остается на гибридизированной орбитали, а электроны с негибридизированных p-орбиталей у серы и двух атомов кислорода образуют резонансную структуру, где электроны делокализованы.
С гибридизацикй SO3 пока не очень понятно.
Но почему соединение SO нестабильно? Почему кислород и сера не делит две электронные пары с s- и p-орбиталей, образуя ковалентную связь? Но SO может существовать только в условиях пониженного давления и повышенной температуры, при повышении давления и понижении температуры из SO образуется S2O2. Почему? И какая гибридизация у атомов серы в этом соединении (S2O2)?