NelloN06
Пользователи-
Постов
107 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент NelloN06
-
-
В этом случае ответ тоже равен 2.5
-
Извиняюсь ,я допустил ошибку Если разложилось 80% вещества ,то останется 20% вещества. В таком случае полураспад равен: (t1/2)1=6.89 мин Если разложилось 85.7% вещества ,то останется 14.3% вещества В таком случае полураспад равен: (t1/2)2=11,404 мин а1 и a2 это конечное количество, вещества А,то есть 0.2 и 0.143 соответственно Подставляя в изначальную формулу находим ,что порядок реакций равен: n=2.5 Если сказано ,что реакция имеет целый порядок ,то нужно округлять до 3?
-
Я решил найти порядок через полураспад. [A]=0.8•[A]° 0.8[A]°=[A]°•exp{-kt} 0.8=exp{-ln2/t1/2•t} (t1/2)1=49.7мин 0.857[A]°=[A]°•exp{-kt} 0.857=exp{-ln2/t1/2•t} (t1/2)2=143,734мин Подставляя значения в эту формулу,вышло отрицательное число Можете подсказать правильное решение
-
r=k•PxH2•PyCl2 r=k•(2PH2)x•(4PCl2)y=2x+2y•kPxH2PyCl2=2x+2y•r 2x+2y=2 x+2y=1 В Ответе вышло 3/2 ,где я ошибся?
-
Прошу прощения,я имел в виду константа скорости
-
Как я понял k'-это константа скорости СО,k''-Cl2 То есть при высокой концентраций Cl2, константа СО не значительна и ее можно не считать?
-
Почему мольные доли?вы же считаете парциальные давления
-
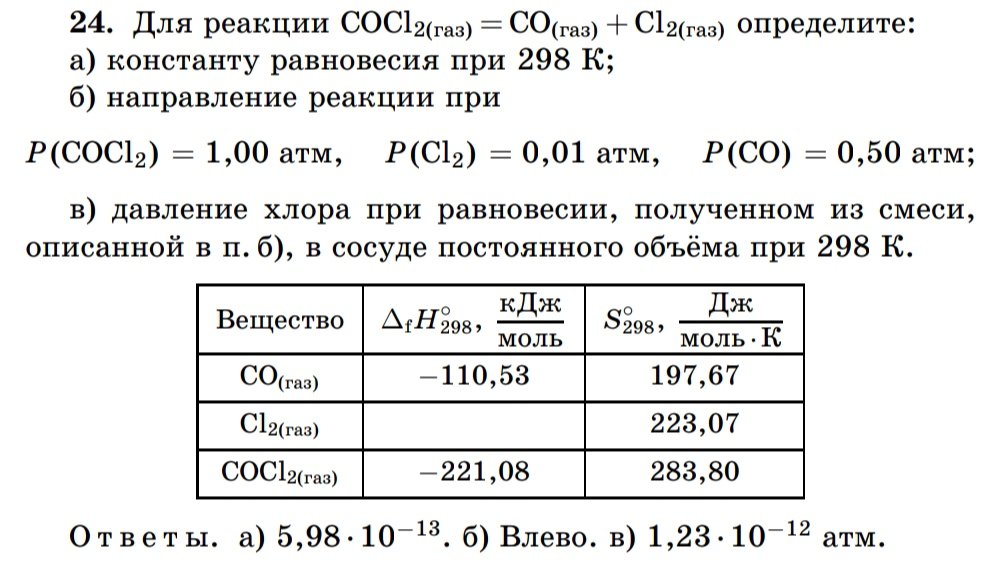
Как найти давление хлора в подпункте "В"?"давление хлора при равновесии, полученном из смеси описанной в п. б)"то есть имеют в виду чтобы мы использовали Кр из подпункта "б"?
-
Кстати ,константу не правильно посчитал, оказывается там 250°С. Кр=1,78,а так ответ выходит
-
-
m(спирта)=147,2г
-
Даже не подумал об этом Х(каждого продукта)=(0,5*0,4)/1=0,2 Х(каждого реагента)=(0,5-0,2)/1=0,3 Типа так?ответ же тогда не выйдет
-
Прошу прощения Х(каждого продукта)=(0,5*0,4)/1,4=0,14286 Х(каждого реагента)=0,5/1,4=0,35714 Кх=(0,14286)^2/(0,35714)^2=0,16 Кх=х^2/0,2х*1=0,16 х=0,032 m(этанола)=1,472,что в 100 раз меньше настоящего ответа Это из за процентов?
-
Хорошо нашел,а как затем найти массу спирта
-
При смешении по 0,5 моль 100%-х этанола и уксусной кислоты выход реакции этерификации составил 40%. Рассчи тайте константу равновесия. Какую массу этанола надо доба вить к 1 молю уксусной кислоты, чтобы в реакцию при этой же температуре вступило 20% спирта? CH3COOH+C2H5OH=CH3COOC2H5+H2O Kp=0,2^2/0,5^2=0,16 0,16=0,2^2/(x-0,2)*0,8 x=0,5125моль Где я ошибся?
-
Ага ,это я нашел n(газов)=1,41 моль 1,41=(1-x)+x+x X=0,41 Не знаю как найти Kр,а точнее парциальное давление
-
Один моль сероводорода поместили в сосуд объёмом 30 л и нагрели до 800°C. Давление в сосуде оказалось равным 420 кПа. Рассчитайте степень разложения сероводорода и константу равновесия Кр для реакции Н2S<->H2 +S.
-
Q3=Q1+Q2? Вы кажется CuSO4(р-р) и CuSO4•5H2O местами перепуталт
-
Но для этого нужно уравнение.Я примерно догадываюсь какие реакции проходят CuSO4(тв.)=CuSO4(р-р) CuSO4•5H2O(тв.)=CuSO4(р-р)+H2O CuSO4(тв.)+5H2O=CuSO4•5H2O(тв.) Я примерно представляю диаграмму,но не понимаю как ее построить
-
При растворении в воде 1 моль CuSO4 выделяется 66,5 кДж теплоты, а при растворении 1 моль CuSO4 . 5Н20 поглощается 11,93 кДж теплоты. Определите тепловой эффект процесса образования кристаллогидрата CuSO4.5Н2О из безводной соли. Можете подсказать ход решений,не могу понять как составлять уравнения
-
Теплота сгорания метана равна 800 кДж/моль, а этана 1500 кДж/моль. Сколько выделится теплоты (в кДж) при сго рании 150 л (н.у.) природного газа, содержащего только метан и этан и имеющего плотность 0,78 г/л? 16х+28у=117 х+у=150/22.4 Отсюда х=5.875,у=0,82 Q=(800*5,875)+(1500*0,82)=5930кДж в ответе вышло 5880.Это погрешность или я допустил ошибку?
-
Fe2S3+KMnO4+H2SO4=Fe2(SO4)3+MnSO4+K2SO4+H2O MnO4(-)+8H(+) +5e=Mn(2+)+4H2O S(2-)- 8e=S(6+) Как дальше уравнять ,и можно ли вообще писать серу?т.к. Fe2S3 разлагается в воде