Nikolay_t
Пользователи-
Постов
32 -
Зарегистрирован
-
Посещение
Тип контента
Профили
Форумы
События
Весь контент Nikolay_t
-
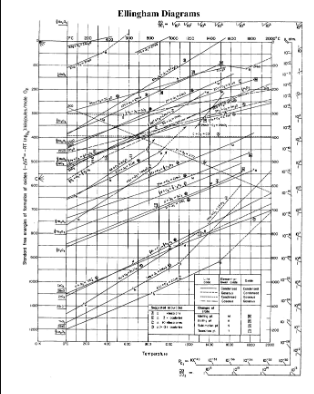
Что то в какие то дебри полезли, диаграмма Эллингема показывает сколько энергии выделится при окислении вещества?
-
Насколько я понял эн. Гиббса - это разность энтальпии веществ до и после реакции, диаграмма Эллингема - это зависимость этой разницы для различных оксидов от температуры.
-
Это если взяли холодные вещества. Меня интересует выход энергии без учета разогрева веществ, т.е. разогрели воздух и углерод до 1200, соединили и нужно знать сколько энергии выделилось.
-
Из диаграммы Эллингема. Ну дак она же нас и интересует (какая энергия выделится в процессе реакции окисления), или я неправильно ее понимаю?
-
Согласно диаграммы Эллингема реакция дальше не пойдет при 1200C, углерод будет восстанавливать СО2 до СО, точнее сказать только 1/1000 будет окислятся до СО2 (равновесная концентрация СО/СО2=1000/1 при такой температуре в присутствии С) Тоже из диаграммы Эллингема (480 кДж/моль вещества, которое окисляет О2, в реакции учувствуют 2С, т.е. 480/24 =20 кДж/гр) На диаграмме Эллингема как раз dH вроде бы, там почему то -240 тут я исходил что плотность воздуха 1,2 кг/куб. Если исходить из этих цифр, то полное сгорание такого кол-ва углерода даст 7,616 Мдж (32 МДж/кг, и оно не зависит от температуры), на 1200С на этапе С->СО выделяется 60% тепла, т.е. вообще 4,5 Мдж.
-
Пытаюсь понять сколько выделится тепла при неполном сжигании одного куб. метра воздуха об углерод. Реакция 2С+О2=2СО при 1200С дает 20 МДж на 1 кг углерода, или 15 МДж на кг кислорода (через соотношение молярных масс), в одном кубе воздуха 0,24 кг кислорода, т.е. на один куб воздуха выделится 3600 кДж, правильно ли я все посчитал?
-
Я не уверен, что это был вообще ЮТ, просто какая то советская статья. не, я собираюсь сделать по такому же принципу как КЭНы, толстые графитовые электроды выходят за пределы печки, внутри печки между ними тонкий стержень из батарейки, засыпан древесноугольной пылью, чтобы не горел, 3 таких стержня включены последовательно, каждый имеет сопротивление порядка 0,25 Ом в холодном состоянии (проверял сварочником), на 40В от сварочника должно быть где то 30А, в горячем ток будет расти. Стержни образуют букву П вокруг тигля.
-
Читал какую то статью чуть ли не из журнала ЮТ, где описывалась подобная печка, только там шихта закладывалась в графитовый порошок между коллекторных щёток, мне нужно было визуально смотреть что происходит в тигле, поэтому родилась такая конструкция. Если сверху засыпать корунд, то его бы надо было полметра для теплоизоляции, ну и в вате у меня было окно, через которое шихту закидывал. Слабым местом оказалась сажа, нужна без примесей, где взять не знаю, с озона опять не понятно что привезут, сейчас хочу попробовать в качестве нагревателей использовать стержни от пальчиковых батареек.
-
В общем ложная тревога, печка остыла - разобрал, все с ватой нормально, проблема была с чистотой материалов, сажей (П-803): на электродах и между ними куча зеленого вещества, думаю что это оксид хрома восстановился, так же сажа эта магнитится, в общем помимо сажи там куча примесей, с нее могло и натечь. С шихтой та же ситуация, видимо: использовал жезезооксиный пигмент, думал там только fe3o4, скорее всего не только. Конструкция такая: взял горшок от цветов, наспал сажи, утопил в нее алундовый тигель, вокруг него 4 графитовых электрода воткнуты в сажу, сверху вата, электроды к сварочнику. Горшок обмотал ватой, поставил в железный тазик. Температуру мерял термопарой S в чехле, но без нормального кабеля (медь) рядом с ней в тигле еще была термопара К показывала то же самое, да и по цвету 1300 там было (в литеных цехах бывал). Но вопрос по снижению огнеупорности (если оно вообще имеет место быть) теплоизоляции от восстановительной атмосферы остается открытым: даже если si02 восстанавливается, то концентрация al2o3 растет, т.е. огнеупорность должна тоже расти.
-
Проводил тут эксперименты с печкой, нагревателем которой является сажа, обнаружил что коалиновая вата, используемая в качестве теплоизоляции, натекла в тигель, температура там не поднималась выше 1300С, не могу понять с какой радости она плавится при такой температуре, al2o3-sio2 не должен плавится ниже 1585, скорее всего вата не понятно какая (куплена на озоне), но обнаружил на одном сайте вот такое: "Волокна устойчивы к воздействию температуры в окислительной и нейтральной средах. В восстановительной среде теплоизоляционные свойства снижаются.", как раз мая ситуация (раскаленный углерод дает восстановительную среду), но не могу понять почему, какая природа этого явления?
-
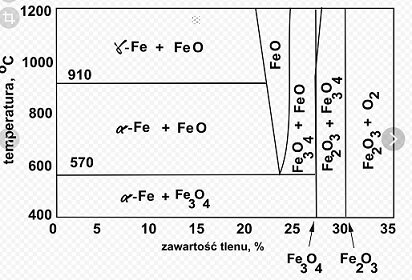
Открыл диаграмму Fe-O2, насколько я понимаю природный магнитит - это то, что показано стрелкой Fe3O4, если предположить что окалина находится левее, в районе 20%, то при нагревании вообще не образуется Fe3O4, может в этом дело?
-
Дак и я о том же, почему тогда не сыплют окомкованную окалину? Есть информация что сыплют в дуговую печь как окислитель, для производства агломерата, а вот чтобы в доменную сыпали - нету.
-
эээ, что то не понял, а где тогда их используют? Если что, я имею ввиду железорудные окатыши (не восстановленные).
-
Читал в википедии, что в Европе силикат кальция используется в качестве альтернативы асбесту, вероятнее всего китайцы, или еще кто, подхватили тему и шлепают плиты из гидравлического силиката, а огнеупорные плиты, скорее всего, из безводного, называются одинаково, химический состав тоже.
-
Я так понимаю это в дуговую печь, там окалина используется в качестве окислителя, у меня то в другом вопрос, почему окалину не используют в доменной печи?
-
Вроде бы тот же оксид железа, может же так же катать в окатыши и плавить, раз не делают значит есть какая то веская причина, нигде не могу найти информации по этому вопросу.
-
Т.е. питы делают из расплавленного силиката, или сплавлением? Тогда еще попутный вопрос: а почему тогда алюминат (огнеопорный цемент) не разваливается? там же тоже затворенная вода, тоже при нагревании гидрооксид кальция должен переходить в оксид?
-
Везде пишут что силикатный кирпич разваливается при нагреве более 500 град (я так понимаю CaOH разлагается), а плиты наоборот используются как огнеупорный материал, я так понимаю там именно оксид кальция, может кто знает как их делают? Что то не могу найти информации
-
Ключевой момент тут - "мешал", т.е. вокруг титана создаются потоки, которые его размывают, именно для этого инструмент обматывают стеклотканью, она доступу расплава не препятствует, но не дает расплаву омывать инструмент. За скорость растворения отвечает вот этот кусок диаграммы, чем она положе, тем быстрее растворяется, у железа вообще эвтектика 99,1 на температуре 655, поэтому сталь быстро растворяется, у титана и у хром с этим получше. А смачиваемость определяется диаграммой Эллингема, нижестоящие металлы смачивают вышестоящие из-за того что растворяют оксидную пленку, алюминий там почти ниже всех, поэтому он смачивает практически все, но сам при этом не смачивается, поэтому его трудно паять. Цинк и олово ниже меди, поэтому они смачивают медь при пайке.
-
Вот еще какая гипотеза в голову пришла: как известно оксидная пленка на нержавейке состоит из оксида хрома, когда алюминий восстанавливает этот оксид, то пленка превращается просто в хром, т.е. происходит хромирование, автоматически. Хром в алюминии растворяется очень медленно, возможно даже растворенный с поверхности хром успевает замещаться диффузионным из нержавейки, но при росте температуры скорость растворения растет, диффузия не поспевает и привет. Только вот я не понимаю как получить не более 700С на тигле: тигель же не может быть до краев заполнен, а в начале плавки он вообще пустой, спирали вокруг него 1300С, в общем та часть тигля, что не покрыта металлом, всяко разно должна быть больше 700 и сильно больше.